Содержание
- 2. Вспомните, какие вещества мы называем углеводородами? УГЛЕВОДОРОДЫ – это органические соединения, состоящие из двух химических элементов
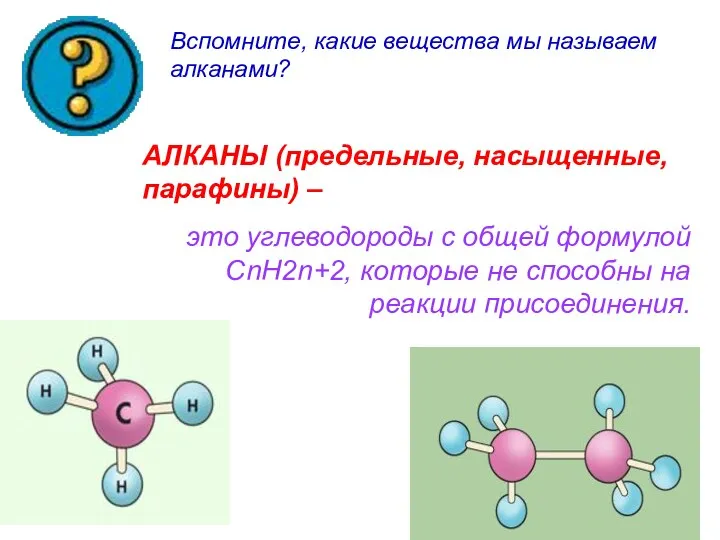
- 3. Вспомните, какие вещества мы называем алканами? АЛКАНЫ (предельные, насыщенные, парафины) – это углеводороды с общей формулой
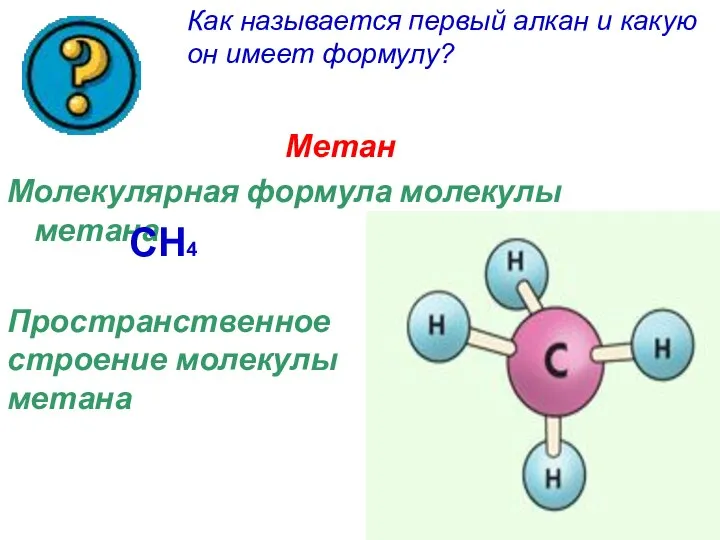
- 4. Метан Молекулярная формула молекулы метана CH4 Пространственное строение молекулы метана Как называется первый алкан и какую
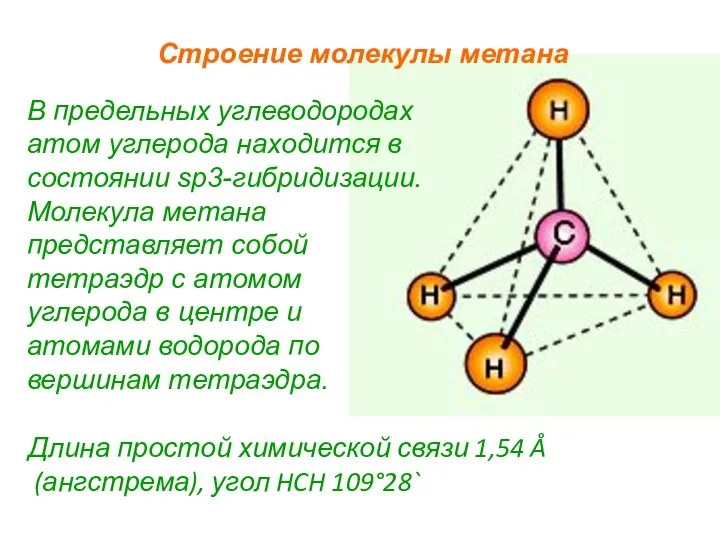
- 5. Длина простой химической связи 1,54 Å (ангстрема), угол HCH 109°28` В предельных углеводородах атом углерода находится
- 7. Тема урока «Физические и химические свойства алканов» Определение углеводородов Определение алканов Номенклатура алканов Физические свойства Химические
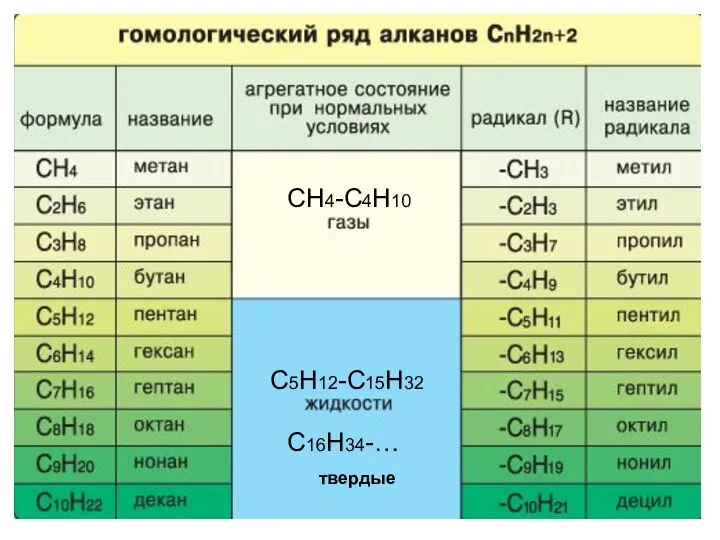
- 8. ГОМОЛОГИЧЕСКИЙ РЯД АЛКАНОВ Вспомните, какие вещества мы называем гомологами? ГОМОЛОГИ – это вещества со схожими строением
- 9. СН4-С4Н10 С5Н12-С15Н32 С16Н34-… твердые
- 10. Физические свойства Температуры плавления и кипения увеличиваются с молекулярной массой и длиной главной углеродной цепи При
- 11. ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ. МЕТАН – газ, без цвета и запаха, почти в 2 раза легче воздуха,
- 12. ЭТАН, ПРОПАН И БУТАН входят в состав природного и попутного нефтяного газов. АЛКАНЫ содержатся в нефти.
- 13. Химические свойства В обычных условиях алканы химически инертны. Они устойчивы к действию многих реагентов: не взаимодействуют
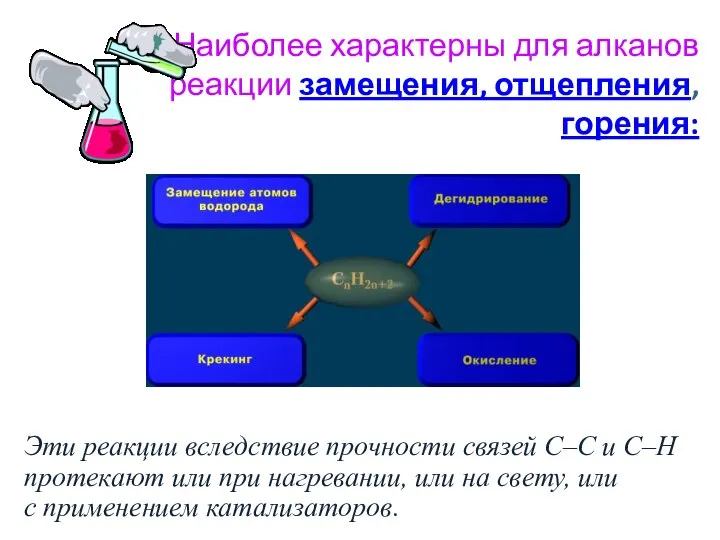
- 14. Наиболее характерны для алканов реакции замещения, отщепления, горения: Эти реакции вследствие прочности связей C–C и C–H
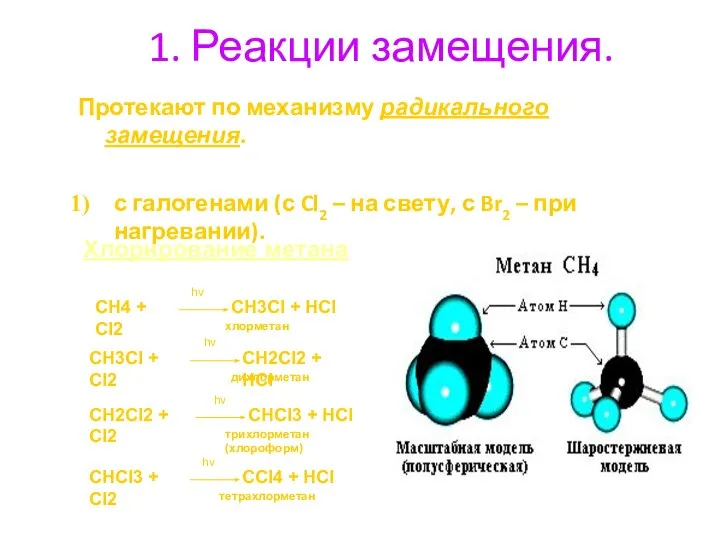
- 15. 1. Реакции замещения. Протекают по механизму радикального замещения. с галогенами (с Cl2 – на свету, с
- 16. Реакции галогенирования –замещение атома водорода атомом галогена. Замещение атома водорода галогеном легче всего идет у менее
- 17. CH4 + Cl2 → CH3Cl + HCl CH3Cl + Cl2 → CH2Cl2 + HCl CH2Cl2 +
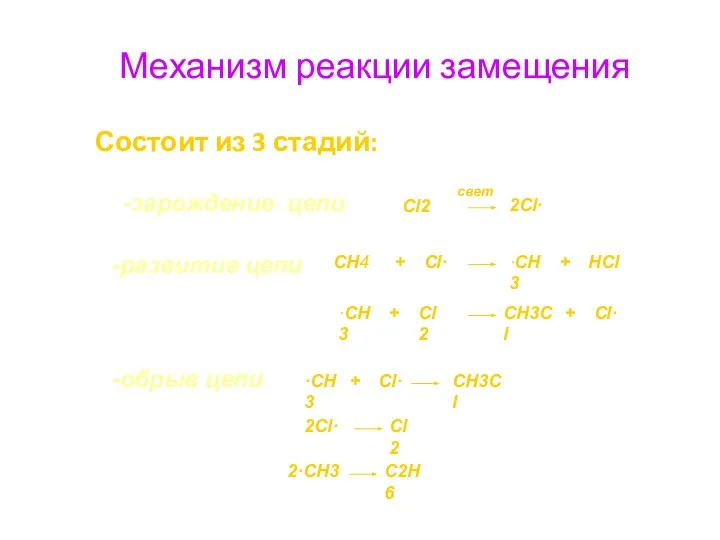
- 18. Механизм реакции замещения Состоит из 3 стадий: -зарождение цепи Cl2 2Cl· -развитие цепи CH4 + Cl·
- 19. Перед нами типичная цепная реакция… Теоретически хлорирование метана может идти до бесконечности, т.е. до тех пор
- 20. Запишите определение! Реакции, в результате которых происходит цепь последовательных превращений, называют цепными реакциями. (стр. 24)
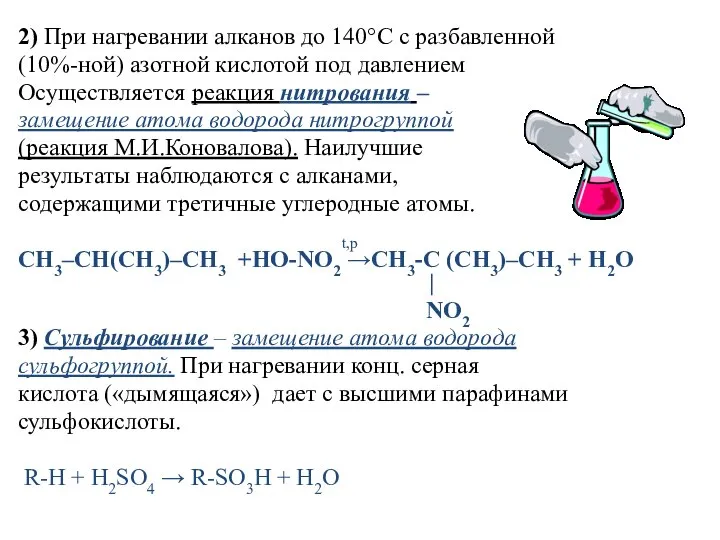
- 21. 2) При нагревании алканов до 140°С с разбавленной (10%-ной) азотной кислотой под давлением Осуществляется реакция нитрования
- 22. Запомните! Для алканов характерны реакции замещения атомов водорода на другие атомы или группы атомов. В этих
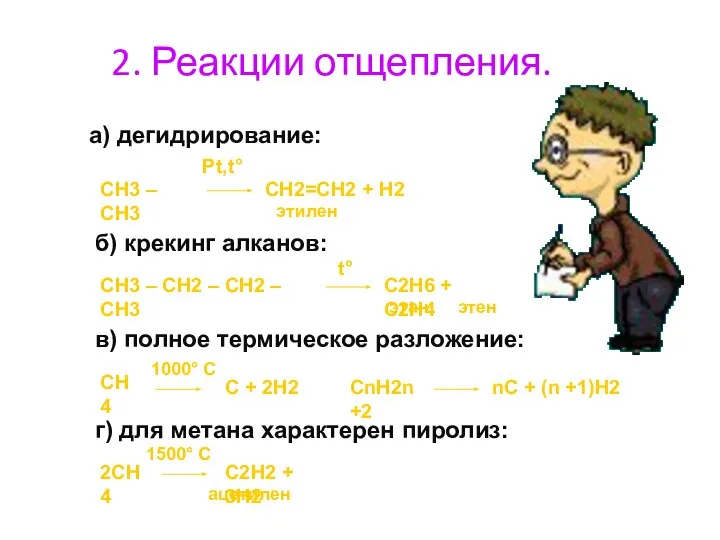
- 23. 2. Реакции отщепления. а) дегидрирование: CH3 – CH3 Pt,t° CH2=CH2 + H2 б) крекинг алканов: CH3
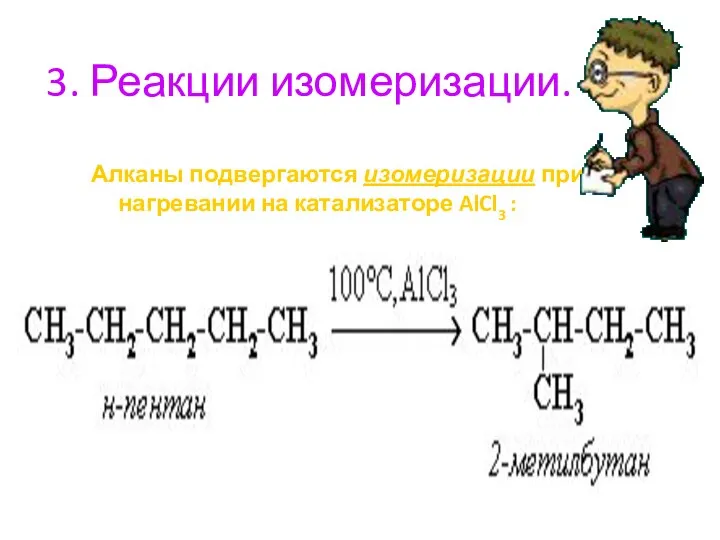
- 24. 3. Реакции изомеризации. Алканы подвергаются изомеризации при нагревании на катализаторе AlCl3 :
- 25. 4. Реакции окисления. а) все алканы горят с образованием углекислого газа и воды : б) при
- 26. Взрыв метана с кислородом Для полного сгорания метана на один объем метана нужно взять два объема
- 28. Запомните! Алканам характерны следующие химические реакции: 1. Реакции замещения; 2. Реакции отщепления; 3. Реакции изомеризации; 4.
- 29. Вопросы для самопроверки
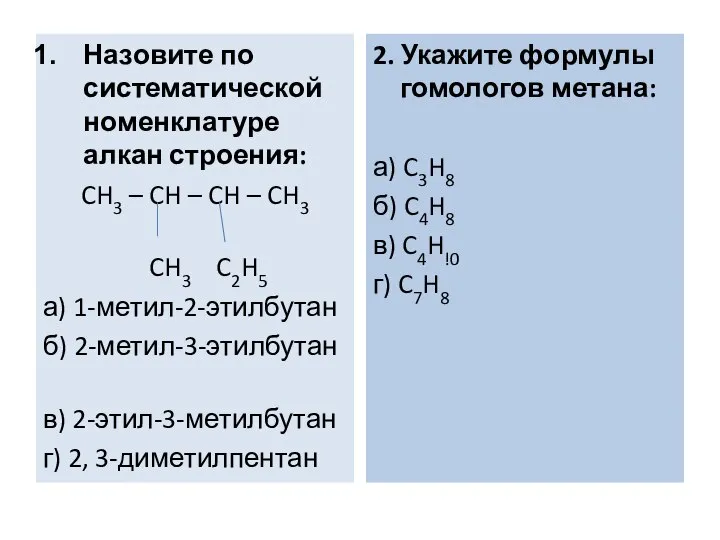
- 30. Назовите по систематической номенклатуре алкан строения: CH3 – CH – CH – CH3 CH3 C2H5 а)
- 31. 3. Каким соединениям даны неправильные названия? а) 2-метилпентан б) 2-этилбутан в) 1-метилпентан г) диметилбутан 4. Какое
- 32. 5. Какие характеристики применимы для описания реакции хлорирования этана? а) цепная б) свободнорадикальная в) протекает в
- 33. 7. В отличие от пропана бутан вступает в реакцию: а) горения в кислороде б) хлорирования при
- 34. Выставляем оценки Оценка «5» – Выполнено: 7 - 8 з.; Оценка «4» – Выполнено: 5 -
- 36. Скачать презентацию





















 Вычисление массовой доли элемента в молекуле
Вычисление массовой доли элемента в молекуле Жаңа синтетикалық есірткілер
Жаңа синтетикалық есірткілер Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах
Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах Периодический закон Д. Менделеева с точки зрения строения атома. Часть 1
Периодический закон Д. Менделеева с точки зрения строения атома. Часть 1 1_Лекція Комплексн
1_Лекція Комплексн Premeny látok. Požiar a jeho hasenie
Premeny látok. Požiar a jeho hasenie Презентация на тему Величие гениального творчества великого соотечественника
Презентация на тему Величие гениального творчества великого соотечественника  Биохимия статическая, динамическая, функциональная
Биохимия статическая, динамическая, функциональная Ovr-1
Ovr-1 Адсорбция на границе раствор-газ. ПАВ и ПНАВ
Адсорбция на границе раствор-газ. ПАВ и ПНАВ Реализация примерной адаптированной основной общеобразовательной программы по предмету Химия
Реализация примерной адаптированной основной общеобразовательной программы по предмету Химия Характеристика высших гидроксидов по положению в ПСХЭ
Характеристика высших гидроксидов по положению в ПСХЭ Агрегатные состояния вещества
Агрегатные состояния вещества Углеводороды: классификация
Углеводороды: классификация Лекарственные растения содержащие флавоноиды
Лекарственные растения содержащие флавоноиды Вода - самое удивительное вещество в природе. (8 класс)
Вода - самое удивительное вещество в природе. (8 класс) Термодинамика живого объекта. Основы биоэнергетики. Лекция 2
Термодинамика живого объекта. Основы биоэнергетики. Лекция 2 Процессы массопередачи в гомогенных средах
Процессы массопередачи в гомогенных средах Водород в природе. Получение водорода и его физические свойства. 8 класс
Водород в природе. Получение водорода и его физические свойства. 8 класс Галогены и их соединения
Галогены и их соединения Классификация неорганических веществ
Классификация неорганических веществ Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Классификация силикатов
Классификация силикатов Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Соли в свете теории электролитической диссоциации
Соли в свете теории электролитической диссоциации Вредна ли губная помада
Вредна ли губная помада Германий, его характеристика, способы получения органопроизводных, химические свойства. Практическое применение
Германий, его характеристика, способы получения органопроизводных, химические свойства. Практическое применение Кислотно-основное равновесие
Кислотно-основное равновесие