Слайд 2Процесс распада электролитов на ионы в водном растворе или расплаве называется электролитической

диссоциацией.
Положительные ионы называют катионами,
отрицательные ионы – анионами.
К катионам относятся: ион водорода и ионы металлов, катионы основных солей.
К анионам относятся: гидроксид-ион, ионы кислотных остатков, анионы кислых солей.
Слайд 3ДИССОЦИАЦИЯ КИСЛОТ:
H2SO4 → 2H+ + SO42-
HCl → H+ + Cl-
HNO3 → H+

+ NO32-
Слайд 4ДИССОЦИАЦИЯ ОСНОВАНИЙ:
NaOH → Na+ + OH-;
Ca(OH)2 → Ca2+ + 2OH-;

Слайд 5Диссоциация растворимых солей:
NaCI Na+ + CI-
AI2(SO4)3 2AI3+ + 3SO42-

Слайд 6ДИССОЦИАЦИЯ ВОДЫ:
Н2О → Н+ + ОН –
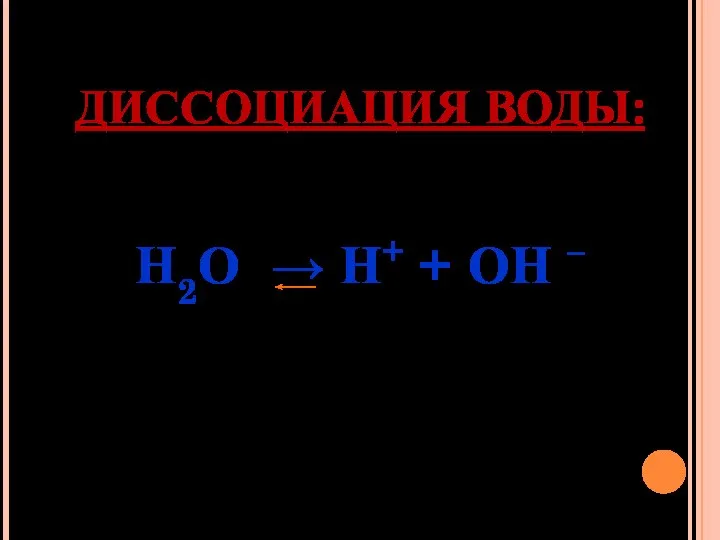
Слайд 7В чистой воде соотношение ионов водорода и гидроксид-ионов равное:
Н+ = ОН-
среда

нейтральная;
При добавлении кислоты равновесие нарушается:
Н+ > ОН-
среда раствора кислая;
При добавлении щёлочи:
Н+ < ОН-
среда раствора щелочная.
Слайд 8ГИДРОЛИЗ СОЛЕЙ
Гидролиз солей

Слайд 9ГИДРОЛИЗ -
от греч. «гидро» - вода,
«лизис» - разложение.

Слайд 10ГИДРОЛИЗ СОЛЕЙ –
реакция обмена между солью и водой,
приводящая к образованию

слабого
электролита.
Слайд 114 ТИПА СОЛЕЙ:
соль, образованная
сильной кислотой и слабым основанием (ALCl3);
сильным основанием и

слабой кислотой (Na2 S);
сильным основанием и сильной кислотой (NaCl);
слабым основанием и слабой кислотой (СН3СООNH4).
Слайд 12:
Соль, образованная сильной кислотой и слабым основанием.
AlCl3 → Al3+ + 3Cl-;
Н2О →

Н+ + ОН –;
Al3+ + Н+ + ОН – → AlОН2+ + Н+;
в растворе в свободном виде остался ион водорода (Н+), значит среда раствора кислая;
полное уравнение гидролиза:
AlCl3 + Н2О → AlОНCl2 + НCl;
Слайд 13Соль, образованная, сильным основанием и слабой кислотой.
Na2S 2Na++S2-
Н2О → Н+

+ ОН –;
S2- + H2O HS- + OH-
в растворе в свободном виде остался гидроксид ион ( OH-), значит среда раствора щелочная.
Полное уравнение гидролиза
Na2S + H2O NaHS + NaOH
Слайд 14Соль, образованная сильным основанием и сильной кислотой
КСl + Н2О ↔

КСl ↔ К + + Сl¯
Н2О ↔ OH¯ + H +
Все ионы остаются в растворе – гидролиз не происходит. Среда нейтральная, рН =7, т.к.
концентрации катионов водорода и гидроксид - анионов в растворе равны, как в чистой воде.
Слайд 15Соль, образованная слабым основанием и сильной кислотой.
CH3COONH4 CH3COO- +NH4+
Н2О → Н+

+ ОН –;
CH3COO- + NH4+ +H2O CH3COOH + NH3*H2O
CH3COONH4 + H2O CH3COOH + NH3*H2O
В этом случае гидролизу подвергаются как катион, так анион, образуются слабые электролиты, и среда раствора оказывается близкой к нейтральной или слабокислая, или слабощелочная, что зависит от констант диссоциации кислоты и основания.
Слайд 16Индикаторы –вещества, которые меняют окраску в зависимости от среды.

Слайд 17ИЗМЕНЕНИЕ ЦВЕТА РАЗЛИЧНЫХ ИНДИКАТОРОВ ПРИ ДЕЙСТВИИ РАСТВОРОВ КИСЛОТ И ЩЕЛОЧЕЙ
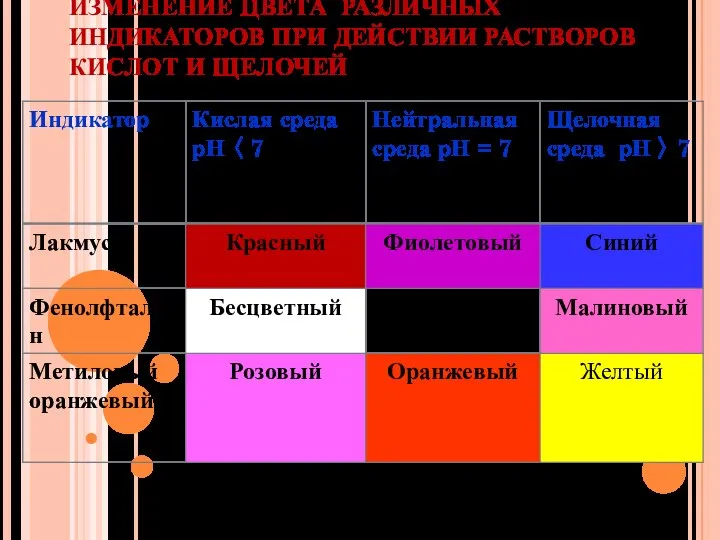
Слайд 18Демонстрационный опыт: к раствору соды Na2CO3 приливаем поочерёдно индикаторы лакмус и метилоранж,

Слайд 19
Вывод:
раствор соли, образованной слабым основанием и сильной кислотой имеет кислую среду.

Слайд 20КАКОЙ ВЫВОД МОЖНО СДЕЛАТЬ, ИСХОДЯ ИЗ СОСТАВА СОЛИ И СРЕДОЙ ЕЁ РАСТВОРА?
Раствор

соли, образованной сильным основанием и слабой кислотой имеет щелочную среду.
Слайд 21Вывод:
Среда нейтральная,т.к. не образуется слабый электролит;
такие соли гидролизу не подвергаются.

Слайд 23СИЛУ УМУ ПРИДАЮТ УПРАЖНЕНИЯ
1.Кислую среду имеет водный раствор:
а.Na3PO4
б.KCl

в.Na2CO3
г. ZnSO4
2.Щелочную среду имеет водный раствор:
а.FeCl3
б.K2SO4
в.Na2CO3
г.BaCl2
Слайд 24 3.Нейтральную среду имеет раствор:
а. Нитрата меди (II) Cu(NO3)2
б.Нитрата

бария BaNO3
в.Ацетата калия CH3COONH4
г.Карбоната натрия Na(CO3)2
4.Одинаковую реакцию среды имеют растворы карбоната натрия и
а.нитрата бария BaNO3
б.сульфита калия K2SO3
в.сульфата натрия Na2SO4
г.хлорида алюминия AICI3
Слайд 25 5.Кислую реакцию среды имеет каждый из двух растворов:
а.BaCl2 и ZnCl2

б.AlCl3 и FeCl2
в.FeCl3 и NaCl
г.KCl и CaCl2
6.Соль, образованная сильным основанием и сильной кислотой,
а.Гидролизуется по катиону
б.Гидролизуется по аниону
в.Не подвергается гидролизу
г.Полностью разлагается водой
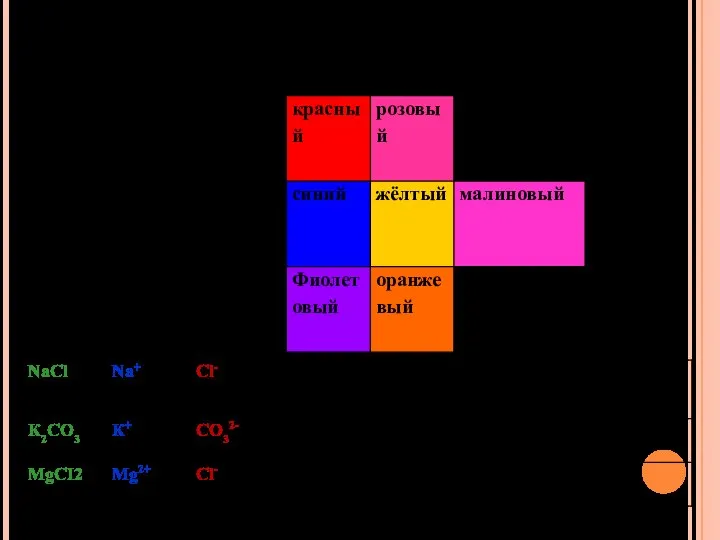
Слайд 267. Установите соответствие между составом соли и реакцией среды её водного раствора
Ответ:

Слайд 27 8. Установите соответствие между названием соли и средой её водного раствора.





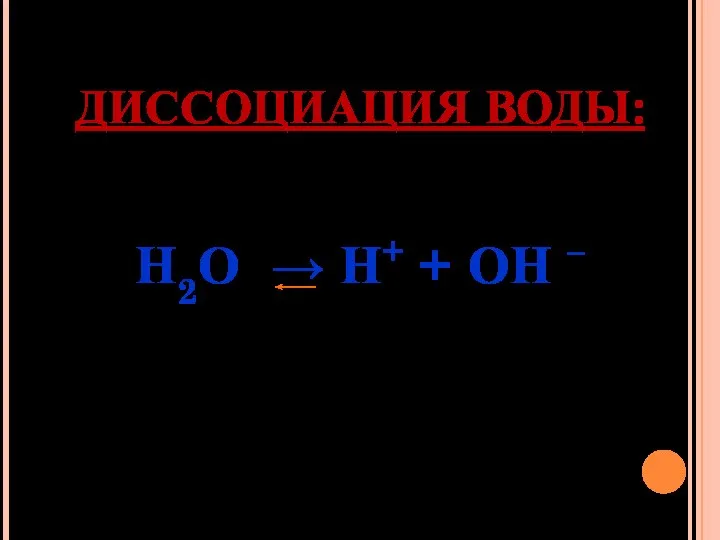




















 Получение кислорода. Практическая работа
Получение кислорода. Практическая работа Презентация на тему Нанотехнологии в химии
Презентация на тему Нанотехнологии в химии  Оксиды. 8 класс
Оксиды. 8 класс Строение электронных оболочек атомов элементов малых периодов
Строение электронных оболочек атомов элементов малых периодов Квантовая химия
Квантовая химия теория строения
теория строения Тестовая работа по теме: Реакции ионного обмена. Химия. 9 класс
Тестовая работа по теме: Реакции ионного обмена. Химия. 9 класс Химия в еде
Химия в еде Классификации по атомному весу
Классификации по атомному весу Вода. Строение молекулы воды. Анализ и синтез воды
Вода. Строение молекулы воды. Анализ и синтез воды Спирт и его влияние на организм человека
Спирт и его влияние на организм человека Коллоидно-химическая теория схватывания и твердения вяжущих веществ
Коллоидно-химическая теория схватывания и твердения вяжущих веществ Презентация по Химии "Токсическое действие неорганических веществ"
Презентация по Химии "Токсическое действие неорганических веществ"  Цикл Кребса
Цикл Кребса Кислоты в химии
Кислоты в химии Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов
Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов аналит хим
аналит хим Конкурс проектных работ Химический элемент … – и это все о нем
Конкурс проектных работ Химический элемент … – и это все о нем Оксиды
Оксиды Кристаллы и аморфные тела
Кристаллы и аморфные тела Спирты. Классификация, номенклатура, изомерия, получение и применение. 10 класс
Спирты. Классификация, номенклатура, изомерия, получение и применение. 10 класс Презентация по Химии "Химическая номенклатура и филология"
Презентация по Химии "Химическая номенклатура и филология"  Презентация на тему Барометр анероид
Презентация на тему Барометр анероид  Презентация на тему Алкины
Презентация на тему Алкины  Химия 11 класс
Химия 11 класс Классы неорганических веществ
Классы неорганических веществ Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов Материаловедение. Модуль
Материаловедение. Модуль