Слайд 2Закон постоянства состава
Жозеф Луи Пруст
Состав вещества молекулярного строения остается постоянным.
Независимо от

способа получения и места нахождения.
Слайд 3Что показывает химическая формула?
NH3,H2O,HCL,CH4.

Слайд 4РЕШИТЕ ЗАДАЧУ:
Определить формулу вещества, содержащего 43,4% натрия, 11,3 % углерода, 45,3%

кислорода
Слайд 5Определение
Валентность – это способность атомов удерживать при себе определенное число атомов других элементов.

Слайд 6Определение
Валентность – способность атома элемента образовывать связь с другими атомами за счёт

электронов, находящихся на внешнем энергетическом уровне.
Слайд 7ИЗ ИСТОРИИ ПОНЯТИЯ «ВАЛЕНТНОСТЬ»
В середине XIX века, когда были определены точные

относительные веса атомов (И.Я. Берцелиус и др.), стало ясно, что наибольшее число атомов, с которыми может соединяться данный атом, не превышает определённой величины, зависящей от его природы. Эта способность связывать или замещать определённое число других атомов и была названа Э.Франклендом в 1853 г. “валентность”. Поскольку в то время для водорода не были известны соединения, где он был бы связан более чем с одним атомом любого другого элемента, атом водорода был выбран в качестве стандарта, обладающего валентностью, равной 1.
Слайд 8Валентность элементов
Все элементы можно разделить на две группы:
C постоянной валентностью:
Одновалентны: H F Li

Na K
Двухвалентны: O Mg Ca Ba
Трехвалентны: Al B
Слайд 9Валентность элементов
C переменной валентностью:
Cu I II
Fe II III
S II IV VI
Cl I

III V VII
C II IV
P III V
N I II III IV
Слайд 10Как определить валентность других элементов?
Запоминать валентность каждого элемента необязательно. Достаточно посмотреть в

таблицу Менделеева. В периодической таблице высшей валентности соответствует номер группы. Низшую валентность можно узнать, отняв от восьми номер группы.
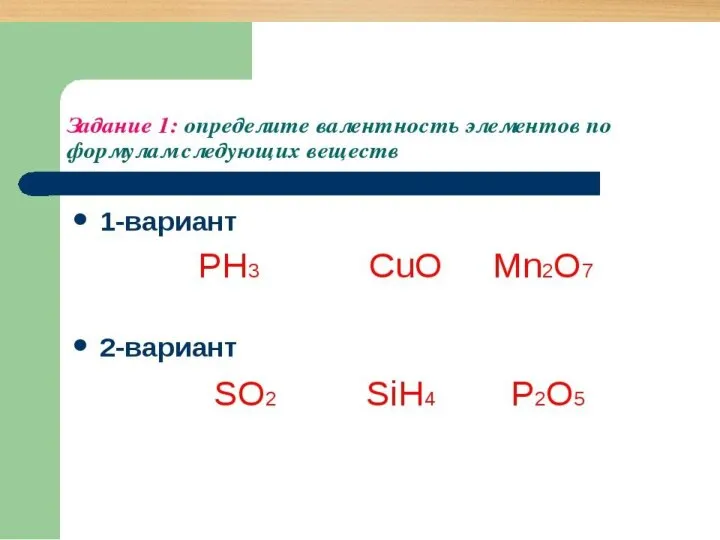
Слайд 15Упражнение 1.
Определите валентности .
Валентность элементов в соединениях с кислородом уменьшается в ряду

веществ, формулы которых:
1) Cr2O3 → MgO → СаО
2) К2О → ВаО → Cu2O
3) NO2 → NO → N2O
4) CuO → Cu2O → Mn2O7
Слайд 16Упражнение 2.
Определите валентности элементов в соединениях
1) CrO3 → Cr2O3 → CrO
2) N2O3 → NO →

N2O
3) СО2 → SiO2 → РbO2;
4) Na2O → MgO → Al2O3
Слайд 17Упражнение 3.
Валентность II селен имеет в каждом из двух веществ, формулы которых:
1)

SеO2 и SеO3
2) Н2Sе и СSе2
3) SеCl6 и SеCl4
Слайд 18Упражнение 4.
Определите валентности элементов в соединениях. В каком ряду валентности азота одинаковы?
1)

NO2 и N2О3
2) NH3 и K3N
3) Са3N2 и N2O
4) NCl3 и N2O5
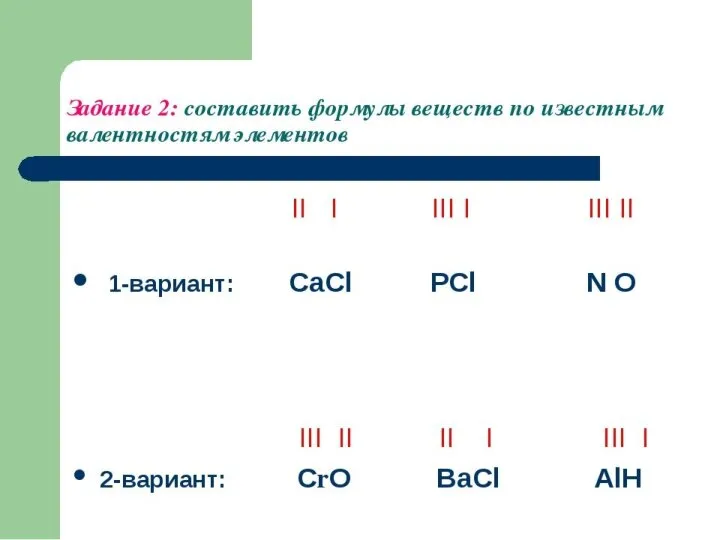
Слайд 19Упражнение 5.
Составьте формулы соединений фосфора с металлами, в которых фосфор проявляет валентность

III:
1) литием
2) кальцием
3) алюминием
Слайд 20Упражнение 6.
Составьте формулы соединений серы с металлами, в которых сера проявляет валентность

II:
1) калием
2) кальцием
3) алюминием
Слайд 21Упражнение 7
Пример H3PO4- валентность кислотного остатка III
К имеет постоянную валентность I
K3 PO4
Напишите

формулы Al Na Ca c остатками этой кислоты


















 Химические реакции в органике
Химические реакции в органике Химическая связь
Химическая связь Интеллектуальный турнир для старшеклассников Умножая таланты 2020
Интеллектуальный турнир для старшеклассников Умножая таланты 2020 Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка
Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка Поверхностные и массовые силы. Вывод уравнения неразрывности сплошной однокомпонентной среды
Поверхностные и массовые силы. Вывод уравнения неразрывности сплошной однокомпонентной среды Классификация кислот
Классификация кислот Подготовка к контрольной работе химические реакции 8 класс
Подготовка к контрольной работе химические реакции 8 класс Карбоновые кислоты
Карбоновые кислоты Радиоактивность. Тест
Радиоактивность. Тест Ионная химическая связь
Ионная химическая связь Презентация на тему Аммиак
Презентация на тему Аммиак  Каскадный синтез пептидов
Каскадный синтез пептидов Презентация на тему Расчеты по химическим уравнениям
Презентация на тему Расчеты по химическим уравнениям  Оксиды азота
Оксиды азота Азотосодержащие органические соединения
Азотосодержащие органические соединения Применение алкенов
Применение алкенов Презентация на тему Основные понятия химии
Презентация на тему Основные понятия химии  Типы химических реакций
Типы химических реакций Ортофосфорная кислота
Ортофосфорная кислота Окислительно - восстановительные реакции
Окислительно - восстановительные реакции Свойства аренов
Свойства аренов Физические свойства металлов
Физические свойства металлов Основания, их состав и название
Основания, их состав и название Свойства атомов. Типы связей
Свойства атомов. Типы связей Средства ухода за кожей
Средства ухода за кожей Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Exotermické a endotermické reakcie
Exotermické a endotermické reakcie Изучение основных породообразующих минералов горных пород. Лабораторная работа №1
Изучение основных породообразующих минералов горных пород. Лабораторная работа №1