Содержание
- 2. NH3 , H2S , PCI5 , SO3 , CS2 , Na3N , PH3 Упр. 1 Определить
- 3. II. Типы химических реакций - § 30-33 р. разложения р. соединения р. замещения р. обмена АВ
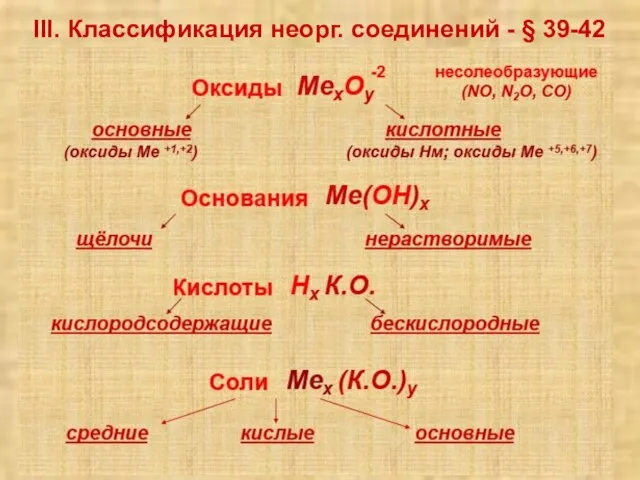
- 4. III. Классификация неорг. соединений - § 39-42
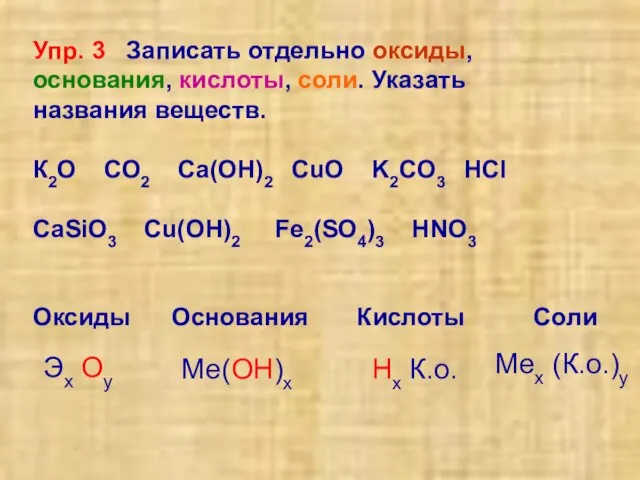
- 5. Упр. 3 Записать отдельно оксиды, основания, кислоты, соли. Указать названия веществ. К2О СО2 Са(ОН)2 СuO K2CO3
- 6. IV. Физические и химические явления - § 3 Упр. 4 Выписать только химические явления (хим. реакции):
- 8. Скачать презентацию



 Полиморфизм. Аморфные вещества
Полиморфизм. Аморфные вещества Природный газ
Природный газ Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах
Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах Язык химии. Знаки химических элементов
Язык химии. Знаки химических элементов Атомы химических элементов
Атомы химических элементов Положение галогенов в Периодической системе Д.И. Менделеева
Положение галогенов в Периодической системе Д.И. Менделеева Мезомерный эффект
Мезомерный эффект Состояния вещества. Тест. 5 класс
Состояния вещества. Тест. 5 класс Кислородные соединения азота, азотная кислота. Соли азотной кислоты. Удобрения
Кислородные соединения азота, азотная кислота. Соли азотной кислоты. Удобрения 564481
564481 Воздух
Воздух Побочная подгруппа VIII группы
Побочная подгруппа VIII группы 9 урок простые и сложные вещества
9 урок простые и сложные вещества Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома
Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома Химическое равновесие. Принцип Ле Шателье
Химическое равновесие. Принцип Ле Шателье Сложные эфиры. Жиры
Сложные эфиры. Жиры Металлическая и водородная и химическая связь
Металлическая и водородная и химическая связь Фотометрический анализ
Фотометрический анализ Фотографии к исследовательской работе в рамках конкурса УРАЛХИМиЯ
Фотографии к исследовательской работе в рамках конкурса УРАЛХИМиЯ Закон сохранения массы веществ
Закон сохранения массы веществ Вклад Д.И. Менделеева в науку
Вклад Д.И. Менделеева в науку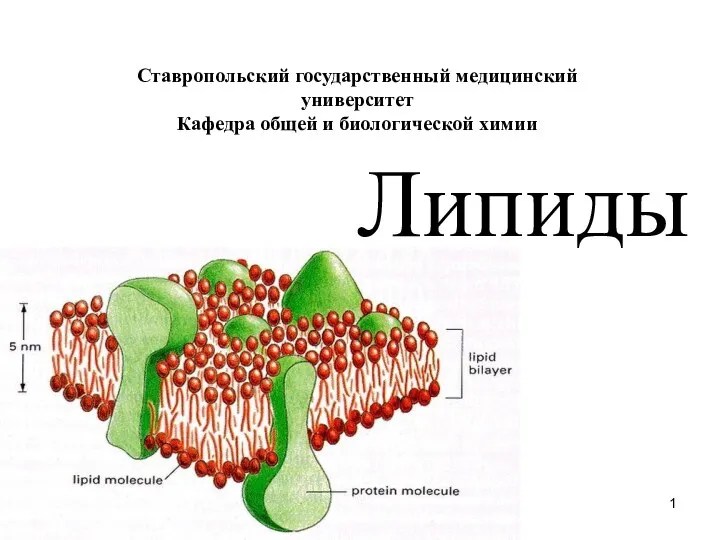 Липиды
Липиды Скорость химических реакций
Скорость химических реакций анлекция 3
анлекция 3 Проблемы и меры по защите окружающей среды ПМР
Проблемы и меры по защите окружающей среды ПМР Кислоты. Общая формула кислот
Кислоты. Общая формула кислот Строение вещества
Строение вещества