Содержание
- 2. Цель урока: Изучение закона сохранения массы вещества Задачи: Обучение учащихся составлению уравнений химических реакций Усвоение учащимися
- 3. М.В.Ломоносов в 1748 г. впервые сформулировал, а в 1756 г. экспериментально доказал закон сохранения массы веществ
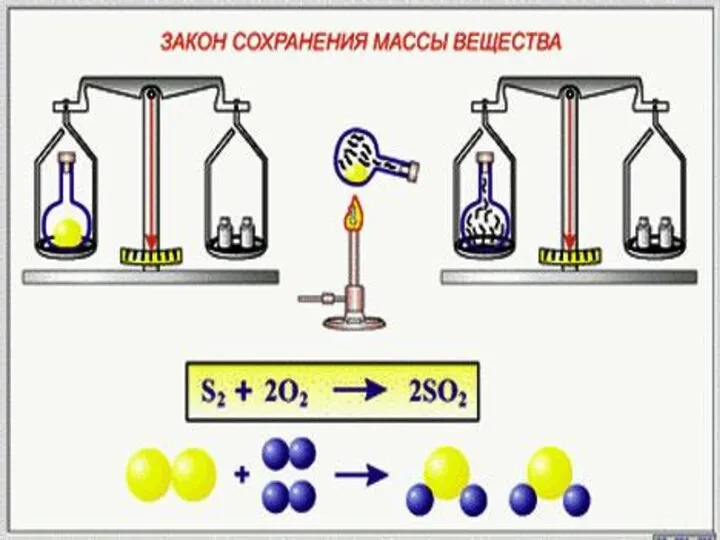
- 5. Формулировка закона Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ
- 6. Сосуд Ландольта
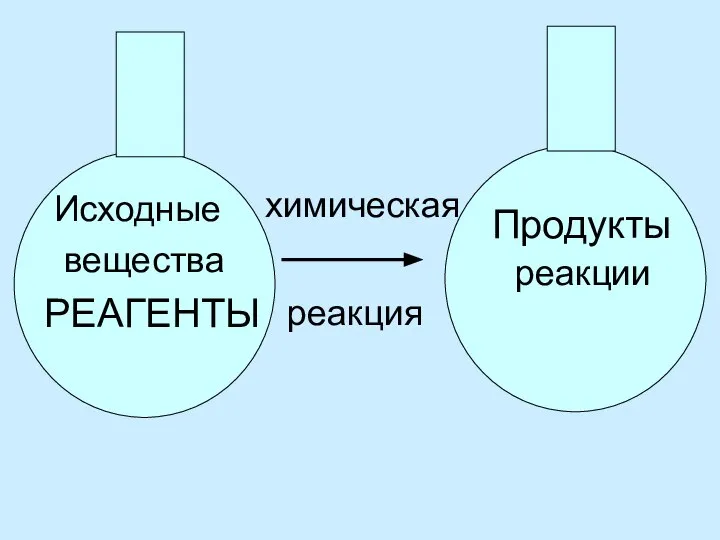
- 7. Исходные вещества РЕАГЕНТЫ химическая реакция Продукты реакции
- 8. Атомы не появляются и не исчезают при химической реакции
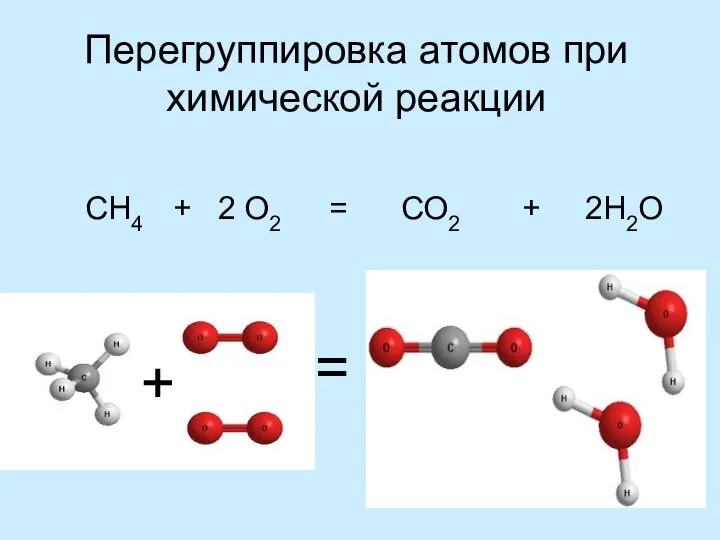
- 9. Перегруппировка атомов при химической реакции СН4 + 2 О2 = СО2 + 2Н2О + =
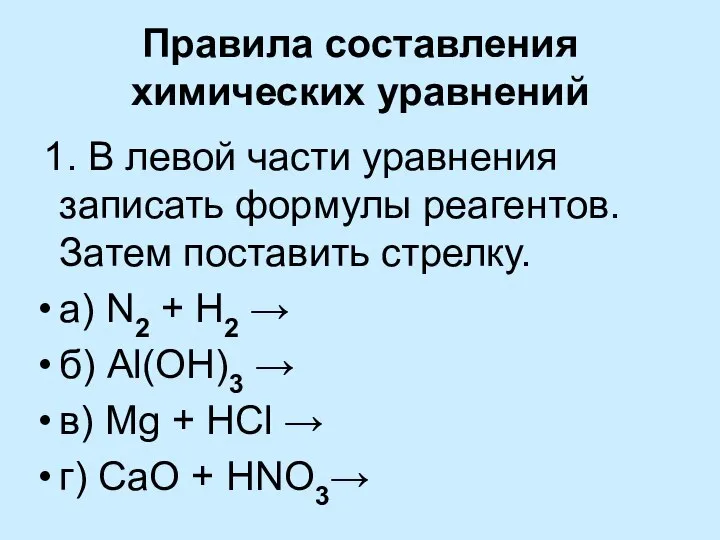
- 10. Правила составления химических уравнений 1. В левой части уравнения записать формулы реагентов. Затем поставить стрелку. а)
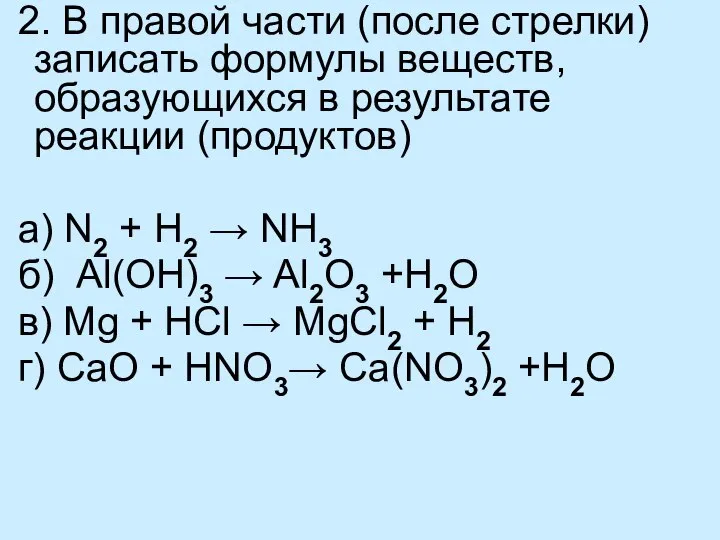
- 11. 2. В правой части (после стрелки) записать формулы веществ, образующихся в результате реакции (продуктов) а) N2
- 12. 3. Уравнение реакции составляется на основе закона сохранения массы веществ, т. е. слева и справа должно
- 13. Алгоритм расстановки коэффициентов в уравнении химической реакции. 1. Подсчитать количество атомов каждого элемента в правой и
- 14. 4. Пересчитать количество атомов, при необходимости действия повторить. 5. Начинать лучше с атомов О или любого
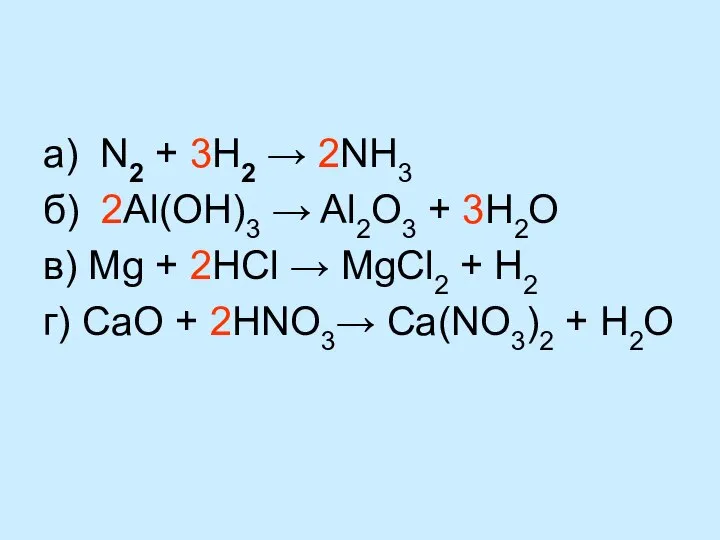
- 15. а) N2 + 3H2 → 2NH3 б) 2Al(OH)3 → Al2O3 + 3H2O в) Mg + 2HCl
- 17. Скачать презентацию








 Презентация на тему Обобщение знание и умений и предельных и непредельных углеводородах
Презентация на тему Обобщение знание и умений и предельных и непредельных углеводородах  Vvedenie_v_khimiyu
Vvedenie_v_khimiyu Цезій
Цезій Повторение по химии (8 класс)
Повторение по химии (8 класс) Презентация на тему Занимательная химия
Презентация на тему Занимательная химия  Щелочные металлы
Щелочные металлы Строение вещества
Строение вещества Химия крови. Состав и функции крови
Химия крови. Состав и функции крови Строение вещества
Строение вещества Этанол. Химические свойства этанола
Этанол. Химические свойства этанола Кислород
Кислород Закон постоянства состава веществ. Химические формулы. (8 класс)
Закон постоянства состава веществ. Химические формулы. (8 класс) Коррозия металлов. Способы защиты от коррозии
Коррозия металлов. Способы защиты от коррозии Повторение пройденного
Повторение пройденного Пластмассы
Пластмассы Кислоты. Что нас объединяет?
Кислоты. Что нас объединяет? Физико-химия поверхностных явлений в функционировании живых систем
Физико-химия поверхностных явлений в функционировании живых систем Какую воду мы пьем
Какую воду мы пьем Строение молекул. Метод валентных связей. Лекция 5
Строение молекул. Метод валентных связей. Лекция 5 Лекарственные средства – производные пиримидина
Лекарственные средства – производные пиримидина Презентация на тему Моющие средства
Презентация на тему Моющие средства  Углеводороды. Урок-игра
Углеводороды. Урок-игра Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории
Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории Переваривание и всасывание липидов. Транспортные формы липидов в крови. Лекция № 7
Переваривание и всасывание липидов. Транспортные формы липидов в крови. Лекция № 7 Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb
Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb Обобщение металлов
Обобщение металлов Ð_еÑ_еÑ_огенное Ñ_авн (1)
Ð_еÑ_еÑ_огенное Ñ_авн (1)