Слайд 2Химическая связь - взаимодействие атомов, связывающее их в единую устойчивую систему (молекулу,

ион, кристалл и др.)
Слайд 3Если число электронов на внешнем уровне атома максимальное, то такой уровень называется

завершённым. Такие атомы не вступают в химическое взаимодействие при обычных условиях. Это благородные газы, находящиеся в главной подгруппе 8 группы Периодической системы.
Внешние электронные уровни атомов других хим. элементов являются незавершенными. Они стремятся довести его до 8-электронного.
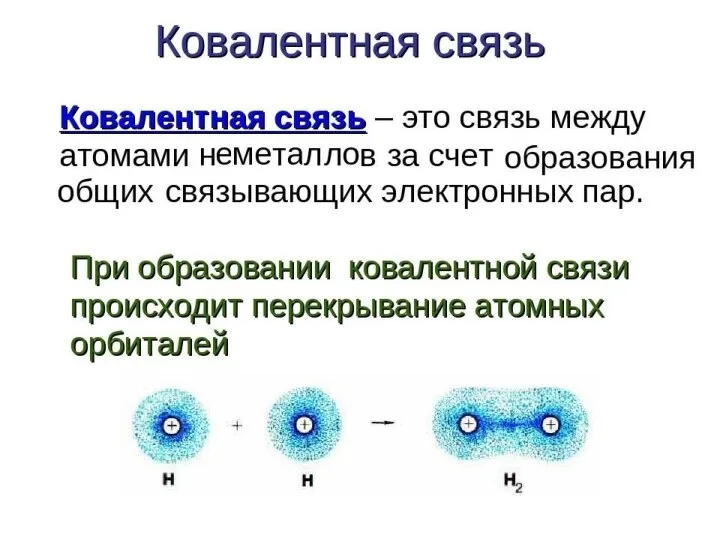
Электроны внешнего энергетического уровня являются валентными. При взаимодействии этих электронов образуется химическая связь.
В молекуле электроны становятся общими
Слайд 7Способы перекрывания электронных облаков:

Слайд 8Характеристики ковалентной связи:
Энергия связи – энергия, которую необходимо затратить для разрыва данной

связи. Измеряется в кДж/моль. Зависит от радиуса перекрывающихся облаков.
Кратность связи – число химических связей между двумя атомами. Её можно показать сплошной линией между атомами либо точками. Чем больше кратность связи, тем прочнее связь.
Длина связи – расстояние между ядрами атомов в молекуле. Измеряется в нм.
Полярность связи – смещение общей электронной плотность к более электроотрицательному атому. В зависимости от этого ковалентная связь делится на полярную и неполярную
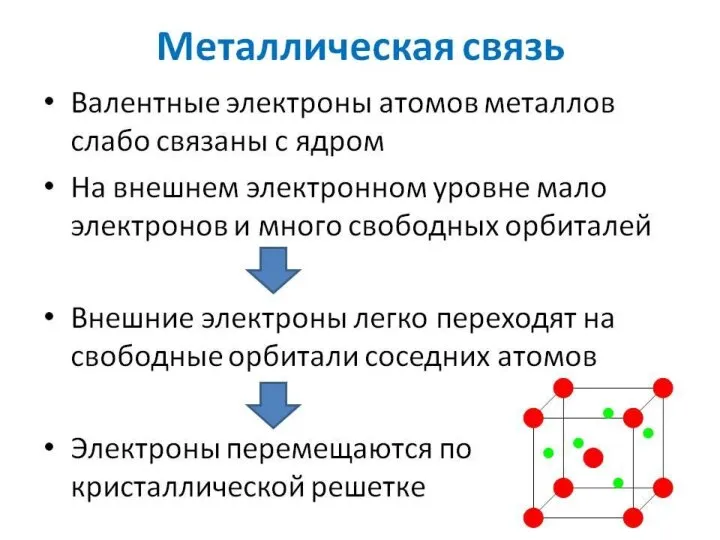
Слайд 11Металлическая связь - химическая связь в металлах и их сплавах, обусловленная наличием
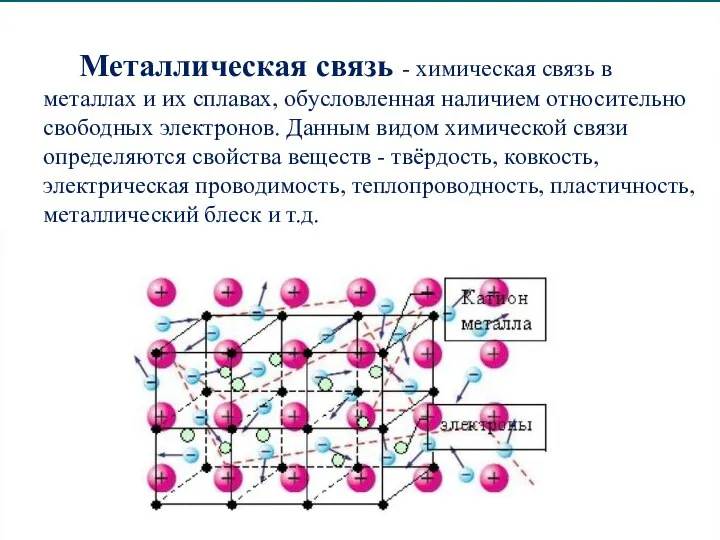
относительно свободных электронов. Данным видом химической связи определяются свойства веществ - твёрдость, ковкость, электрическая проводимость, теплопроводность, пластичность, металлический блеск и т.д.
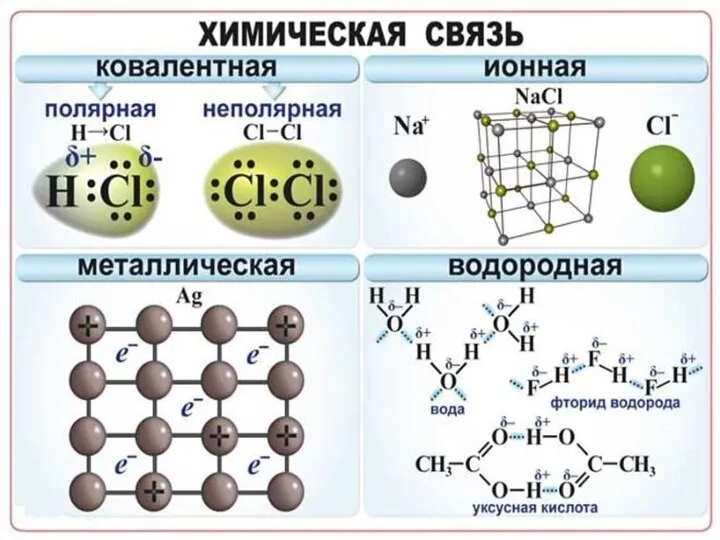
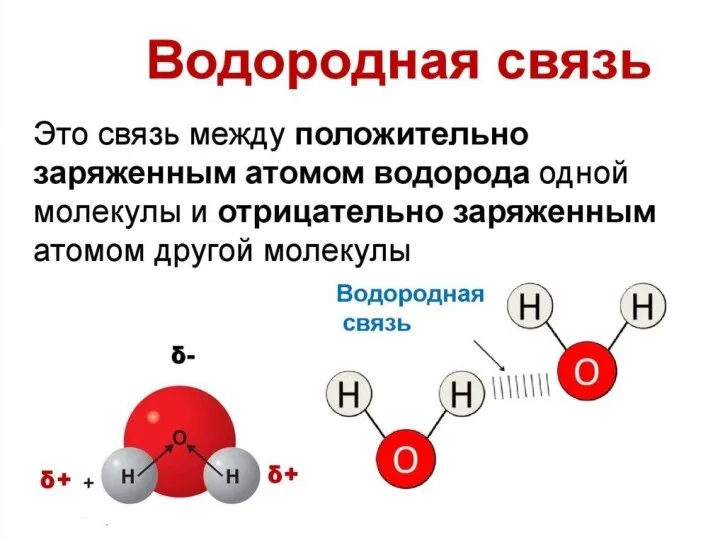
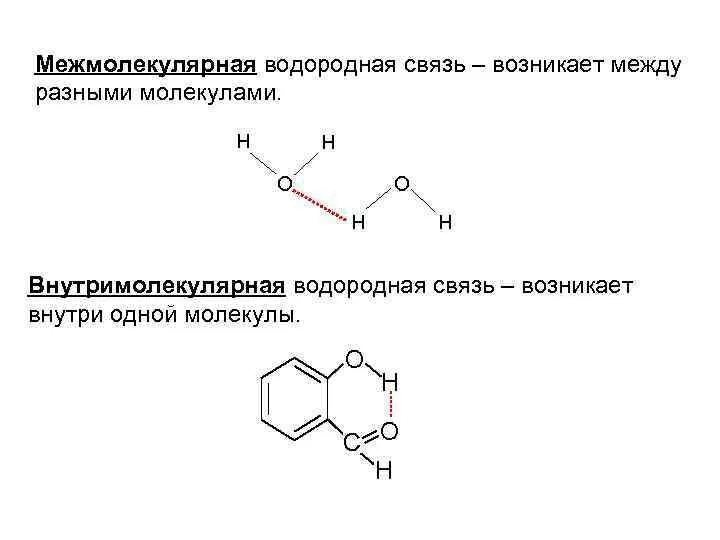
Слайд 15Наличие водородной связи обуславливает физические и химические свойства вещества - высокие температуры

плавления и кипения, хорошую растворимость, высокую испаряемость. Связь слабая и легко рвётся, но множество таких связей способно породить силу, на которой, в буквальном смысле, держится всё живое. Примеры соединений с водородной связью - спирты, карбоновые кислоты, амины, аминокислоты, белки, вода, аммиак, фтороводород










 Стекло. История открытия. Самое древнее производство Эпохи фараонов
Стекло. История открытия. Самое древнее производство Эпохи фараонов Значение химии в медицине
Значение химии в медицине «СберСтарЭнерго» «ЖИДКАЯ РЕЗИНА»
«СберСтарЭнерго» «ЖИДКАЯ РЕЗИНА» Физические свойства элементов 2 (ІІ) - группы
Физические свойства элементов 2 (ІІ) - группы Фенол. Понятие о фенолах
Фенол. Понятие о фенолах Анализ образца доломита методами аналитической химии
Анализ образца доломита методами аналитической химии Презентация на тему Уголь
Презентация на тему Уголь  Углеводы (сахара). Строение, свойства, участие в функционировании живых систем
Углеводы (сахара). Строение, свойства, участие в функционировании живых систем Строение вещества
Строение вещества Строение атома Степень окисления. Валентность. Ионы
Строение атома Степень окисления. Валентность. Ионы Количество вещества - моль
Количество вещества - моль Сплавы металлов (познавательная презентация)
Сплавы металлов (познавательная презентация) bc95487a97b0472591b20aef8d569081
bc95487a97b0472591b20aef8d569081 Алюминий
Алюминий Положение металлов в периодической системе Д.И. Менделеева. Физические свойства металлов
Положение металлов в периодической системе Д.И. Менделеева. Физические свойства металлов Вода… Химические названия
Вода… Химические названия Степень окисления. Бинарные соединения
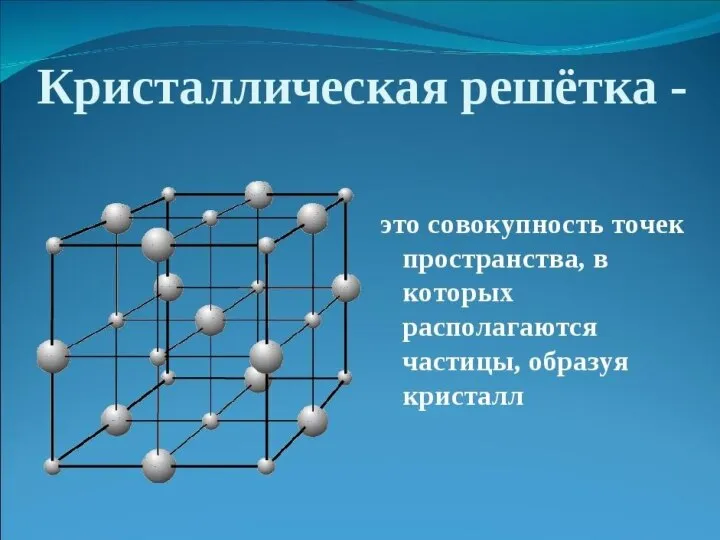
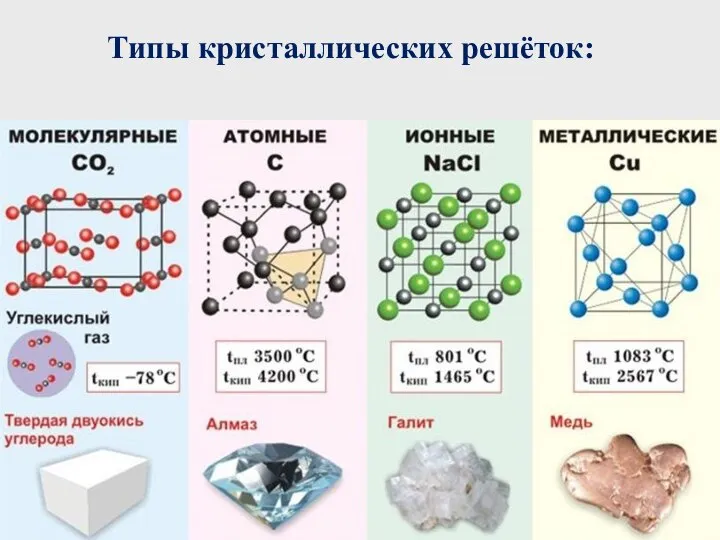
Степень окисления. Бинарные соединения Химическая связь. Типы кристаллических решёток
Химическая связь. Типы кристаллических решёток Химическое равновесие
Химическое равновесие Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Інструктаж з БЖД. Особливості органічних сполук (порівняно з неорганічними). Вуглеводні. Метан
Інструктаж з БЖД. Особливості органічних сполук (порівняно з неорганічними). Вуглеводні. Метан Основные понятия и законы химии
Основные понятия и законы химии Буферные растворы. Буферная емкость
Буферные растворы. Буферная емкость Введение в органическую химию. Состав и структура органических веществ
Введение в органическую химию. Состав и структура органических веществ Классификация коррозионных процессов металлов
Классификация коррозионных процессов металлов Переработка нефти. 10 класс
Переработка нефти. 10 класс Диагностическое тестирование по химии в 8 классе
Диагностическое тестирование по химии в 8 классе Консерванты, их виды и применение
Консерванты, их виды и применение