Содержание
- 2. Ионная связь: Рассмотрим пример образования бинарной ионной связи на примере хлорида натрия NaCl. Атом натрия передал
- 3. Ковалентная полярная связь: Прочитать и вспомнить
- 4. Степень окисления: Проанализировать по прочитанному на 2 предыдущих слайдах:
- 5. Степень окисления – условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что все
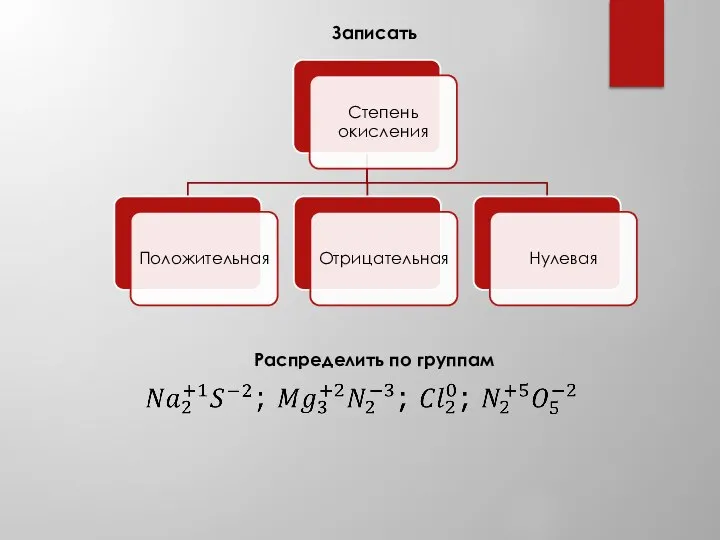
- 6. Записать Распределить по группам
- 7. Степень окисления: Отрицательное значение степени окисления имеют те атомы, которые приняли электроны от других атомов или
- 8. Отрицательная степень окисления: Записать
- 9. Степень окисления: Положительную степень окисления имеют те атомы, которые отдают свои электроны другим атомам или от
- 10. Положительная степень окисления: Степень окисления в соединениях с металлами: Степень окисления в соединениях с водородом: Записать
- 11. Нулевая степень окисления: Нулевую степень окисления имеют атомы простых веществ (ковалентная неполярная связь) и атомы в
- 12. Понятие валентность и степень окисления: Понятия степень окисления и валентность не одно и то же. Записать
- 13. Записать
- 14. Запиши правила определения степеней окисления (с.о.) 1) Степень окисления простых веществ и свободных атомов равна нулю
- 15. 4) Постоянные степени окисления: H +1 (кроме гидридов активных металлов, например:Na+1H-1) O-2 (кроме O+2F2, H2O2-1,пероксидов металлов)
- 16. Правило креста Правило креста: для составления химических формул по названию вещества надо записать соответствующие знаки химических
- 17. Алгоритм для составления формулы вещества: Записать знаки химических элементов рядом (сначала записывается менее электроотрицательный элемент). Определить
- 18. Составим формулу соединения карбида алюминия: Посмотреть пример
- 19. Составим формулу соединения оксида алюминия (III): Посмотреть пример 2
- 20. Название бинарных соединений: Записать
- 21. Составление формул по степени окисления Оксид натрия - Хлорид железа (III) - Нитрид магния - Оксид
- 23. Скачать презентацию



















 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ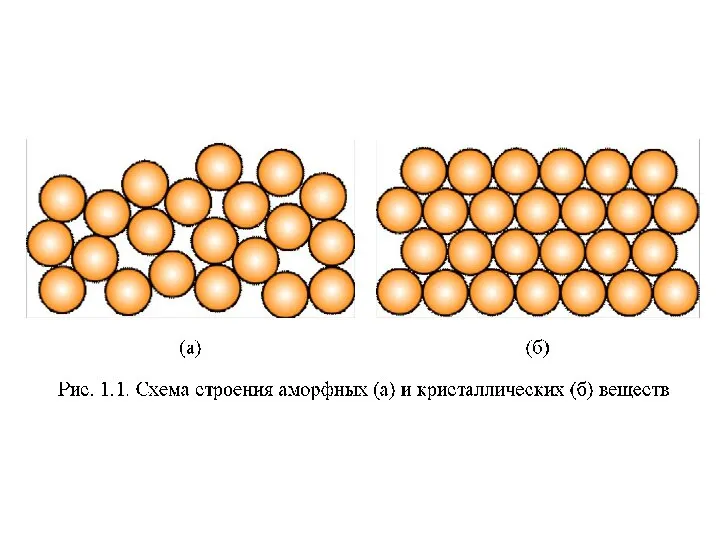 Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов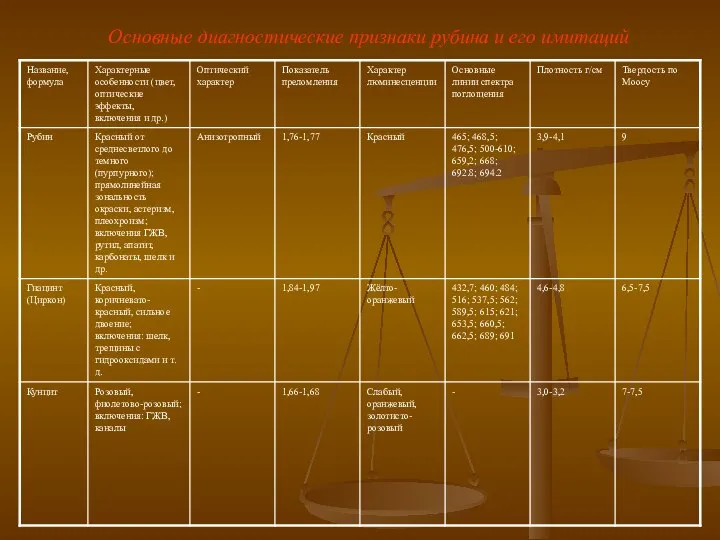 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися