Содержание
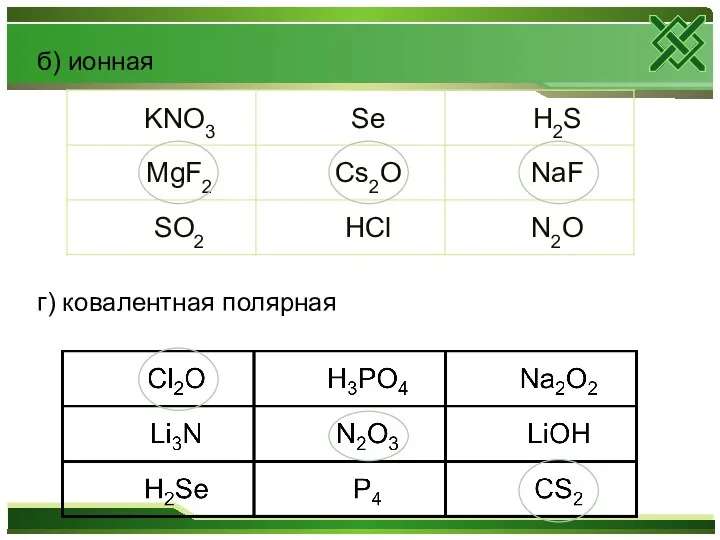
- 2. б) ионная г) ковалентная полярная
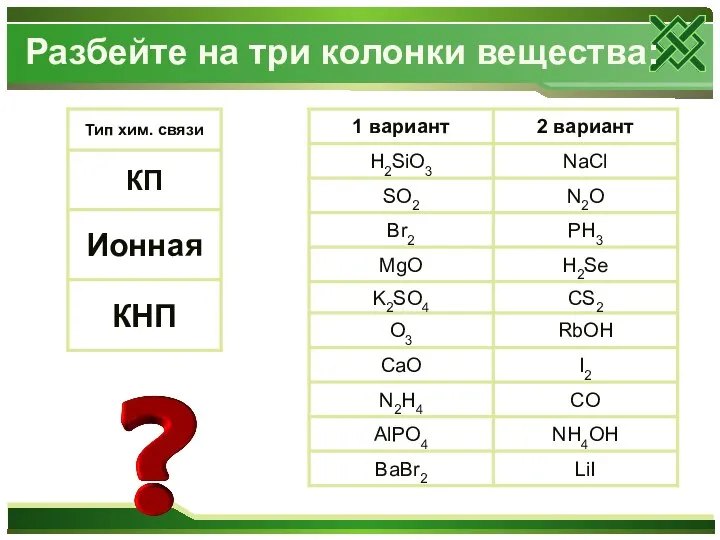
- 3. Разбейте на три колонки вещества:
- 4. Влияние Na на организм человека Хранят простое вещество «натрий» как Кощееву смерть. Как может повлиять натрий
- 5. Влияние Cl2 на организм человека Хлор – отравляющее вещество, применявшееся во время первой мировой войны
- 6. Образование сложного вещества Na0 +11 2е,8е,1е Cl0 +17 2e,8e,7e Какой вид связи может образоваться между этими
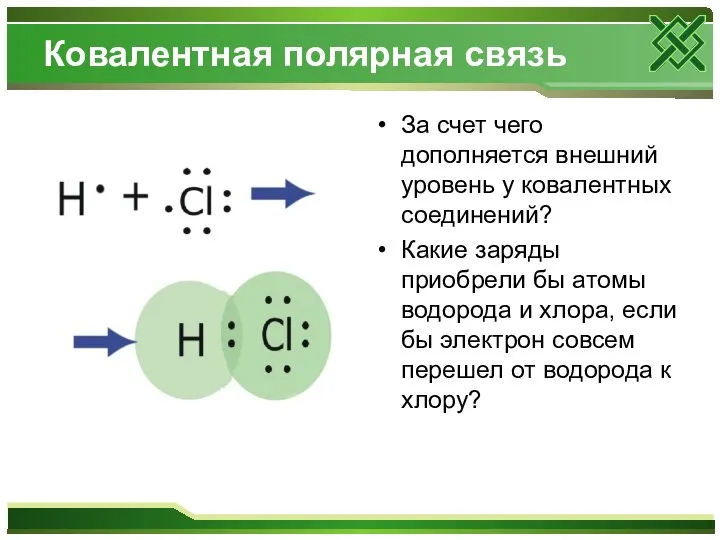
- 7. Ковалентная полярная связь За счет чего дополняется внешний уровень у ковалентных соединений? Какие заряды приобрели бы
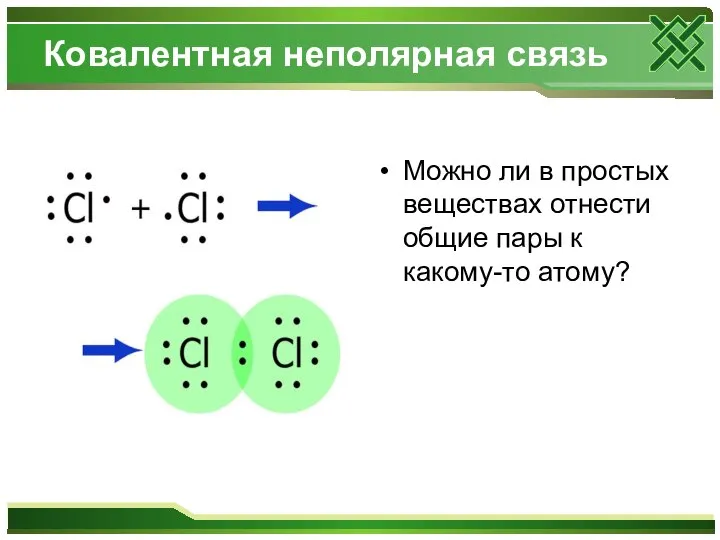
- 8. Ковалентная неполярная связь Можно ли в простых веществах отнести общие пары к какому-то атому?
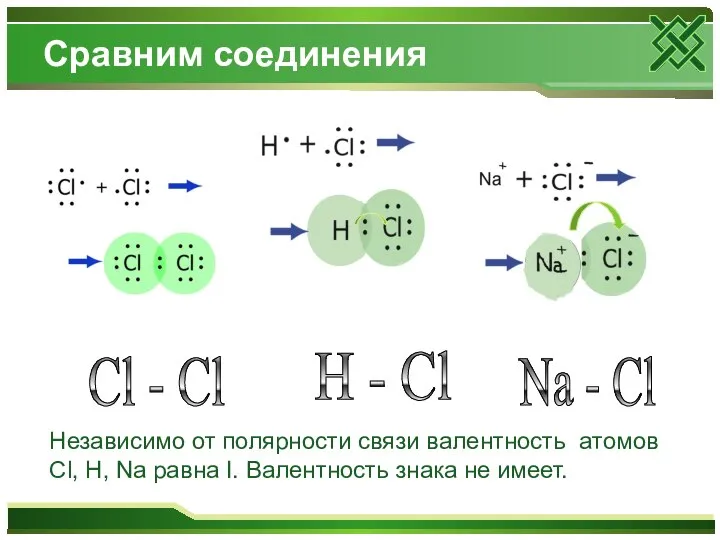
- 9. Сравним соединения H - Cl Cl - Cl Na - Cl Независимо от полярности связи валентность
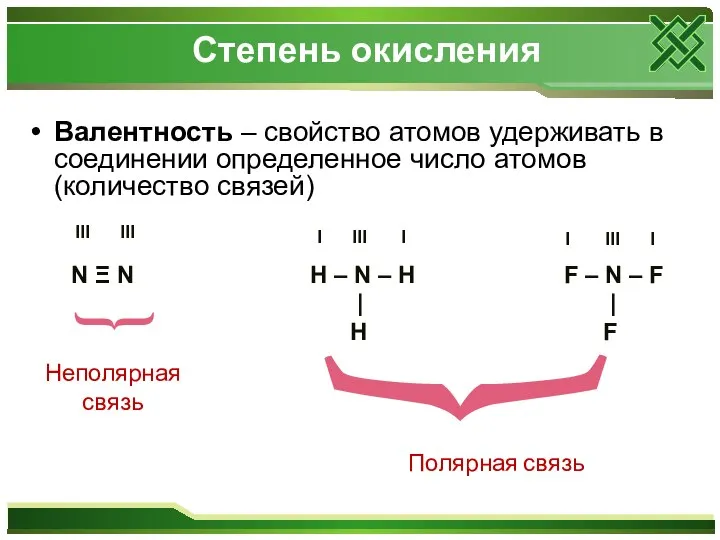
- 10. Степень окисления Валентность – свойство атомов удерживать в соединении определенное число атомов (количество связей) N Ξ
- 11. Степень окисления 8 класс
- 12. Степень окисления – это условный заряд атомов химических элементов в соединении, вычисленный на основе предположения, что
- 13. Правила определения с.о. С.о. атомов в простых веществах = 0 С.о. фтора = -1 С.о. кислорода
- 14. Возможные с.о. Положительная «+» равна числу отданных электронов. Максимальная с.о. равна номеру группы Отрицательная «-» равна
- 15. Промежуточные с.о. Рассмотрим возможные с.о. серы – S Максимальная +6 SO3 Минимальная -2 H2S Сера может
- 16. Определение с.о. N2O3 На первом месте стоит элемент с «+» с.о., на втором с «-» У
- 17. План определения степени окисления элементов в соединениях 1. Степень окисления атомов в простых веществах равна нулю.
- 18. 3. Определите наиболее электроотрицательный элемент и направление смещения общих электронных пар. Расставьте степени окисления элементов. N2O,
- 19. Определяем степени окисления известных элементов. H2SO4 +1 X -2 2. Для определения степени окисления неизвестного элемента
- 20. 1. Определите степень окисления атомов в соединении. Задания CH4, KCl, AlI3, P2O5. -4 +1 +1 -1
- 21. Задание 1 Определите С.О. по формулам Cl2O7, NaH, Na2S, MgO, H3N, N2, Al2S3, Cu2O
- 23. Скачать презентацию














 Подготовка к контрольной работе
Подготовка к контрольной работе Новые грани парфюмерии. Задача 5
Новые грани парфюмерии. Задача 5 Кинетика катодного выделения водорода на дисилициде хрома в щелочном и кислом электролитах
Кинетика катодного выделения водорода на дисилициде хрома в щелочном и кислом электролитах каталитический крекинг
каталитический крекинг Лакокрасочные материалы
Лакокрасочные материалы Химические реакции (игра)
Химические реакции (игра) Химия в быту
Химия в быту Слюда. История открытия
Слюда. История открытия 20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya
20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Свойства атомов. Типы связей
Свойства атомов. Типы связей Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ
Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ Химическое равновесие и способы его смещения. Принцип Ле Шателье. 9 класс
Химическое равновесие и способы его смещения. Принцип Ле Шателье. 9 класс Щелочные металлы и их соединения
Щелочные металлы и их соединения Алканы. Циклоалканы
Алканы. Циклоалканы Закон сохранения массы. 11 класс
Закон сохранения массы. 11 класс Кетоновые тела
Кетоновые тела Коллоидные системы
Коллоидные системы Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Химические элементы
Химические элементы Презентация на тему Химический "Звездный час"
Презентация на тему Химический "Звездный час"  Растворимость веществ. Кристаллогидраты
Растворимость веществ. Кристаллогидраты Водород. Вода
Водород. Вода Общая химия, понятия
Общая химия, понятия Алканы. Этан
Алканы. Этан Амины. Аминокислоты
Амины. Аминокислоты Valentnost
Valentnost