Слайд 2Вставь пропущенные слова.
Вопрос 1
Химический элемент – это ……. …… …….. .
Химический элемент

– это определённый вид атомов.
Слайд 3Вопрос 2
Атом состоит из ……, находящегося в центре атома, и …….., движущихся

около него.
Атом состоит из ядра, находящегося в центре атома, и электронов, движущихся около него.
Слайд 4Вопрос 3
В состав ….. входят протоны и нейтроны. Заряд протона равен ….,

нейтрона - ….. . Их массы одинаковы и равны …… .
В состав ядра входят протоны и нейтроны. Заряд протона равен + 1, нейтрона - 0 . Их массы одинаковы и равны 1.
Слайд 5Вопрос 4
В ядре сосредоточена основная …… атома, ядро заряжено ……. .
В ядре

сосредоточена основная масса атома, ядро заряжено положительно.
Слайд 6Вопрос 5
Заряд электрона равен ……, его масса считается равной …… .
Заряд электрона

равен -1, его масса считается равной 1.
Слайд 7Вопрос 6
Атом в целом имеет заряд, равный …… (электронейтрален), потому что число

протонов и электронов ……. .
Атом в целом имеет заряд, равный нулю (электронейтрален), потому что число протонов и электронов одинаково.
Слайд 8Вопрос 7
Число электронов, как и протонов, в атоме химического элемента равно ……

…… химического элемента.
Число электронов, как и протонов, в атоме химического элемента равно порядковому номеру химического элемента.
Слайд 9Вопрос 8
Число нейтронов находится как ….. атомной массы и ……. ……. ……..

.
Число нейтронов находится как разность атомной массы и порядкового номера элемента.
Слайд 10Вопрос 9
Важнейшей характеристикой атома является ……. ……. ……. .
Важнейшей характеристикой атома является

заряд ядра атома.
Слайд 11Вопрос 10
Атомы одного и того же элемента, отличающиеся количеством ….. (а потому

и массой) называются …… . Несмотря на разную массу, это атомы одного и того же элемента, потому что …… …… у них одинаков.
Слайд 12Вопрос 10
Атомы одного и того же элемента, отличающиеся количеством нейтронов (а потому

и массой) называются изотопами. Несмотря на разную массу, это атомы одного и того же элемента, потому что заряд ядра у них одинаков.
Слайд 13Вопрос 11
Атомная масса элементов дробная величина, потому что существуют ….. , и

в периодической системе приводится среднее арифметическое их масс.
Слайд 14Вопрос 11
Атомная масса элементов дробная величина, потому что существуют изотопы, и в

периодической системе приводится среднее арифметическое их масс.
Слайд 15Вопрос 12
Орбиталь – это …. ….. ….. ….. ….. . Орбитали сферической

формы - … - орбитали, орбитали в форме восмёрки - ..., …., …. – орбитали.
Слайд 16Вопрос 12
Орбиталь – это область пространства вокруг ядра атома. Орбитали сферической формы

- s - орбитали, орбитали в форме восмёрки – p, d, f – орбитали.
Слайд 17Вопрос 13
Важнейшей характеристикой движения электрона является запас его …. . В зависимости

от запаса его …. электрон может находиться на определённом энергетическом уровне.
Слайд 18Вопрос 13
Важнейшей характеристикой движения электрона является запас его энергии. В зависимости от

запаса его энергии электрон может находиться на определённом энергетическом уровне.
Слайд 19Вопрос 14
На первом энергетическом уровне максимально может быть …. электрона.
На первом энергетическом

уровне максимально может быть два электрона.
Слайд 20Вопрос 15
На втором энергетическом уровне максимально может быть …. электронов.
На втором энергетическом

уровне максимально может быть восемь электронов.
Слайд 21Вопрос 16
Общее количество энергетических уровней в атоме равно номеру ……, в котором

находится элемент.
Общее количество энергетических уровней в атоме равно номеру периода, в котором находится элемент.
Слайд 22Вопрос 17
В периоде происходит ….. заполнение орбиталей электронами. Каждый новый период начинается

с заполнения электронами ….. энергетического уровня.
Слайд 23Вопрос 17
В периоде происходит постепенное заполнение орбиталей электронами. Каждый новый период начинается

с заполнения электронами нового энергетического уровня
Слайд 24Вопрос 18
Число электронов на высшем (внешнем, самом дальнем от ядра) уровне равно

….. ….. . Внешний электронный слой атомов элементов одной группы (главной подгруппы) ….. .
Слайд 25Вопрос 18
Число электронов на высшем (внешнем, самом дальнем от ядра) уровне равно

номеру группы. Внешний электронный слой атомов элементов одной группы (главной подгруппы) одинаков.
Слайд 26Вопрос 19
Запись электронного строения с указанием энергетических уровней, вида орбиталей и количества

электронов на орбиталях - ……. …… .
Слайд 27Вопрос 19
Запись электронного строения с указанием энергетических уровней, вида орбиталей и количества

электронов на орбиталях – электронная формула.
Слайд 28Вопрос 20
Периодический закон был сформулирован … …. …. в …. году.
Периодический закон

был сформулирован Дмитрием Ивановичем Менделеевым в 1869 году.
Слайд 29Вопрос 21
Формулировки периодического закона: свойства элементов и их соединений находятся в периодической

зависимости от …. …. (Д.И. Менделеев), от …. ….. (современная).
Слайд 30Вопрос 21
Формулировки периодического закона: свойства элементов и их соединений находятся в периодической

зависимости от массы атома (Д.И. Менделеев), от заряда ядра (современная).
Слайд 31Вопрос 22
Д.И. Менделеев рассматривал зависимость свойств от ….. …. , поскольку ….

…. …. …. .
Д.И. Менделеев рассматривал зависимость свойств от массы атома, поскольку не было известно о строении атома.
Слайд 32Вопрос 23
Свойства элементов и их соединений изменяются периодически, потому что периодически повторяется

строение ….. .
Слайд 33Вопрос 23
Свойства элементов и их соединений изменяются периодически, потому что периодически повторяется

строение атома.
Слайд 34Вопрос 24
Периодическая система содержит 7 ….. и 8 …….. .
Периодическая система содержит

7 периодов и 8 групп.
Слайд 35Вопрос 25
Период - …… ……. В периоде радиус атомов элементов слева направо

…… . Число электронов внешнего энергетического уровня ….. . Металлические свойства элементов ….. , а неметаллические ….. .
Слайд 36Вопрос 25
Период – горизонтальный ряд. В периоде радиус атомов элементов слева направо

уменьшается. Число электронов внешнего энергетического уровня увеличивается. Металлические свойства элементов ослабевают, а неметаллические усиливаются.
Слайд 37Вопрос 26
Группа - ….. ….. . Группы содержат две ….. (главную и

побочную). В группе (сверху вниз)радиус атомов элементов ….. , число электронов внешнего энергетического уровня ….. . Неметаллические свойства элементов ….., а металлические - …… .
Слайд 38Вопрос 26
Группа – вертикальный ряд. Группы содержат две подгруппы (главную и побочную).

В группе (сверху вниз) радиус атомов элементов увеличивается, число электронов внешнего энергетического уровня одинаково. Неметаллические свойства элементов ослабевают, а металлические - усиливаются.





































 Презентация на тему Соединения серы
Презентация на тему Соединения серы  Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Незаменимая уксусная кислота
Незаменимая уксусная кислота Перегонка. Вклад алхимиков в органическую химию
Перегонка. Вклад алхимиков в органическую химию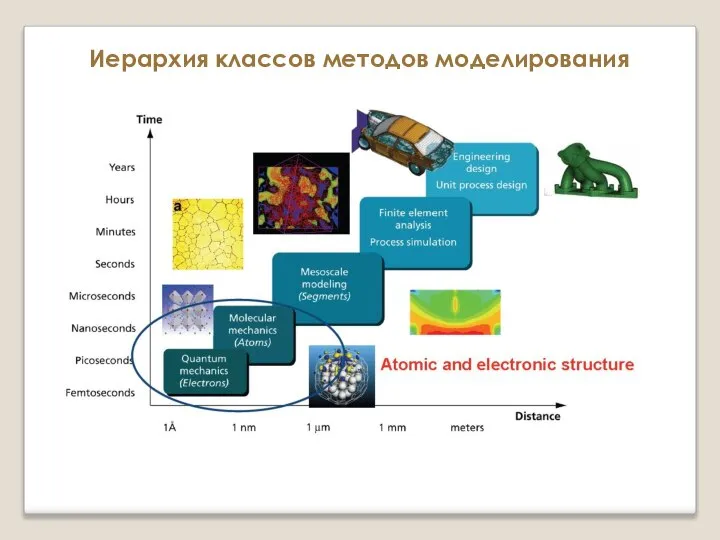 Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Магний и кальций
Магний и кальций Сахароза, крахмал, целлюлоза
Сахароза, крахмал, целлюлоза Строение сложного фермента
Строение сложного фермента Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент
Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Углеводороды. Общие знания
Углеводороды. Общие знания Gelation in aqueous solution of L-cysteine and silver nitrate
Gelation in aqueous solution of L-cysteine and silver nitrate Заполни электронные уровни элементов
Заполни электронные уровни элементов Явление аллотропии
Явление аллотропии Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала
Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала Центробежное осаждение
Центробежное осаждение Характеристика кислорода и серы
Характеристика кислорода и серы Актуальные задачи химии
Актуальные задачи химии Металлы - наши друзья или враги
Металлы - наши друзья или враги Получение, свойства и применение алкенов
Получение, свойства и применение алкенов Классификация силикатов
Классификация силикатов Способы получения металлов
Способы получения металлов Фуллерены
Фуллерены 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Природные источники углеводородов
Природные источники углеводородов علاوي الندوة
علاوي الندوة Цезій
Цезій