Содержание
- 2. Литература 1. Попков В.А., Пузаков С.А. Общая химия: Учебник. - М.: ГЭОТАР-Медиа, 2007. -976 с. 2.Пузаков
- 3. 5.Биоорганическая химия. Учебник. (Тюкавкина Н.А., Бауков Ю.И.). 7 изд., Дрофа. 2008 – 543 с. 6.Руководство к
- 4. Интернет-источники http://www.chem.msu.su http://www.xumuk.ru/ http://www.alhimik.ru/ http://www.chemlib.ru http://alhimikov.net/ http://chemistry.narod.ru/ http://www.chemport.ru/
- 5. Значение химии в медицине 1.78 химических элементов входят в состав живых организмов. 2.44 элемента входят в
- 6. Задача, стоящая перед медиками в ближайшее время, предупреждать, а не лечить болезни. Чтобы стать высококвалифицированным специалистом
- 7. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
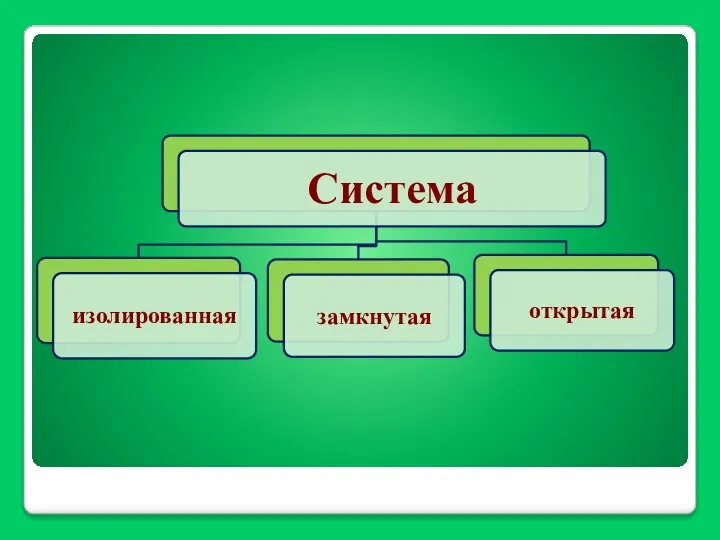
- 8. Термодинамика – наука, изучающая общие законы взаимного превращения одной формы энергии в другую. Система – это
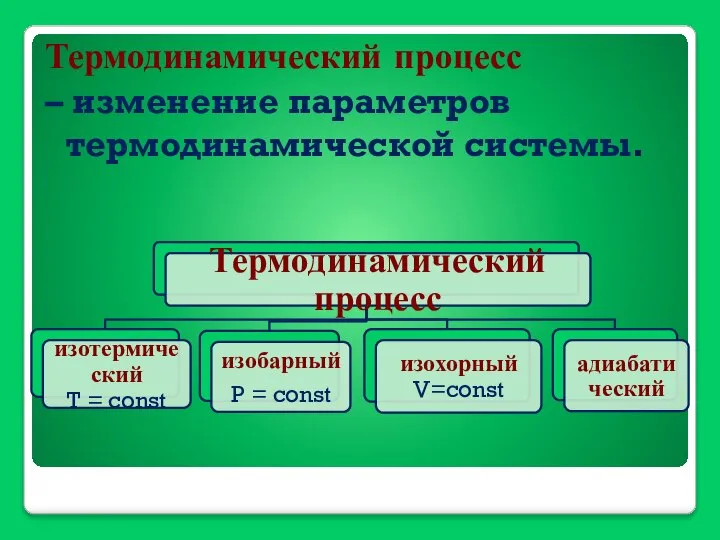
- 11. Термодинамический процесс – изменение параметров термодинамической системы.
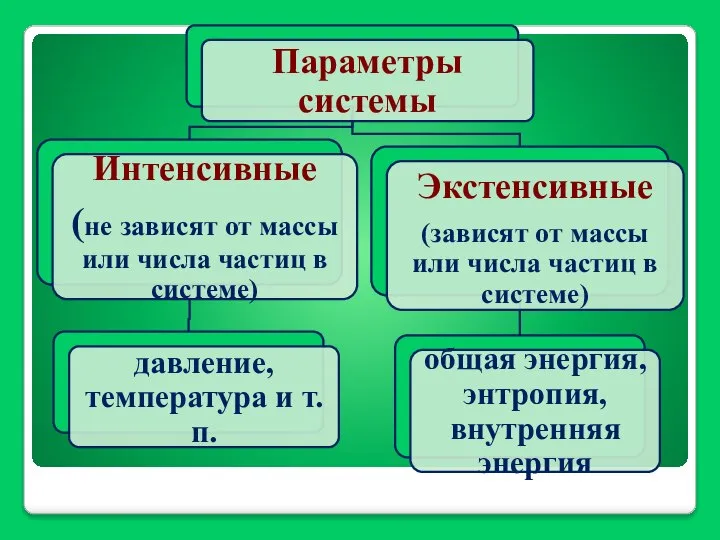
- 12. Энергия системы (W) - совокупность двух частей: зависящей от движения и положения системы как целого (Wц)
- 13. Внутренняя энергия разделяется на свободную энергию и связанную энергию: U = G + Wсв Свободная энергия
- 14. При сообщении термодинамической системе некоторого количества теплоты Q в общем случае происходит изменение внутренней энергии системы
- 15. Энергия расширенной системы, или внутреннее теплосодержание системы называется энтальпией (Н). Для экзотермических реакций Q>0, ΔH Для
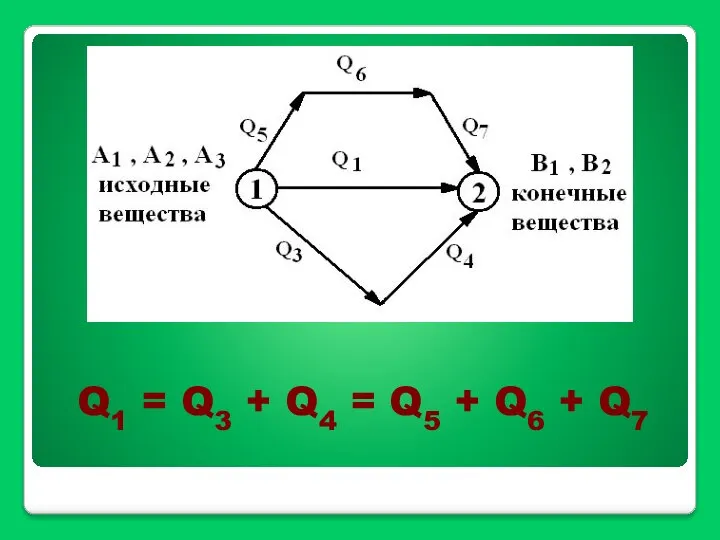
- 16. Q1 = Q3 + Q4 = Q5 + Q6 + Q7
- 17. I следствие закона Гесса где νн, νк - стехиометрические коэффициенты для реакции аА + bB→dD ∆Hреакц.
- 18. Величина и знак теплоты образования характеризуют устойчивость соединения в данных условиях Вещество NH3 PH3 AsH3 SbH3
- 19. Энтропия (S) - функция состояния термодинамической системы, используемая во втором законе т/д для выражения через нее
- 20. ΔG – изобарно-изотермический потенциал (свободная энергия Гиббса) ΔG = ΔH – T · ΔS где ΔH
- 21. Особенности живых организмов с позиции термодинамики 1.Живой организм – открытая система, непрерывно обменивающаяся с окружающей средой
- 22. 3. Все биохимические процессы, происходящие в клетках живых организмов, протекают при постоянной температуре, давлении, при незначительных
- 23. Главными компонентами пищи являются углеводы, жиры и белки. Калорийность, то есть энергия, выделяемая в процессе диссимиляции
- 25. Скачать презентацию


















 Нобелевские лауреаты и их достижения
Нобелевские лауреаты и их достижения Алканы. Строение,номенклатура, изомерия
Алканы. Строение,номенклатура, изомерия Органическая химия
Органическая химия Презентация на тему Увлекательные факты из жизни Менделеева
Презентация на тему Увлекательные факты из жизни Менделеева  Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли
Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли  Растворы электролитов
Растворы электролитов Пятичленные гетероциклы с двумя и более атомами азота
Пятичленные гетероциклы с двумя и более атомами азота Гидролиз солей
Гидролиз солей Скорость химических реакций
Скорость химических реакций Веселый химический КВН
Веселый химический КВН Понятие об ароматических спиртах и фенолах. Особенности строения фенола
Понятие об ароматических спиртах и фенолах. Особенности строения фенола Химическая коррозия
Химическая коррозия Строение атома
Строение атома Проблемы и меры по защите окружающей среды ПМР
Проблемы и меры по защите окружающей среды ПМР Алкены. Гомологический ряд алкенов. Изомерия алкенов
Алкены. Гомологический ряд алкенов. Изомерия алкенов Современные способы защиты ОТТ
Современные способы защиты ОТТ Закон сохранения массы веществ. 8 класс
Закон сохранения массы веществ. 8 класс Криогенный разрыв пласта
Криогенный разрыв пласта Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Применение неметаллов
Применение неметаллов Растворение
Растворение алотропні модифікації неметалів
алотропні модифікації неметалів Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Разбор заданий на амины
Разбор заданий на амины Интеллектуальный турнир для старшеклассников Умножая таланты 2020
Интеллектуальный турнир для старшеклассников Умножая таланты 2020 Презентация на тему Теория электролитической диссоциации обобщающий урок
Презентация на тему Теория электролитической диссоциации обобщающий урок  Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Сода: мифы и реальность
Сода: мифы и реальность