Содержание
- 2. Выберите тему основные сведения о строении атома Изменения в составе ядер атомов химических элементов. Изотопы. Строение
- 3. Основные сведения о строении атома
- 4. Изменения в составе ядер атомов химических элементов . Изотопы
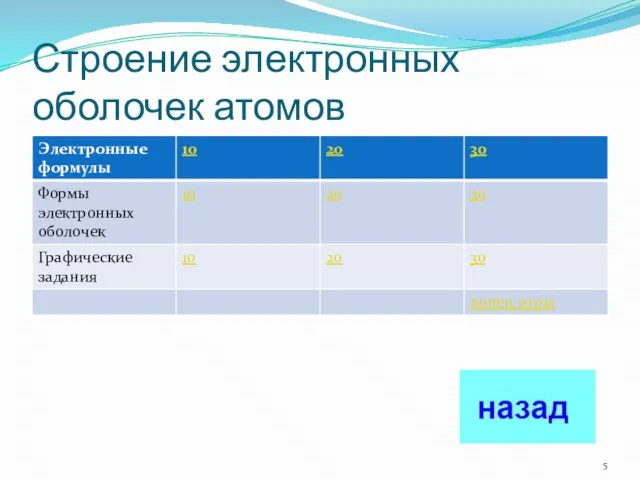
- 5. Строение электронных оболочек атомов
- 6. Правильный ответ назад
- 7. Неверно. Подумайте ещё. назад
- 8. Частицы 10 Протон обозначается Р n e
- 9. Частицы 20 Заряд электрона +1 0 -1 Неизвестен назад
- 10. Частицы 30 Каковы заряд и масса частицы , число которых определяется по формуле N=A-Z Масса 1
- 11. Ученые и открытия10 Фамилия ученого , который проводил опыт по схеме: Дж. Томсон Д.И.Менделеев Э.Резерфорд Ж.
- 12. Ученые и открытия 20 Кто предложил модель атома «кекс» Э. Резерфорд Дж. Томсон и Ж Перрен
- 13. Ученые и открытия 30 Кто открыл радиоактивность? Э. Резерфорд Дж. Томсон А. Беккерель Д.И.Менделеев
- 14. Состав атома 10 Какая частица не входит в состав атома Протон Электрон Альфа-частица нейтрон
- 15. Состав атома 20 Какой заряд имеет частица ,не входящая в состав ядра атома? 0 +1 -1
- 16. Состав атома 30 Массовое число показывает Число протонов Число нейтронов Число электронов Число частиц в ядре
- 17. Графические задания 10 Как называется данная модель атома? Планетная Планетарная Модель Резерфорда Модель Томсона
- 18. Графические задания 20 На рисунке изображен атом Ве В С N
- 19. Графические задания 30 Н а рисунке изображен Атом кислорода Атом фтора Положительный ион кислорода 4. Отрицательный
- 20. Электронные формулы10 Электронная схема кислорода 2е,4е 2е,6е 2е,8е 2е,8е,1е
- 21. Электронные формулы 20 Электронная формула фтора 1s22s12p5 1s22s22p4 1s22s22p5 1s22s22p6
- 22. Электронные формулы 30 Характеристикам какого химического элемента соответствует данная электронная формула 1s22s22p63s23p1 Массовое число 23;зарядовое число11
- 23. Правильный ответ
- 24. Неверно. Подумайте ещё.
- 25. Формы электронных оболочек 10 Правильный порядок заполнения электронами уровней и подуровней 1p,2s,2p,3s,3p 1s,2p,2s,3s,3p 1s,2s,2p,3p,3s 1s,2s,2p,3s,3p
- 26. Формы электронных оболочек 20 Пространство вокруг ядра атома, где наиболее вероятно нахождение данного электрона, называют Слой
- 27. Формы электронных оболочек 30 В состав какого химического элемента входит большее число электронов , находящихся на
- 28. Графическое задание 10 На рисунке изображена S- орбиталь p-орбиталь d- орбиталь f -орбиталь
- 29. Графическое задание 20 у натрия стрелкой указана орбиталь 4s 3s 4p 3p
- 30. Графические задания 30 Сколько электронов должно быть на этой оболочке у аргона? 2 8 6 0
- 31. ГИА 10 Найдите неверное определение химического элемента -это определенный вид атомов -это совокупность атомов с одинаковым
- 32. Ядерные процессы 10 Если уменьшить на один число протонов в ядре то, получится Положительный ион Химический
- 33. Ядерные процессы 20 Какая частица образуется в ходе ядерной реакции 3 7Li +2 4He 5 10B
- 34. Ядерные процессы30 Если атом азота обстрелять протоном 7 14 N+11H ? ,то образуется атом Углерода Кислорода
- 35. Правильный ответ
- 36. Неверно.Подумайте
- 37. Изотопы 10 Чему равно число нейтронов в атоме алюминия 13 26 27 14
- 38. Изотопы 20 В каком атоме число электронов, протонов, нейтронов одинаково и равно 12 Na Ne Mg
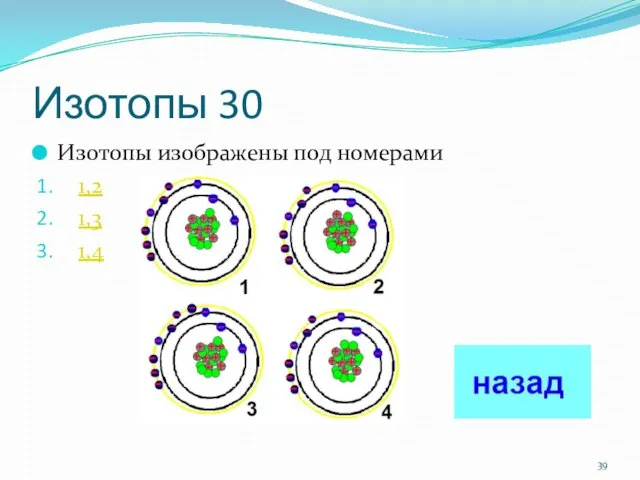
- 39. Изотопы 30 Изотопы изображены под номерами 1,2 1,3 1,4
- 40. ГИА-20 Атомы химических элементов азота и фосфора имеют одинаковое число Заполненных электронных слоев Протонов Электронов во
- 41. ГИА-30 Какой частице не соответствует следующее расположение электронов 2,8,8 Атом аргона Отрицательный ион хлора Положительный ион
- 43. Скачать презентацию






































 Углеводороды. Предельные (насыщенные) углеводороды
Углеводороды. Предельные (насыщенные) углеводороды Характеристика химического элемента по его положению в ПСХЭ Д.И.Менделева
Характеристика химического элемента по его положению в ПСХЭ Д.И.Менделева Металл XXI века титан
Металл XXI века титан Электролитическая диссоциация
Электролитическая диссоциация Технология переработки редкоземельного сырья
Технология переработки редкоземельного сырья Пробоотбор и пробоподготовка
Пробоотбор и пробоподготовка Использование комбинаторных задач для подсчета вероятностей
Использование комбинаторных задач для подсчета вероятностей Аммиак. Азот
Аммиак. Азот валентность (1)
валентность (1) Стекло. Определение стекла
Стекло. Определение стекла Изменения, происходящие с веществами. Физические явления в химии
Изменения, происходящие с веществами. Физические явления в химии Минералы алюминия
Минералы алюминия Определение формул органических веществ. Задачи для самостоятельного решения
Определение формул органических веществ. Задачи для самостоятельного решения Растительные источники жиров и жирных масел
Растительные источники жиров и жирных масел Степень окисления
Степень окисления Наука химия. Интеллектуальная игра. 5-8 класс
Наука химия. Интеллектуальная игра. 5-8 класс Вещество. Кристаллические решетки
Вещество. Кристаллические решетки Вода - это жизнь
Вода - это жизнь Классификация органических соединений. 10 класс
Классификация органических соединений. 10 класс Сложные реакции
Сложные реакции Материаловедение
Материаловедение Магматические породы
Магматические породы Алкины (ацетиленовые углеводороды)
Алкины (ацетиленовые углеводороды) Вода
Вода Самородные элементы. Сера. Лекция 7
Самородные элементы. Сера. Лекция 7 Применение муравьиного спирта
Применение муравьиного спирта Получение формальдегида методом дегидрирования метанола
Получение формальдегида методом дегидрирования метанола Презентация на тему Окислительно-восстановительные реакции
Презентация на тему Окислительно-восстановительные реакции