Слайд 2Алгоритм решения задач
-Составить уравнение реакции;
-Перевести данные задачи (массу или объем) в количество

вещества (моль);
-Над формулами веществ в уравнении записать известное и неизвестное количество вещества;
-Под формулами соответствующих веществ записать количество вещества, найденное по уравнению, согласно коэффициентам;
-Составить и решить пропорцию;
- Перевести полученное количество вещества в массу или объем
Слайд 3Задача1
Определите количество вещества соли CuSO4, полученной при взаимодействии гидроксида меди(II) с 58,8

г серной кислоты
Слайд 4Задача1:Определите количество вещества соли CuSO4, полученной при взаимодействии гидроксида меди(II) с 58,8

г серной кислоты
Дано:
m(H2SO4) = 58,8г
Найти n (соли CuSO4)-?
Решение:
1.Составляем уравнение:
0,6 моль х моль по условию
Cu(OH)2+H2SO4=CuSO4+2HOH
1 моль 1 моль по уравнению
2.Найдем n(H2SO4)
m=M·n M=Mr
Mr (H2SO4) = 2+32+64=98
n= m/M= 58,8:98=0,6 моль
3. составляем пропорцию
0,6/1 = x/1
X=0,6 моль
Ответ: n (СuSO4) =0,6 моль






 Внеклассное мероприятие по химии для учащихся 8 классов
Внеклассное мероприятие по химии для учащихся 8 классов Вязкоупругие свойства полимеров
Вязкоупругие свойства полимеров Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений
Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений Строение электронных оболочек
Строение электронных оболочек Ионо-дисперсное состояние микрокомпонентов в растворах
Ионо-дисперсное состояние микрокомпонентов в растворах Химические реакции в органике
Химические реакции в органике Календарь юного химика. 2013-2014 учебный год
Календарь юного химика. 2013-2014 учебный год Графит. 9 класс
Графит. 9 класс Вода – уникальное вещество на планете Земля
Вода – уникальное вещество на планете Земля Спирты. Строение, классификация, изомерия, физические свойства
Спирты. Строение, классификация, изомерия, физические свойства Оксиды, их классификация и химические свойства. 8 класс
Оксиды, их классификация и химические свойства. 8 класс Современная теория строения атома. Периодический закон и периодическая система элементов Д.И. Менделеева
Современная теория строения атома. Периодический закон и периодическая система элементов Д.И. Менделеева Общая характеристика неметаллов подгруппы кислород
Общая характеристика неметаллов подгруппы кислород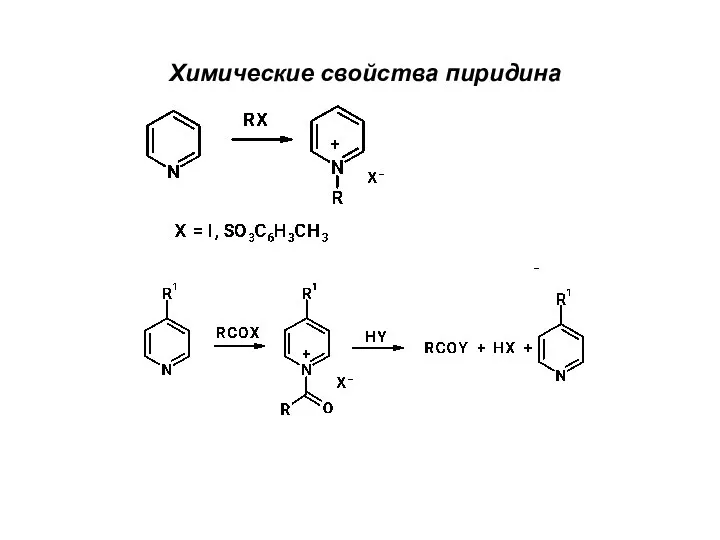 Химические свойства пиридина
Химические свойства пиридина Строение вещества
Строение вещества Техника безопасности на уроках химии
Техника безопасности на уроках химии Путешествие в мир удивительных веществ Оксиды. Химия 8 класс
Путешествие в мир удивительных веществ Оксиды. Химия 8 класс Обобщение знаний об углеводородах
Обобщение знаний об углеводородах Personal сare. Akypo Foam Rl 40
Personal сare. Akypo Foam Rl 40 Закон сохранения массы и энергии
Закон сохранения массы и энергии Чистые вещества и смеси
Чистые вещества и смеси Альдегиды
Альдегиды Изомерия
Изомерия Метод проектов: организация деятельности по химии
Метод проектов: организация деятельности по химии Строение атома. Химия, 8 класс
Строение атома. Химия, 8 класс Химия вокруг нас
Химия вокруг нас Prezentatsia_k_uroku
Prezentatsia_k_uroku Химия и космос
Химия и космос