Содержание
- 2. УГЛЕРОД
- 3. Цели урока: Изучить строение атома углерода Изучить свойства углерода Изучить применение углерода
- 4. 1789 г. Антуан Лоран Лавуазье Углерод – «рождающий уголь»
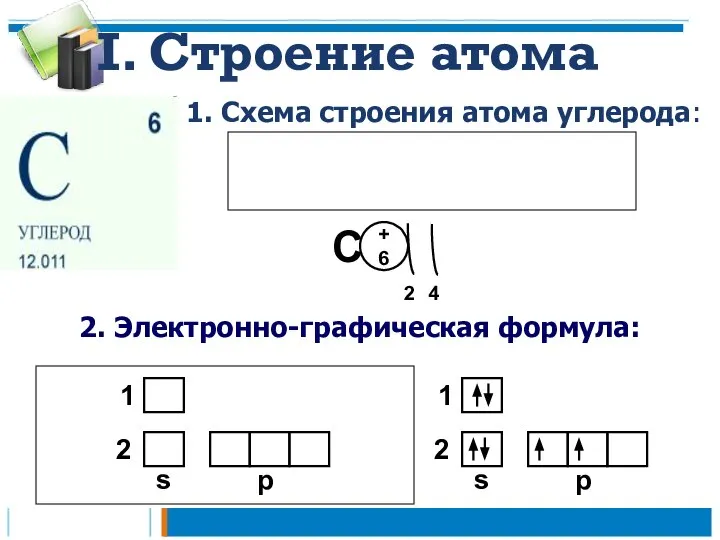
- 5. I. Строение атома C 2. Электронно-графическая формула: 2 1 s p 1. Схема строения атома углерода:
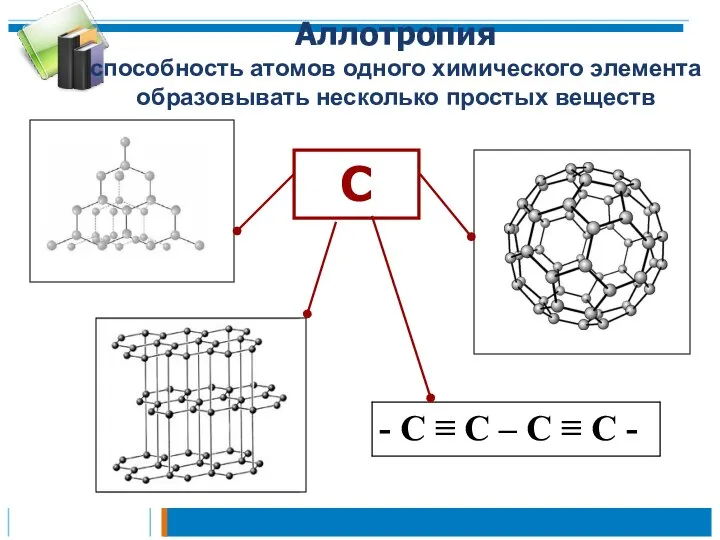
- 6. Аллотропия способность атомов одного химического элемента образовывать несколько простых веществ С - С ≡ С –
- 8. Аллотропия Алмаз Бриллианты – искусственно ограненные алмазы
- 9. Звезда ордена Св. Андрея Первозванного Изделия с бриллиантами Большая императорская корона
- 10. Императорский скипетр Изделия с бриллиантами Малая императорская корона
- 11. Аллотропия Графит Темно-серое кристаллическое вещество, с металлическим блеском, жирное на ощупь, мягкое, обладает электропроводностью, тугоплавкое.
- 12. Применение графита Грифель карандашей, различные смазки, в реактивных двигателях, в ядерных реакторах, для изготовления электродов в
- 13. Карбин — линейный полимер углерода Карбин - мелкокристаллический порошок чёрного цвета полупроводник Применение — в фотоэлементах,
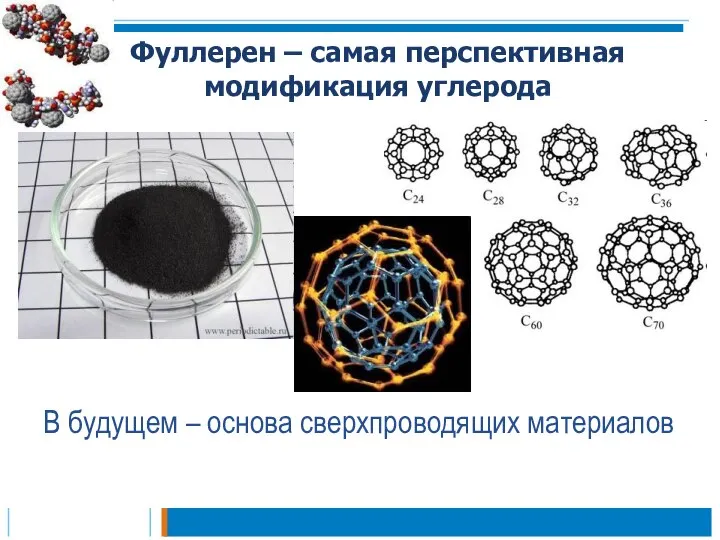
- 14. Фуллерен – самая перспективная модификация углерода В будущем – основа сверхпроводящих материалов
- 15. «Аморфный углерод» - мелкокристаллический графит Сажа Древесный уголь Кокс
- 16. Адсорбция – способность поглощать (адсорбировать) различные вещества (газы, растворенные в воде краски и т.д.)
- 17. Свойство адсорбции применяют: в фильтрах противогазов для очистки сахара, спирта; в медицине; Первый отечественный противогаз конструкции
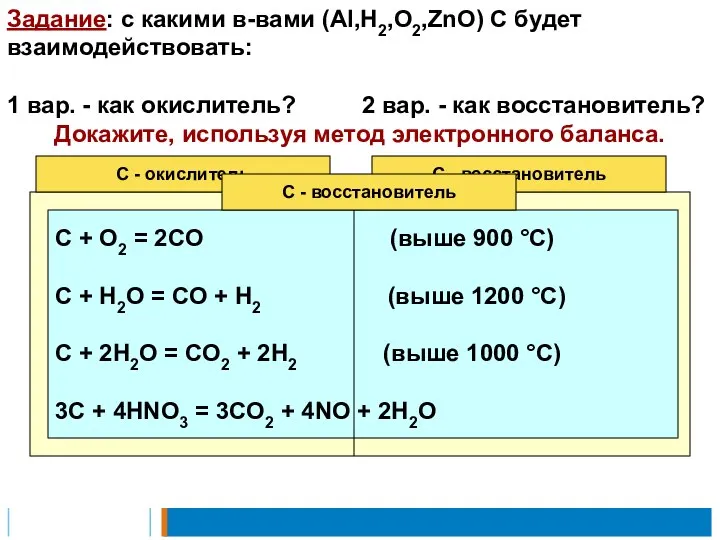
- 18. Задание: с какими в-вами (Al,H2,O2,ZnO) С будет взаимодействовать: 1 вар. - как окислитель? 2 вар. -
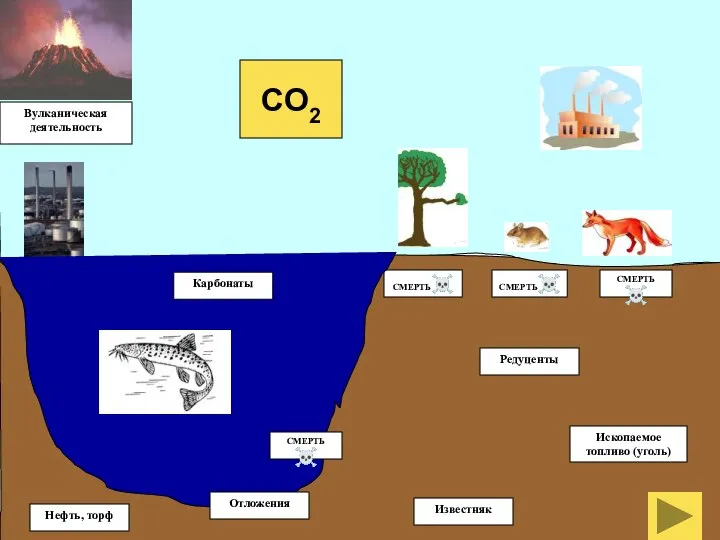
- 19. Домашнее задание Составить схему «Круговорот углерода в природе», используя текст § 27
- 20. Редуценты СМЕРТЬ☠ СМЕРТЬ☠ СМЕРТЬ☠ Известняк Нефть, торф Ископаемое топливо (уголь) Вулканическая деятельность CO2 СМЕРТЬ☠ Карбонаты Отложения
- 21. Проверь себя! А. Атомный радиус Б. Число неспаренных электронов в атоме В. Число s-электронов в атоме
- 22. Проверь себя! А. Углерода Б. Фосфора В. Серы Г. Хлора Задание №2: неметаллические свойства наименее выражены
- 23. Проверь себя! А. Алмаз и графит Б. Аммиак и йод В. Озон и кислород Г. Вода
- 24. Проверь себя! А. Алмаз – самое твердое из природных веществ Б. Алмаз имеет молекулярную кристаллическую решетку
- 25. Проверь себя! А. -4 Б. 0 В. +2 Г. +4 Задание №5: при нагревании углерод реагирует
- 26. Правильные ответы: 1 – Г; 2 – А; 3 – А; 4 – Б; 5 –
- 27. Мне показалось важным… Я был бы рад(а) если… Сегодня я задумался(лась)… Самым интересным было…
- 29. Скачать презентацию




















 Растворы. Виды выражения концентрации
Растворы. Виды выражения концентрации Химическая связь
Химическая связь Амины и анилин
Амины и анилин Мышьяк. История. Нахождение в природе
Мышьяк. История. Нахождение в природе Химическая промышленность России входит в авангардную тройку
Химическая промышленность России входит в авангардную тройку Коллоидные системы
Коллоидные системы Химическая связь
Химическая связь Сплавы со специальными свойствами
Сплавы со специальными свойствами Внутренняя среда организма. Система крови. Физико-химические свойства крови
Внутренняя среда организма. Система крови. Физико-химические свойства крови 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Скорость химической реакции. 9 класс
Скорость химической реакции. 9 класс Химия углеводов
Химия углеводов Хлор
Хлор Уравнение состояния идеального газа
Уравнение состояния идеального газа Моделирование фазовых систем. Тройные взаимные системы
Моделирование фазовых систем. Тройные взаимные системы Адиабатическое приближение, потенциальные поверхности молекулярных систем, неадиабатические переходы
Адиабатическое приближение, потенциальные поверхности молекулярных систем, неадиабатические переходы Расчеты по химическим уравнениям реакций
Расчеты по химическим уравнениям реакций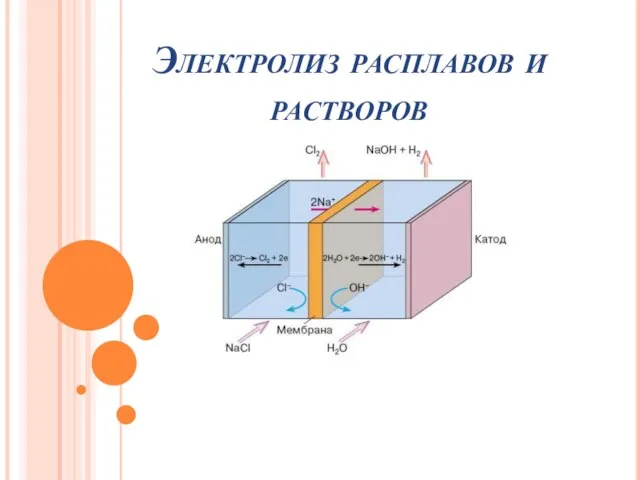 Электролиз расплавов растворов
Электролиз расплавов растворов Первые попытки классификации химических элементов
Первые попытки классификации химических элементов Презентация на тему Важнейшие соединения серы
Презентация на тему Важнейшие соединения серы  Неметаллы. 8 класс
Неметаллы. 8 класс Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота
Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота Строение углеводородов
Строение углеводородов Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс
Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс Периодическая система химических элементов Д. И. Менделеева
Периодическая система химических элементов Д. И. Менделеева Кислоты и их свойства
Кислоты и их свойства Вещество. Кристаллические решетки
Вещество. Кристаллические решетки Презентация на тему В мире индикаторов - исследовательская работа
Презентация на тему В мире индикаторов - исследовательская работа