Содержание
- 2. Гидролиз солей химическое взаимодействие катионов или анионов соли с молекулами воды. В результате образуется слабый электролит.
- 3. Классификация солей Соли, образованные … слабым основанием и слабой кислотой сильным основанием и слабой кислотой слабым
- 4. Сильные кислоты: Сильные основания: HCl - соляная кислота HBr - бромоводород HI - йодоводород HNO3 -
- 5. 1) Гидролиз солей, образованных слабым основанием и слабой кислотой Al2S3 + 6H2O =>2Al(OH)3↓+ 3H2S↑ (в результате
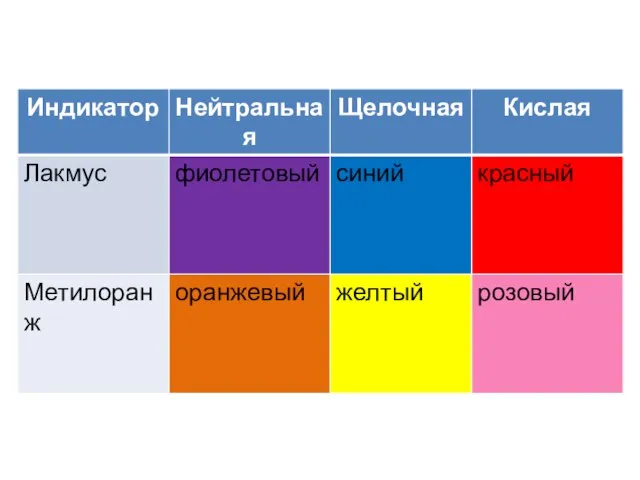
- 6. 2) Гидролиз солей, образованных сильным основанием и слабой кислотой гидролизируется по аниону реакция среды – щелочная
- 7. 3) Гидролиз солей, образованных слабым основанием и сильной кислотой гидролизуется по катиону реакция среды – кислая
- 8. 4) Гидролиз солей, образованных сильным основанием и сильной кислотой не гидролизируется реакция среды – нейтральная
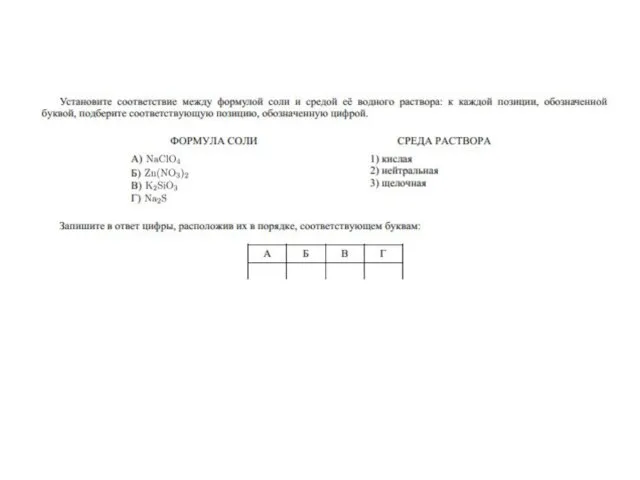
- 10. Задания из ЕГЭ на тему гидролиза солей
- 16. Скачать презентацию











 Электролиз (катод)
Электролиз (катод) Минералы алюминия
Минералы алюминия Электролиз. Применение электролиза
Электролиз. Применение электролиза Химический состав живых организмов. Метаболизм
Химический состав живых организмов. Метаболизм Сера
Сера Алюминий. Из истории открытия
Алюминий. Из истории открытия Химическое сопротивление материалов
Химическое сопротивление материалов Селективная экстракция отдельных групп БАВ сверхкритическими флюидами
Селективная экстракция отдельных групп БАВ сверхкритическими флюидами Использование комбинаторных задач для подсчета вероятностей
Использование комбинаторных задач для подсчета вероятностей Химический опыт с горением борноэтилового эфира
Химический опыт с горением борноэтилового эфира Насыщенные жирные кислоты
Насыщенные жирные кислоты Презентация на тему Пластмасса
Презентация на тему Пластмасса  Химия в косметологии
Химия в косметологии Получение карбоновых кислот
Получение карбоновых кислот Азот. Аммиак. Соли аммония (1)
Азот. Аммиак. Соли аммония (1) Химия цвета
Химия цвета Валентность. Что же это такое?
Валентность. Что же это такое? ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Пример выполнения проверочной работы по теме углеводороды
Пример выполнения проверочной работы по теме углеводороды Установка ЛЧ-35-11/600. Блок Гидроочистки
Установка ЛЧ-35-11/600. Блок Гидроочистки Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Презентация на тему Химия в повседневной жизни человека
Презентация на тему Химия в повседневной жизни человека  Тотығу - тотықсыздану реакциясы
Тотығу - тотықсыздану реакциясы Углеводы: моно-, ди-, полисахариды
Углеводы: моно-, ди-, полисахариды Презентация на тему Природные источники углеводородов (9 класс)
Презентация на тему Природные источники углеводородов (9 класс)  Презентация на тему Угольная и кремниевая кислоты и их соли
Презентация на тему Угольная и кремниевая кислоты и их соли  Презентация на тему М.В. Ломоносов
Презентация на тему М.В. Ломоносов  Кристаллическая структура вещества. Характеристика вещества по формуле
Кристаллическая структура вещества. Характеристика вещества по формуле