Слайд 2Углеводы представляют собой натуральные органические вещества. В их формуле присутствуют углерод и

вода. Благодаря этим элементам организм черпает энергию, которая требуется для поддержания нормальной работы. В зависимости от химической структуры углеводы бывают простыми и сложными.
Слайд 3КЛАССИФИКАЦИЯ УГЛЕВОДОВ
По числу структурных звеньев.
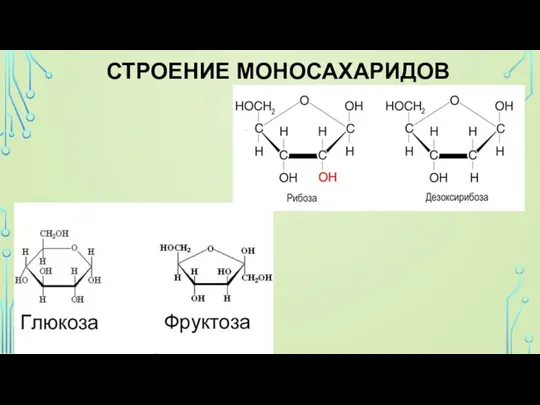
Моносахариды — содержат одно структурное звено.
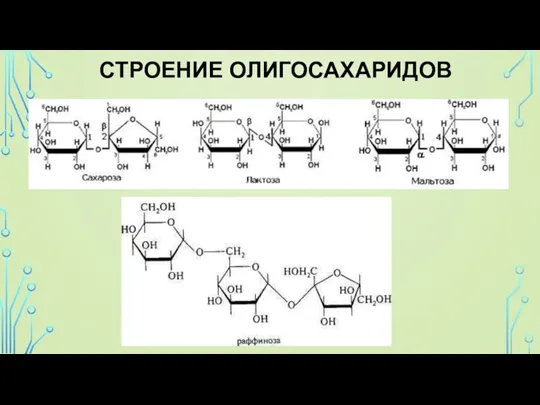
Олигосахариды — содержат

от 2 до 10 структурных звеньев (дисахариды, трисахариды и др.).
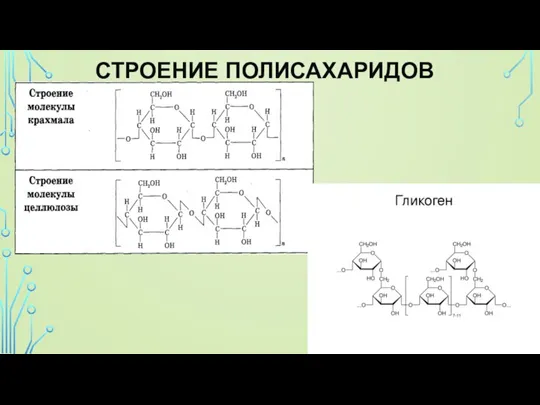
Полисахариды — содержат n структурных звеньев
Некоторые важнейшие углеводы:
Слайд 7ХИМИЧЕСКИЕ СВОЙСТВА ВСЕХ УГЛЕВОДОВ
Горение.
Все углеводы горят до углекислого газа и воды.
Например, при

горении глюкозы образуются вода и углекислый газ:
C6H12O6 + 6O2 → 6CO2 + 6H2O
2. Взаимодействие с концентрированной серной кислотой.
Концентрированная серная кислота отнимает воду от углеводов, при этом образуется углерод С («обугливание») и вода.
Например, при действии концентрированной серной кислоты на глюкозу образуются углерод и вода:
C6H12O6 → 6C + 6H2O
Слайд 9КАЧЕСТВЕННЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ
1.Качественная реакция на многоатомные спирты: реакция со свежеосажденным гидроксидом меди(II).

Слайд 102.Реакции на карбонильную группу – CH=O

Слайд 113. Реакция с гидроксидом меди(II) при нагревании

Слайд 124.Окисление глюкозы бромной водой
При окислении глюкозы бромной водой образуется глюконовая кислота: Также

глюкозу можно окислить хлором, бертолетовой солью, азотной кислотой.
Слайд 135. Каталитическое гидрирование
При взаимодействии глюкозы с водородом происходит восстановление карбонильной группы до

спиртового гидроксила, образуется шестиатомный спирт – сорбит.
Слайд 146. Брожение глюкозы
Брожение — это биохимический процесс, основанный на окислительно-восстановительных превращениях органических

соединений в анаэробных условиях.
7. Спиртовое брожение
При спиртовом брожении глюкозы образуются спирт и углекислый газ:
C6H12O6 → 2C2H5OH + 2CO2
8. Молочнокислое брожение
при молочнокислом брожении глюкозы образуется молочная кислота:
Слайд 159. Маслянокислое брожение
При маслянокислом брожении глюкозы образуется масляная кислота (внезапно):
10. Образование

эфиров глюкозы (характерно для циклической формы глюкозы).
Глюкоза способна образовывать простые и сложные эфиры.
Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила.
Например, α-D-глюкоза взаимодействует с метанолом.
При этом образуется монометиловый эфир глюкозы (α-O-метил-D-глюкозид):
Слайд 16В более жестких условиях (например, с CH3-I) возможно алкилирование и по другим

оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные эфиры как с минеральными, так и с карбоновыми кислотами.
Например, β-D-глюкоза реагирует с уксусным ангидридом в соотношении 1:5 с образованием пентаацетата глюкозы (β-пентаацетил-D-глюкозы):
Слайд 17 Получение глюкозы
А)Гидролиз крахмала
В присутствии кислот крахмал гидролизуется:
(C6H10O5)n + nH2O → nC6H12O6

Слайд 18Б)Синтез из формальдегида
Реакция была впервые изучена А.М. Бутлеровым. Синтез проходит в присутствии

гидроксида кальция:
6CH2=On → C6H12O6
В) Фотосинтез
В растениях углеводы образуются в результате реакции фотосинтеза из CO2 и Н2О:
6CO2 + 6H2O → C6H12O6 + 6O2
Слайд 19 Фруктоза
Фруктоза — структурный изомер глюкозы. Это кетоноспирт (кетоза): она тоже может

существовать в циклических формах (фуранозы); кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза.
Она содержит шесть атомов углерода, одну кетоновую группу и пять гидроксогрупп.
Химические свойства фруктозы связаны с наличием кетонной и пяти гидроксильных групп.
При гидрировании фруктозы также получается сорбит.
Слайд 20Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и
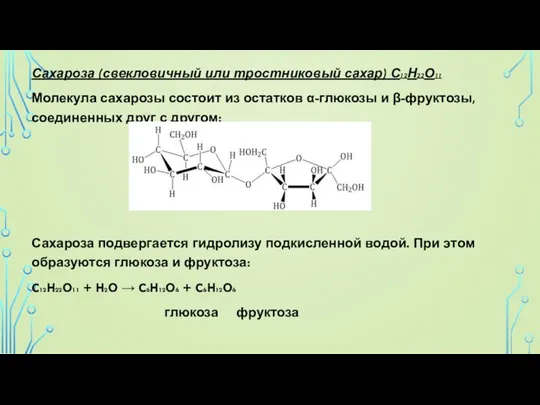
β-фруктозы, соединенных друг с другом:
Сахароза подвергается гидролизу подкисленной водой. При этом образуются глюкоза и фруктоза:
C12H22O11 + H2O → C6H12O6 + C6H12O6
глюкоза фруктоза
Слайд 21Мальтоза С12Н22О11
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом

при гидролизе крахмала.
Мальтоза является восстанавливающим дисахаридом (одно из циклических звеньев может раскрываться в альдегидную группу) и вступает в реакции, характерные для альдегидов.
При гидролизе мальтозы образуется глюкоза.
C12H22O11 + H2O → 2C6H12O6
Слайд 22 Полисахариды
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом

при гидролизе крахмала.
Полисахариды — это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители — крахмал и целлюлоза — построены из остатков одного моносахарида — глюкозы.
Слайд 23В его состав входят:
амилоза (внутренняя часть крахмального зерна) – 10-20%
амилопектин (оболочка крахмального

зерна) – 80-90%
Свойства крахмала
Гидролиз крахмала: при кипячении в кислой среде крахмал последовательно гидролизуется:
Крахмал не дает реакцию “серебряного зеркала” и не восстанавливает гидроксид меди (II).
Качественная реакция на крахмал: синее окрашивание с раствором йода.
Слайд 24 Целлюлоза
Целлюлоза (клетчатка) – наиболее распространенный растительный полисахарид. Цепи целлюлозы построены из

остатков β-глюкозы и имеют линейное строение.
Слайд 25 Свойства целлюлозы
Образование сложных эфиров с азотной и уксусной кислотами.
Так как в

звене целлюлозы содержится 3 гидроксильные группы, то при нитровании целлюлозы избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
Слайд 26Ацилирование целлюлозы.
При действии на целлюлозу уксусного ангидрида (упрощённо-уксусной кислоты) происходит реакция этерификации,

при этом возможно участие в реакции 1, 2 и 3 групп ОН.
Получается ацетат целлюлозы – ацетатное волокно.
Гидролиз целлюлозы.
Целлюлоза, подобно крахмалу, в кислой среде может гидролизоваться, в результате тоже получается глюкоза. Но процесс идёт гораздо труднее.
Слайд 27Применение
Практическое значение. углеводов составляют большую (часто основную) часть пищевого рациона человека. В

связи с этим они широко используются в пищевой и кондитерской промышленности (крахмал, сахароза, пектиновые вещества).























 Расчет физических свойств нефтепродуктов. Практическая работа 1
Расчет физических свойств нефтепродуктов. Практическая работа 1 Массовая доля выхода продукта реакции от теоретически возможного
Массовая доля выхода продукта реакции от теоретически возможного Презентация на тему Индикаторы
Презентация на тему Индикаторы  Применение некоторых химических веществ. Задание 1
Применение некоторых химических веществ. Задание 1 Скорость химической реакции
Скорость химической реакции Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Пероксид водорода
Пероксид водорода Презентация на тему ОВР в органической химии
Презентация на тему ОВР в органической химии  Substancje chemiczne
Substancje chemiczne Презентация на тему Применение электролиза
Презентация на тему Применение электролиза  Относительная молекулярная масса вещества
Относительная молекулярная масса вещества Алканы
Алканы Номенклатура и изомерия аренов
Номенклатура и изомерия аренов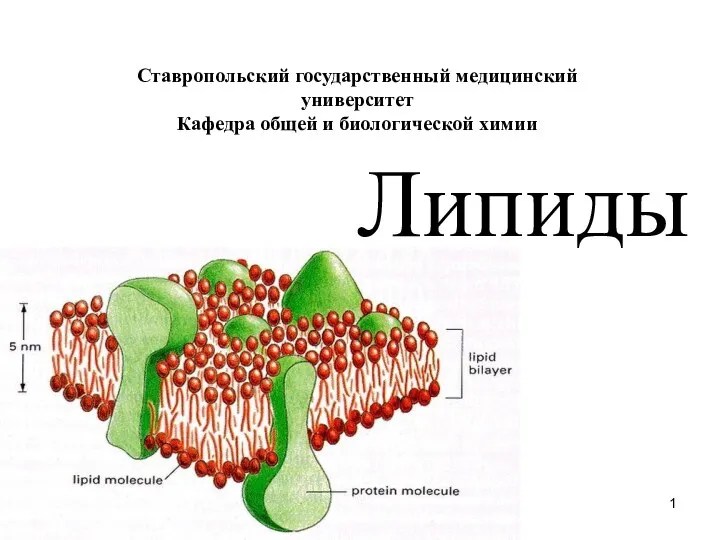 Липиды
Липиды Алканы 10-класс
Алканы 10-класс Теория строения органических соединений
Теория строения органических соединений Металдар мен қорытпалардың құрылысы және қасиеттері
Металдар мен қорытпалардың құрылысы және қасиеттері Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Кислоты, основания и соли как электролиты
Кислоты, основания и соли как электролиты Молекулярно-механическое изнашивание
Молекулярно-механическое изнашивание Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР)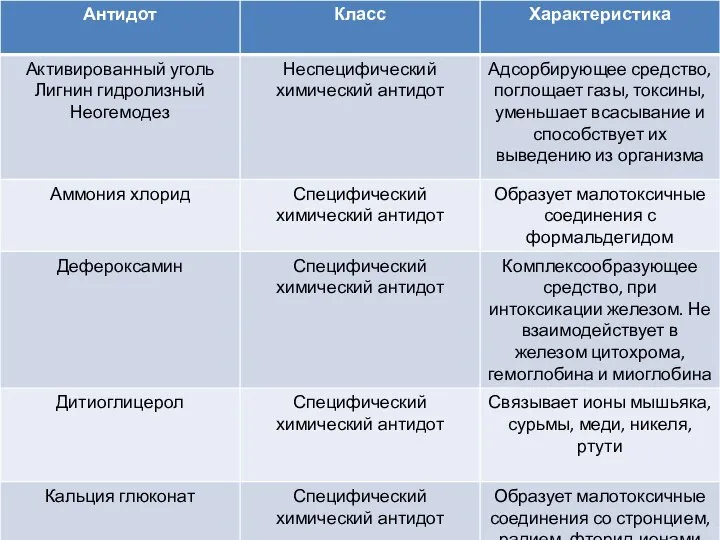 Антидоты. Класс. Характеристика
Антидоты. Класс. Характеристика Кинетика химических и биохимических процессов. Часть 1
Кинетика химических и биохимических процессов. Часть 1 Входное тестирование по химии
Входное тестирование по химии Серная кислота
Серная кислота Органическая химия
Органическая химия Строение атома
Строение атома Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик