Содержание
- 2. ВАЛЕНТНОСТЬ Понятие валентности Правило валентности Определение валентности элементов по формуле их соединений
- 3. Валентность – это способность атомов элементов образовывать определенное число химических связей. Валентность - это важнейшая характеристика
- 4. Валентность определяется числом химических связей, которые образует данный атом с другими атомами в молекуле. Обозначение валентности
- 5. Значения валентности I II III IV V VI VII VIII 1 2 3 4 5 6
- 6. Валентность водорода принята за единицу, т.к. атом водорода всегда образует только 1 химическую связь. Водород в
- 7. Валентность элемента можно также определять по формуле его кислородного соединения, т.к. кислород в соединениях всегда двухвалентен.
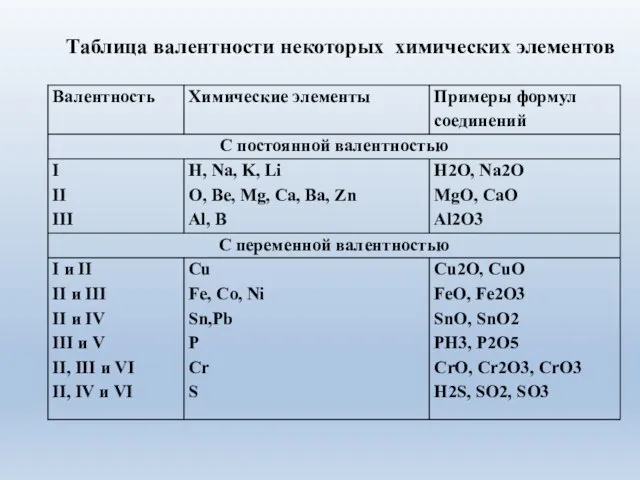
- 8. ЭЛЕМЕНТЫ С ПОСТОЯННОЙ ВАЛЕНТНОСТЬЮ (записать в тетрадь)
- 9. Таблица валентности некоторых химических элементов
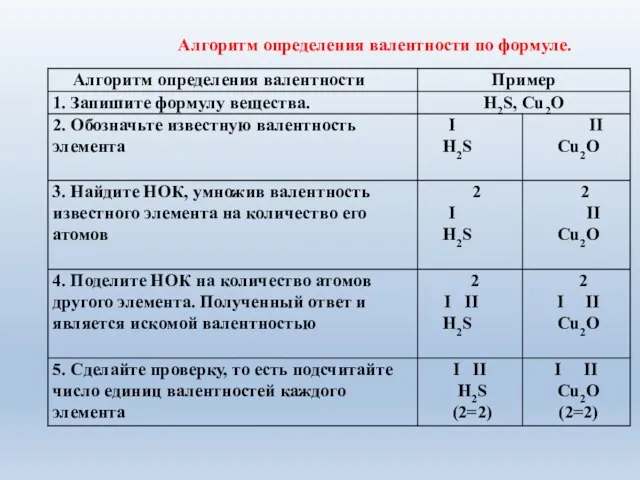
- 10. Алгоритм определения валентности по формуле.
- 11. Соединения, которые состоят из атомов двух элементов, называются бинарными соединениями и выражаются общей формулой:
- 12. Для бинарных соединений существует ПРАВИЛО ВАЛЕНТНОСТИ: Произведение валентности (x) на число атомов (m) одного элемента (A)
- 13. Определение валентности элементов по химической формуле Задача: Определить валентность марганца в его соединении с кислородом Обозначим
- 14. Используя правило валентности и зная валентность элементов составляются ГРАФИЧЕСКИЕ ФОРМУЛЫ ВЕЩЕСТВ Графические формулы веществ – это
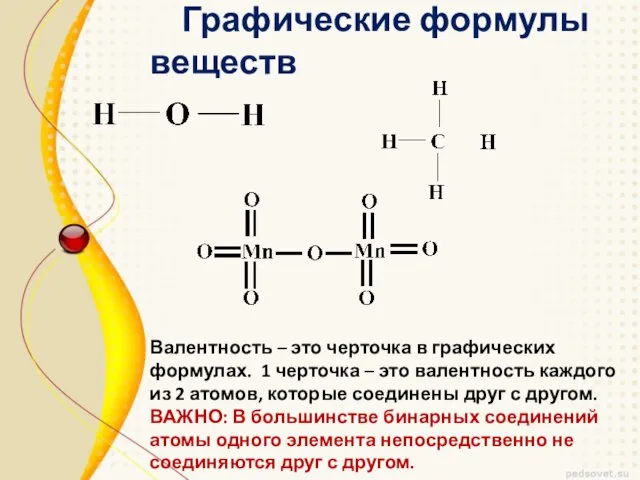
- 15. Графические формулы веществ Валентность – это черточка в графических формулах. 1 черточка – это валентность каждого
- 16. Запомнить Валентность водорода всегда принимают за I (единицу). Кислород в своих соединениях всегда проявляет валентность II.
- 17. В формулах бинарных соединений атом неметалла, проявляющий низшую валентность, всегда стоит на втором месте, а название
- 18. 1.Определить валентность элементов в соединениях: 2. Составить графические формулы этих соединений
- 20. Скачать презентацию














 Ароматерапия
Ароматерапия Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Céramiques lesquelles choisi ?
Céramiques lesquelles choisi ? Арены. 10 класс
Арены. 10 класс Органическая химия. Введение
Органическая химия. Введение Технология получения полиуретанов
Технология получения полиуретанов Практико-ориентированные задачи по химии для студентов гуманитарных специальностей
Практико-ориентированные задачи по химии для студентов гуманитарных специальностей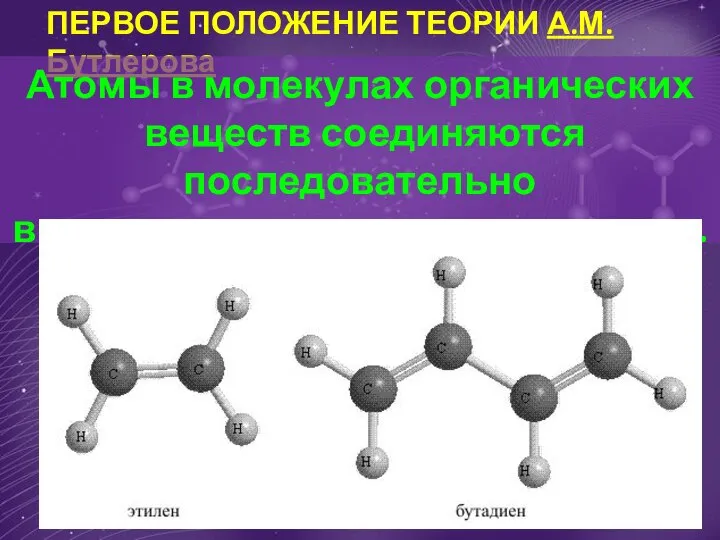 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Презентация на тему Бром
Презентация на тему Бром  Выращивание кристаллов соли и сахара в домашних условиях
Выращивание кристаллов соли и сахара в домашних условиях Презентация на тему Стронций
Презентация на тему Стронций  Алкены
Алкены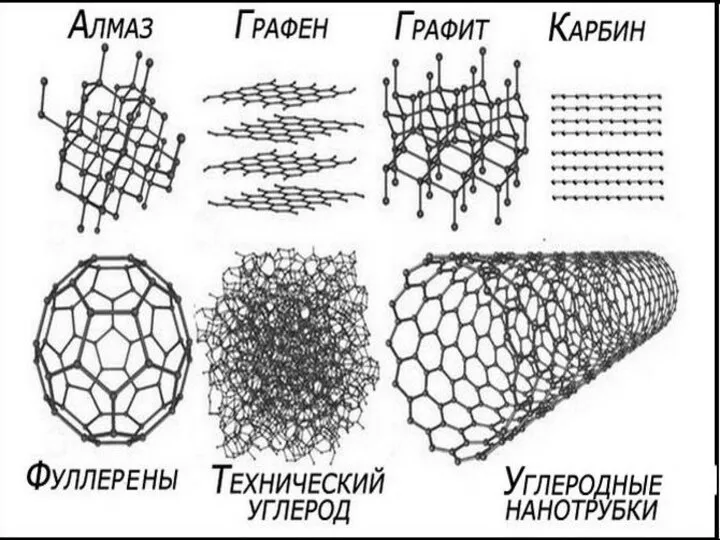 Углеродные нанотрубки
Углеродные нанотрубки Составление формул по валентности. Понятие
Составление формул по валентности. Понятие Положение металлов в периодической системе химических элементов
Положение металлов в периодической системе химических элементов Алканы
Алканы Учебное задание Расчет теплоты сгорания
Учебное задание Расчет теплоты сгорания Избыток, недостаток. Решение задач
Избыток, недостаток. Решение задач Кремний и его соединения
Кремний и его соединения Спирты и фенолы. (Лекция 6.1)
Спирты и фенолы. (Лекция 6.1) Валентность. Определение валентности элемента в оксиде
Валентность. Определение валентности элемента в оксиде Гемоглобин. Структура и свойства молекулы гемоглобина
Гемоглобин. Структура и свойства молекулы гемоглобина Какую воду мы пьем
Какую воду мы пьем Качественная реакция на многоатомные спирты
Качественная реакция на многоатомные спирты Олимпиада Ломоносов
Олимпиада Ломоносов Применение каучука
Применение каучука Презентация на тему Фолиевая кислота
Презентация на тему Фолиевая кислота  Химия в загадках
Химия в загадках