Слайд 32 конкурс «Лаборант».
Лабораторная работа
Тема: Определение веществ.
Оборудование: растворы кислоты, основания, соли, пробирки, подставка

для пробирок, индикатор.
Ход работы:
Вывод: ______________________________________________________________
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Слайд 43 конкурс «Уравняй».
H2 + CuO = Cu + H2O
СаО + Н2О =

Са(ОН)2
Са(ОН)2 = СаО + Н2О
Al + HCl = H2↑ + AlCl3
CaCl2 + Na2CO3 = CaCO3↓ + NaCl
CaBr2 + HF = CaF2↓ + HBr
H2 + O2 = H2O
Zn + CuCl2 = Cu + ZnCl2
NH3 = N2 + H2
Cu + S = CuS
AgF + NaCl = AgCl↓ + NaF
CaCO3 = CaO + CO2 ↑
CuBr2 + NaOH = Cu(OH)2↓ + NaBr
Fe + H2O = H2↑ + Fe2O3
Слайд 65 конкурс «Заполни таблицу».

Слайд 76 конкурс «Решение задач»
1.При восстановлении углем оксида Fe2O3 получили по 20 г

Fe. Сколько граммов оксида было взято?
2. При восстановлении углем оксидов SnO2 получили по 20 г Sn. Сколько граммов оксида было взято?






 Азотная кислота
Азотная кислота Коллоидно-химическая теория схватывания и твердения вяжущих веществ
Коллоидно-химическая теория схватывания и твердения вяжущих веществ Ковалентная химическая связь
Ковалентная химическая связь Reactivi444
Reactivi444 Комлексті қосылыстардың кұрылысы мен қасиеттерін тусіндіретін теория, енгізген 1893 ж А. Вернер
Комлексті қосылыстардың кұрылысы мен қасиеттерін тусіндіретін теория, енгізген 1893 ж А. Вернер Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Арены. Бензол
Арены. Бензол Презентация на тему Амфотерные оксиды и гидроксиды
Презентация на тему Амфотерные оксиды и гидроксиды 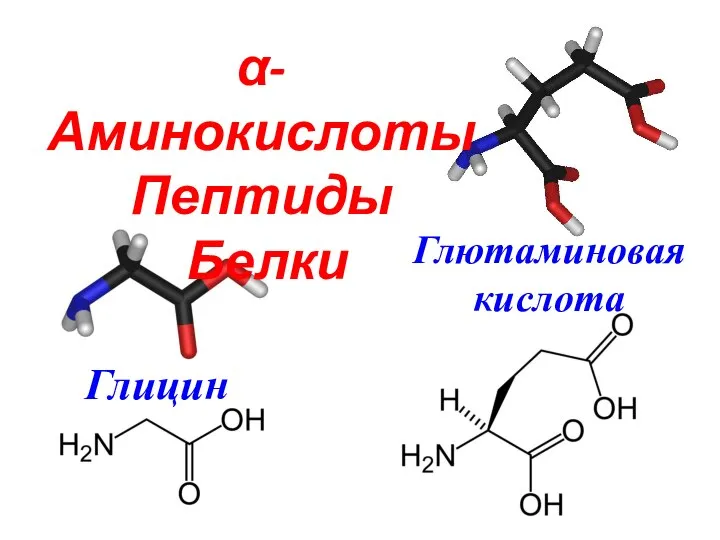 α-Аминокислоты
α-Аминокислоты Классификация и номенклатура аминов. 11 класс
Классификация и номенклатура аминов. 11 класс Получение аммиака и изучение его свойств. Практическая работа № 2
Получение аммиака и изучение его свойств. Практическая работа № 2 Викторина: А не химик ли ты?
Викторина: А не химик ли ты? Электрическая диссоциация
Электрическая диссоциация Щелочные металлы
Щелочные металлы Презентация на тему Движение электрона в атоме
Презентация на тему Движение электрона в атоме  Реакции ионного обмена
Реакции ионного обмена Химические вещества
Химические вещества Химическая связь
Химическая связь Цезий
Цезий Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Презентация на тему Химические свойства металлов
Презентация на тему Химические свойства металлов  Презентация на тему Войди в природу другом
Презентация на тему Войди в природу другом 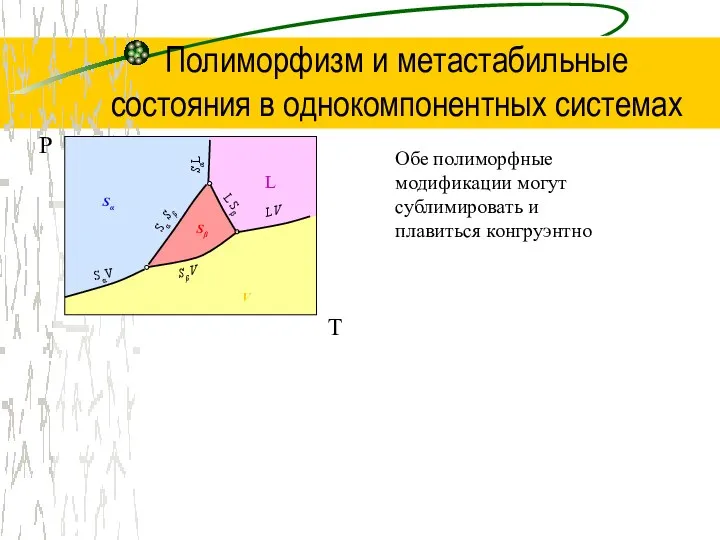 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Кислотність бджолиного обніжжя
Кислотність бджолиного обніжжя Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Кроссворд. Плотность
Кроссворд. Плотность Атом. Ядро и электронная оболочка. Изотопы. Строение электронных оболочек атома. Понятие об орбиталях
Атом. Ядро и электронная оболочка. Изотопы. Строение электронных оболочек атома. Понятие об орбиталях Svins. Iegūšana
Svins. Iegūšana