Содержание
- 2. Положение химического элемента Заряд ядра или число протонов Ядерные реакции
- 3. Протекают с выделением большого количества энергии Другого химического элемента может не образоваться Изотопы
- 4. ИЗОТОПЫ - разновидности атомов одного и того же химического элемента, имеющие одинаковый заряд ядра, но разное
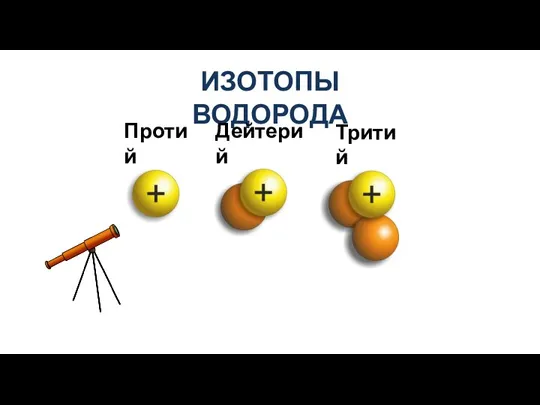
- 5. ИЗОТОПЫ ВОДОРОДА Протий Дейтерий Тритий
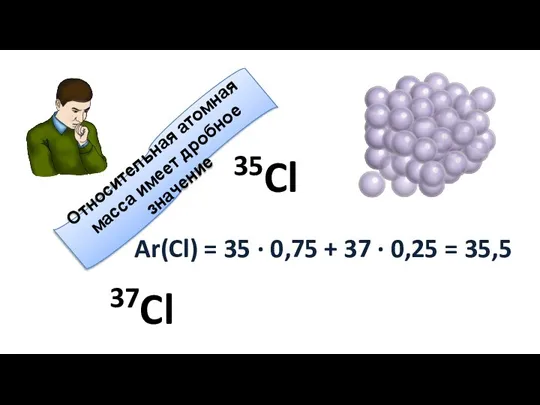
- 6. Относительная атомная масса имеет дробное значение Ar(Cl) = 35 ∙ 0,75 + 37 ∙ 0,25 =
- 8. Скачать презентацию


 Химическое равновесие
Химическое равновесие Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Моющие и чистящие средства
Моющие и чистящие средства Основные химические законы
Основные химические законы Соли: получение
Соли: получение Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Khim_8
Khim_8 Химические реакции
Химические реакции Систематизация знаний по периодической системе химических элементов
Систематизация знаний по периодической системе химических элементов химия
химия Nevarne snovi
Nevarne snovi Основания. Классификация
Основания. Классификация Стелс-материалы
Стелс-материалы Тип кристаллической решетки у белого фосфора…. Тест
Тип кристаллической решетки у белого фосфора…. Тест Классификация и свойства кислот
Классификация и свойства кислот Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Реакции разложения и соединения
Реакции разложения и соединения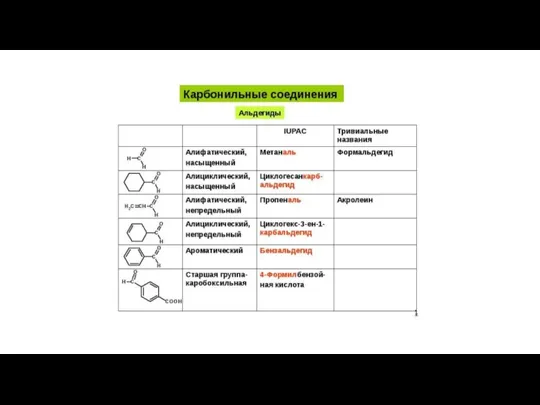 Карбонильные соединения (альдегиды)
Карбонильные соединения (альдегиды) карбоновые кислоты
карбоновые кислоты Вуглеводи. Групи
Вуглеводи. Групи Вычисление температур стеклования полимера при различных степенях отверждения смолы
Вычисление температур стеклования полимера при различных степенях отверждения смолы Сера
Сера Валенттілік. Атом-молекулалы ілім
Валенттілік. Атом-молекулалы ілім Классификация органических соединений
Классификация органических соединений Метанол. Краткая характеристика
Метанол. Краткая характеристика