Содержание
- 2. Колонизационный спектр здорового человека Анаэробы Зеленящие стрептококки Энтерококки CNS 6 «внебольничных» потенциально патогенных микроорганизмов S. pneumoniae
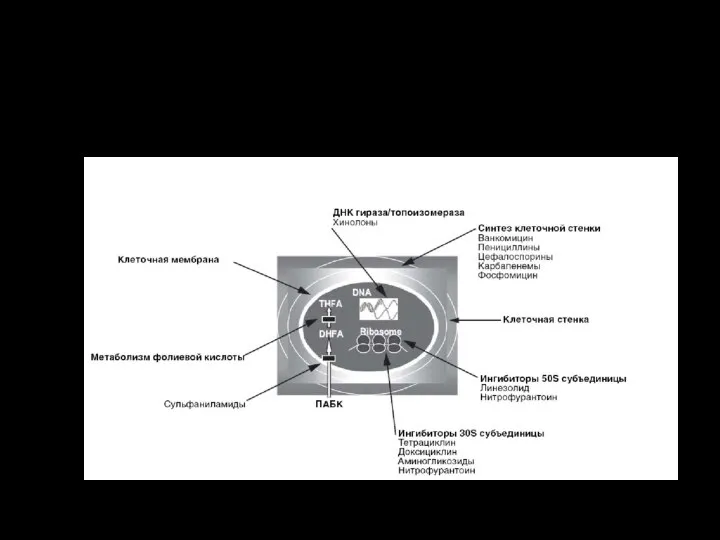
- 3. Мишени и механизмы действия антимикробных препаратов
- 4. Антипсевдомонадные пенициллины Карбокси-П: карбенициллин, тикарциллин Уреидо-П: пиперациллин, азлоциллин Антимикробная активность: Высокая - стрептококки, гемофильная палочка Умеренная
- 5. Антипсевдомонадные пенициллины карбоксипенициллины, уреидопенициллины Клиническое применение: инфекции, вызванные P. aeruginosa (+ АГ) смешанные аэробно-анаэробные инфекции (+
- 6. Защищенные антипсевдомонадные пенициллины Тикарциллин/клавулановая кислота пиперациллин/тазобактам Клиническое применение Инфекции интраабдоминальные и малого таза Лёгочные нагноения Респиратор-ассоциированная
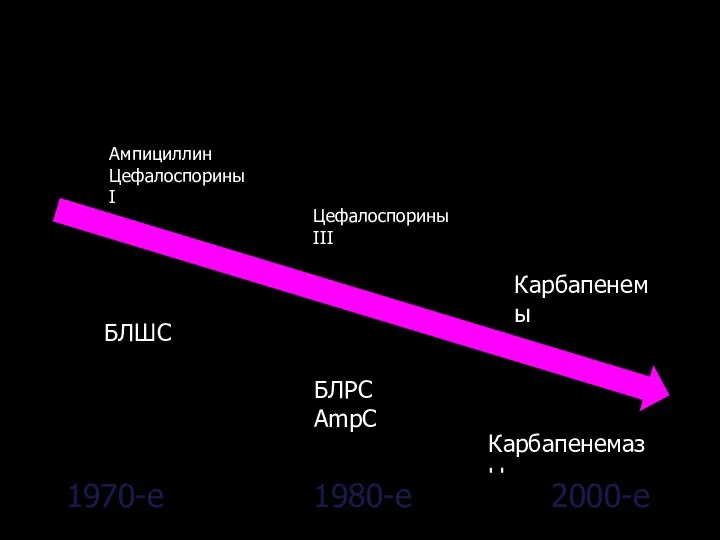
- 8. Природная активность и приобрете㴄〄伄 䀀㔄㜄㠄䄄䈄㔄㴄䈄㴄㸄䄄䈄䰄 䘀㔄䐄〄㬄㸄䄄㼄㸄䀄㠄㴄㸄㈄䬄䔄 㴄䈄㠄㠄㸄䈄㠄㨄㸄㈄ 䤀ⴀ䤀嘀 㼀㸄㨄㸄㬄㔄㴄㠄㤄_x0004_
- 9. Клиническое применение цефалоспоринов Цефалоспорины 1-го поколения (Цефазолин) Интраоперационная профилактика Цефалоспорины 2-го поколения (Цефуроксим) Интраоперационная профилактика Инфекции
- 10. Отличительные особенности цефалоспоринов III поколения Цефотаксим Наиболее высокая активность in vitro в отношении Enterobacteriaceae Цефтриаксон Наиболее
- 11. Клиническое применение цефалоспоринов III и IV поколений в качестве средств 1-го ряда Тяжелая внебольничная пневмония (+
- 12. Сравнительная характеристика цефалоспоринов III и IV поколений Активность в отношении Г- бактерий ЦС III = ЦС
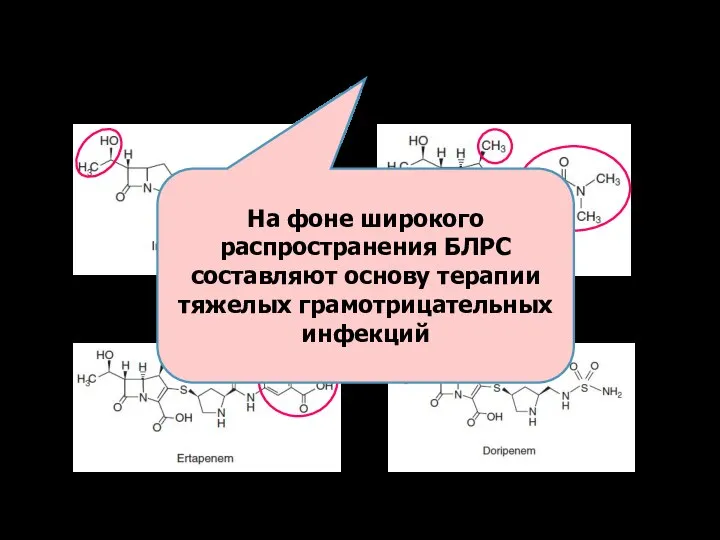
- 14. Карбапенемы На фоне широкого распространения БЛРС составляют основу терапии тяжелых грамотрицательных инфекций
- 15. Механизм действия Подавление синтеза пептидогликана за счет ингибиции активности пенициллинсвязывающих белков (ПСБ) Имипенем ПСБ2 > ПСБ1
- 16. Спектр действия Среди Грам- бактерий природную устойчивость проявляют только Stenotrophomonas maltophilia
- 17. Сравнительная характеристика карбапенемов Имипенем Применяется с циластатином Связывается с ПСБ2 Не применяется для лечения менингита Применяется
- 18. Различия в антимикробной активности имипенема и меропенема in vitro Имипенем в 2-4 раза превосходит меропенем в
- 19. Клиническое применение и режим дозирования карбапенемов Имипенем и меропенем в/в 1,5-2 г/с (0,5 г х 3-4)
- 21. Эртапенем 1 г/сут, однократно, в/в или в/м (спектр активности – как у имипенема и меропенема минус
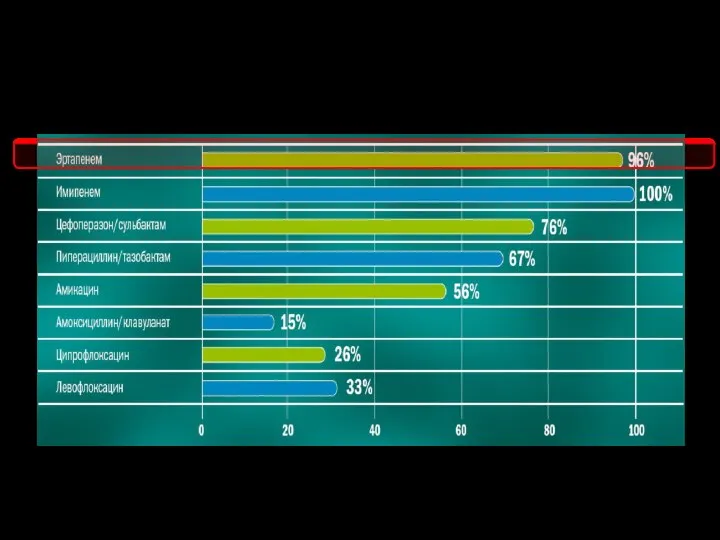
- 22. Энтеробактерии, продуцирующие БЛРС, высокочувствительны к эртапенему Данные исследования РеВАНШ, 2006-2008 гг.
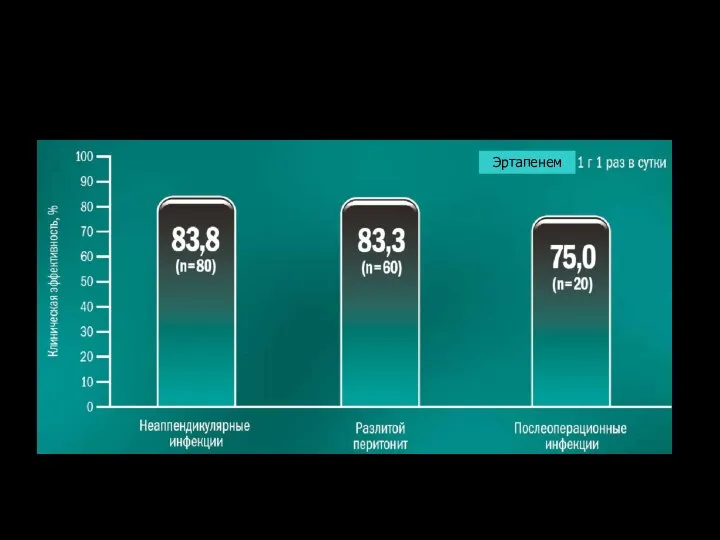
- 23. Эртапенем – препарат выбора для эмпирической терапии интраабдоминальных инфекций Показатели общей эффективности эртапенема при среднетяжелых и
- 24. Дорипенем в клинической практике Только один новый антибиотик одобрен FDA с 2010 года, несколько новых препаратов
- 25. Дорипенем в клинической практике Дорипенем обладает высокой активностью против MSSA, но не эффективен против MRSA, Enterococcus
- 26. Дорипенем в клинической практике Дорипенем зарегистрирован для лечения осложненных абдоминальных инфекций, инфекции мочевых путей, госпитальной пневмонии
- 27. Три десятилетия ингибиторов β-лактамаз Livermore, D.M., R. Hope, S. Mushtag, and M. Warner. 2008. Orthodox and
- 28. Аминогликозиды Стрептомицин - 1944 60-е годы 80-е годы Неомицин - 1949 Гентамицин Амикацин Канамицин - 1957
- 29. Недостатки аминогликозидов Увеличение резистентности бактерий (канамицин, гентамицин, тобрамицин) Невысокие концентрации в тканях бронхолегочной системы Снижение бактерицидной
- 30. Аминогликозиды Стратегия выбора препарата Гентамицин Базовый препарат в отделениях общего профиля Амикацин Отделения интенсивной терапии Высокий
- 31. Применение аминогликозидов Целесообразно применение только при госпитальных инфекциях. При эмпирической терапии - только в комбинации с
- 32. Нетилмицин Активность в отношении гентамицино- и тобрамицинорезистентных штаммов микроорганизмов Низкая нефро- и ототоксичность Может быть использован
- 33. Фторхинолоны Антимикробная активность Высокая: грамотрицательные бактерии Умеренная: стафилококки, псевдомонады Слабая: пневмококки, анаэробы [ ципрофлоксацин > офлоксацин
- 34. Продажи антибактериальных препаратов разных групп в 2009 г (млрд., USD) IMS Health. IMS MIDAS (2009)
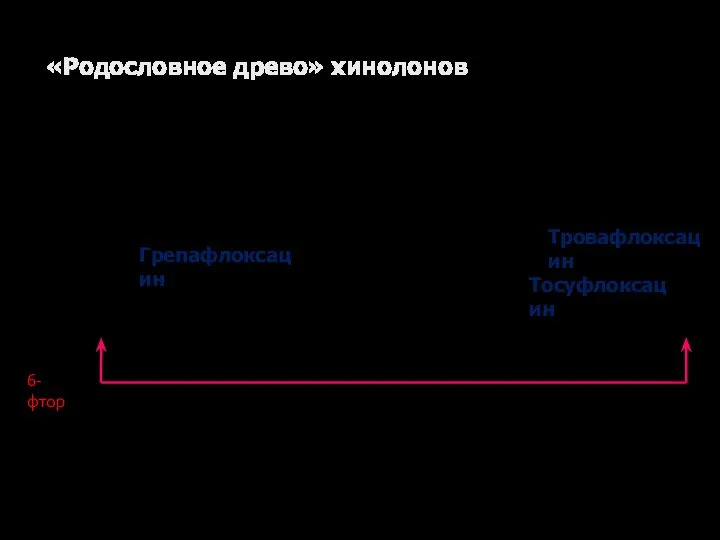
- 35. Хлорохин Хинолоны Нафтуридоны Налидиксовая к-та Норфлоксацин Эноксацин Тосуфлоксацин Тровафлоксацин Гемифлоксацин Офлоксацин Ципрофлоксацин Левофлоксацин Грепафлоксацин Спарфлоксацин Клинафлоксацин
- 38. Сравнительная активность в отношении Грам (-) флоры Нор Ципро*, Офло Мокси, Геми Пефло Лево Спар -----------------------------------------------------
- 39. Сравнительная активность в отношении Грам (+) флоры и других микроорганизмов Нор Ципро*, Офло Мокси, Геми Пефло,
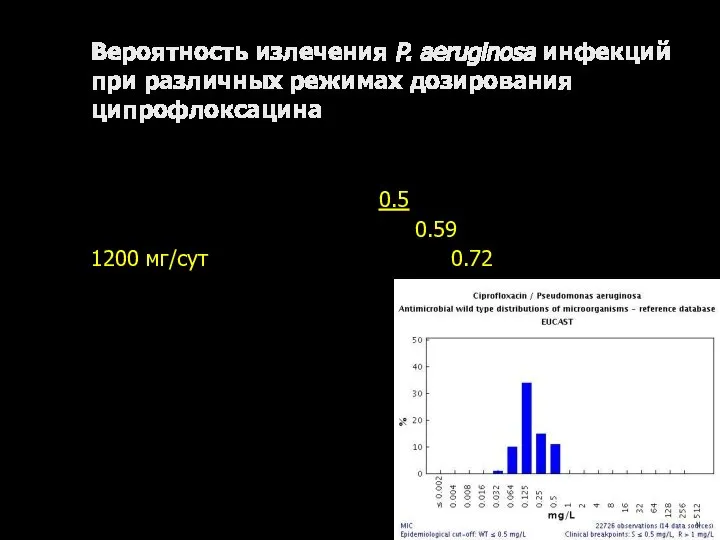
- 40. Вероятность излечения P. aeruginosa инфекций при различных режимах дозирования ципрофлоксацина МПК (мкг/мл) P. aeruginosa 0.125 0.25
- 42. Показания для ципрофлоксацина (ТКФС) Инфекции ЛОР-органов (острый синусит); Инфекции почек и мочевыводящих путей (цистит, пиелонефрит); Осложненные
- 44. Ассоциированная устойчивость Применение фторхинолонов – один из ведущих факторов риска распространения MRSA и устойчивости к карбпенемам
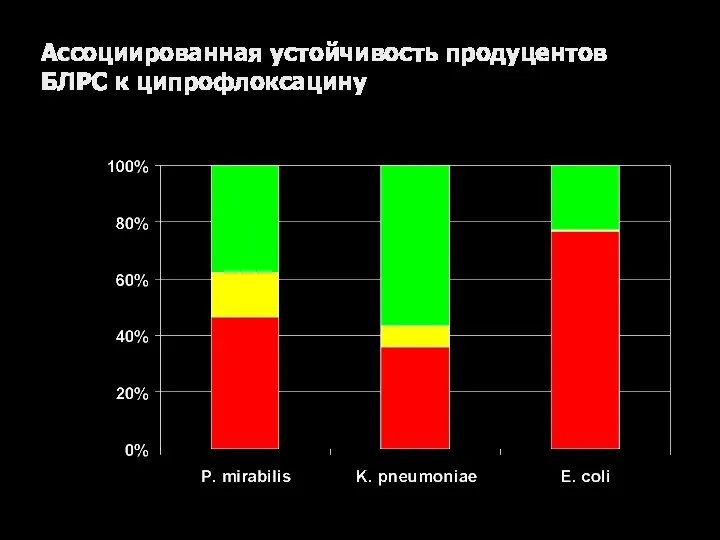
- 45. Ассоциированная устойчивость продуцентов БЛРС к ципрофлоксацину
- 46. Появление устойчивости к фторхинолонам Первое сообщение Lewis DA, Brook MG, Shafi MS. High level ciprofloxacin resistant
- 47. Новые хинолоны в медицинской практике Гареноксацин (Япония, 2007) Повышенная антипневмококковая активность, MRSA, VRE Ситафлоксацин (Япония, 2008)
- 48. Хинолоны на разных стадиях изучения Клиника Делафлоксацин, финафлоксацин, прулифлоксацин, забофлоксацин, озеноксацин, немоноксацин Преодоление устойчивости Грам+ и
- 49. Заключение Хинолоны – один из ведущих классов антибактериальных средств При наличии эффективных антибактериальных средств других классов
- 51. Эффективность и безопасность даптомицина у пациентов с Грам+ бактериемией и онкологическими заболеваниями *Клинический и микробиологический ответ
- 52. Антимикробная терапия Ренессанс «старых» антибиотиков Ни одного антибиотика среди 89 одобренных новых лекарственных средств (2002 г.)
- 53. Полимиксины Лечение НПИВЛ, вызванной A. baumannii Колистин vs имипенем/циластин Нет достоверных различий по частоте развития ОПН
- 54. Фосфомицин Бактерицидное действие Широкий спектр MRSA Гликопептид-чувствительные и резистентные энтерококки Большое число грамотрицательных бактерий
- 55. Фузидиновая кислота (ФК) Перспективно использование ФК при лечении средне- и тяжелых стафилококковых инфекций вызванных штаммами резистентными
- 57. Другие антибиотики Триметоприм/сульфаметоксазол Высокая эффективность при инфекциях вызванных S. maltophilia Препарат выбора при пневмонии, вызванной Pneumocystis
- 58. Новые антимикробные препараты Даптомицин (циклический липопептид) действует на мембрану бактериальных клеток. Активен в отношении Гр+, включая
- 60. Новые антимикробные препараты Тебипенем (карбапенем для приема per os). Действует на Гр+ и Гр-, кроме P.
- 61. Новые антимикробные препараты Новые фторхинолоны (некоторые обладают активностью в отношении MRSA): балофлоксацин, гаренофлоксацин, гемифлоксацин, ципрофлоксацин ХР,
- 62. Новые антимикробные препараты Цефтобипрол – антиMRSA цефем, активен в отношении стафилококков (включая MRSA и VISA), пневмококков,
- 63. На стадии доклинических исследований Ингибиторы MurA (фермента, участвующего в синтезе КС) Ингибиторы систем эффлюкса Конъюгаты сидерофора
- 64. Бренды или дженерики? Опыт сравнения Препарат – цефтриаксон 34 дженерика производства Европы,Азии,Латинской Америки. Сравнение фармацевтического качества
- 65. Результаты Все 34 генерика не соответствовали стандартам оригинального препарата Наиболее частое нарушение – наличие продукта разложения
- 66. Патологический колонизационный спектр Аэробные Гр- микроорганизмы Klebsiella spp. Proteus spp. Morganella spp. Enterobacter spp. Citrobacter spp.
- 67. «Проблемные» возбудители инфекций в хирургии Enterobacteriaceae (Klebsiella spp., E. coli, Proteus spp.) – продуценты БЛРС: ненадежны
- 68. Механизмы устойчивости Гидролиз бета-лактамазами Снижение проницаемости Активное выведение Модификация мишеней Комбинация различных механизмов
- 69. Карбапенемазы класса А Класс А – подавляются клавуланатом, некоторые не разрушают цеф III и азтреонам, карбапенемы
- 70. Карбапенемазы класса D Класс D – более 100 производных, мало чувствительны к клавуланату, карбапенемазную активность проявляют
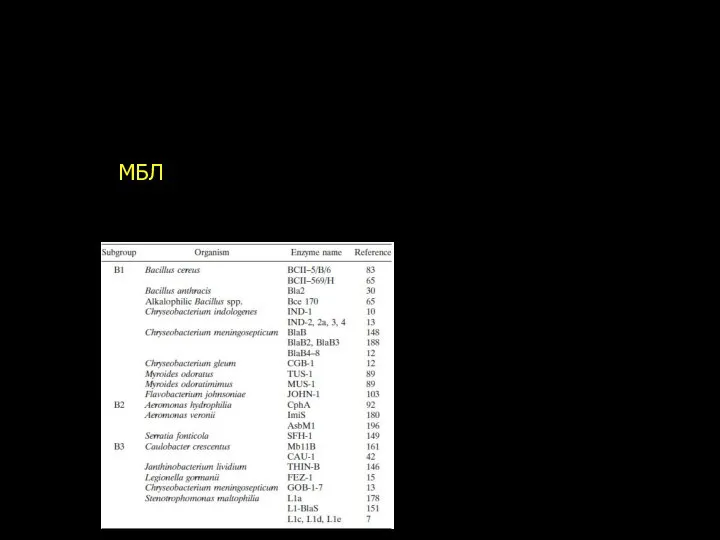
- 71. Карбапенемазы класса В – металло-бета-лактамазы МБЛ – не подавляются клавуланатом, чувствительны к ЭДТА Хромосомные МБЛ широко
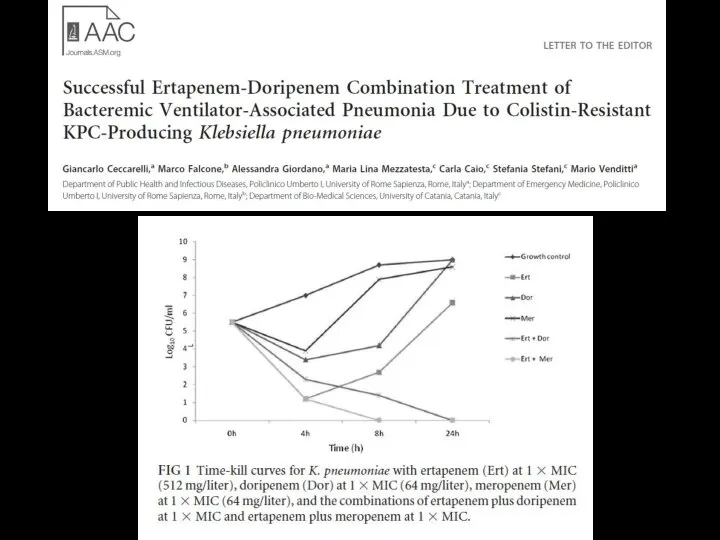
- 72. Комбинация двух карбапенемов против КП-нечувствительных возбудителей Экспериментальные данные: КРС имеют наибольшее сродство к эртапенему. Суицидное ингибирование
- 75. Пути преодоления механизмов бактериальной резистентности к β- лактамным антибиотикам Использование специальных веществ, инактивирующие β-лактамазы, и тем
- 76. Пути преодоления механизмов бактериальной резистентности к β- лактамным антибиотикам Использование специальных веществ, инактивирующих β-лактамазы Клавулановая кислота
- 77. Грамотрицательные возбудители в ОИТ Продуценты плазмидных БЛРС Klebsiella spp E. coli P. mirabilis
- 78. Грамотрицательные возбудители в ОИТ продуценты хромосомных бета-лактамаз класса С (AmpC) Enterobacter spp. Serratia marcescens Citrobacter fr.
- 79. Pseudomonas aeruginosa 20-30% всех случаев ГИ связано с P. aeruginosa Первичное инфицирование – при иммунодефицитах и
- 80. Устойчивость P. aeruginosa Преимущественная комбинация трех механизмов Гиперпродукция хромосомных бета-лактамаз AmpC Активация эффлюкса Модификация или утрата
- 83. Устойчивость Enterobacteriaceae В РФ устойчивость энтеробактерий к карбапенемам остается редкостью При выявлении устойчивого фенотипа необходимо подтверждение
- 84. Геннадий Онищенко: Бактерии с геном NDM-1 России не грозят По сообщению РИА Новости, главный государственный санитарный
- 85. Предпосылки для быстрого распространения Локализация генов в составе подвижных генетических элементов – интегронов Обеспечивают перемещение генетической
- 86. Возможности терапии Высокая частота ассоциированной устойчивости – возможности фторхинолонов и аминогликозидов ограничены Карбапенемы При невысоком уровне
- 87. Правила лечения НИ, вызванных Pseudomonas aeruginosa чувствительность P. aeruginosa предсказать сложно – необходим локальный мониторинг! наибольшая
- 88. Правила лечения НИ, вызванных Pseudomonas aeruginosa нередки случаи выделения Pseudomonas aeruginosa, устойчивой ко всем АМП, кроме
- 89. Проблемные грам-положительные возбудители (MRSA, CNS, Enterococcus spp) Гликопептиды (ванкомицин, тейкопланин) Оксазолидиноны (линезолид)
- 90. Современный феномен агрессивности грамположительных бактерий обусловлен Активным внедрением в клинику инвазивных вмешательств, нарушающих целостность кожи и
- 91. Современный феномен агрессивности грамположительных бактерий обусловлен Ростом числа операций протезирования суставов и пр. Широким использованием иммунодепрессантов,
- 92. Энтерококки всё чаще становятся причиной тяжёлых, жизнеугрожающих инфекции Энтерококки – важнейшие возбудители госпитальных инфекций. Являются, наряду
- 93. Роль энтерококков в хирургии E. faecalis (85%); E. faecium (15%) «Безвредный член кишечного клуба» (S.E. Wilson,
- 94. Система “Quorum sensing” в патогенезе инфекционного процесса Система поддерживает стабильность популяции бактерий внутри биоплёнки на инородных
- 95. Программы терапии инфекций, вызванных MRSA Документированная эффективность Ванкомицин +/- гентамицин Ванкомицин + рифампицин Линезолид Предполагаемая эффективность
- 96. Возможности антибактериальной терапии энтерококковых инфекций Enterococcus faecalis Чувствительный к ампициллину Ампициллин При тяжелых инфекциях (+ гентамицин)
- 97. Возможности антибактериальной терапии энтерококковых инфекций Enterococcus faecium Чувствительный к ванкомицину Ванкомицин + гентамицин Линезолид Устойчивый к
- 98. Длительность лечения энтерококковых инфекций При большинстве инфекций 7-10 дней При выделении резистентных штаммов сроки лечения определяются
- 99. Возможности антибактериальной терапии энтерококковых инфекций Enterococcus faecalis Чувствительный к ампициллину Ампициллин При тяжелых инфекциях (+ гентамицин)
- 100. Возможности антибактериальной терапии энтерококковых инфекций Enterococcus faecium Чувствительный к ванкомицину Ванкомицин + гентамицин Линезолид Устойчивый к
- 101. Правила лечения НИ, вызванных продуцентами БЛРС Не назначать ЦIII даже при чувствительности in vitro Наиболее надежны
- 102. Препараты для лечения инфекций, вызванных грамположительными микроорганизмами Метициллинчувствительные штаммы - оксациллин Метициллинрезистентные штаммы - ванкомицин, рифампицин,
- 103. Препараты, наиболее «надежные» при тяжелых нозокомиальных инфекциях у хирургических больных Активные в отношении Гр(-) возбудителей Меропенем
- 104. Правила лечения НИ, вызванных Pseudomonas aeruginosa чувствительность P. aeruginosa предсказать сложно – необходим локальный мониторинг! наибольшая
- 105. Какие антибиотики нужны в ОРИТ?
- 106. Внедрение новых АМП и чувствительность Гр(-) флоры Ампициллин Цефалоспорины I БЛШС Цефалоспорины III БЛРС AmpC Карбапенемы
- 107. Особенности ОРИТ Значительное селективное давление антибиотиков Ослабление физиологических барьеров Интенсивное перекрестное инфицирование ОРИТ – зона повышенного
- 108. Рекомендуемые режимы АМТ при внебольничных инфекциях При отсутствии факторов риска: Цефалоспорины без антисинегнойной активности ± метронидазол
- 109. АМТ «ранних» нозокомиальных инфекций вне ОРИТ (риск БЛРС ± MRSA) Эртапенем При высоком риске MRSA +
- 110. АМТ «поздних» нозокомиальных инфекций в ОРИТ (риск инфицирования БЛРС, НФГОБ, MRSA, энтерококками) Карбапенемы II группы (дорипенем,
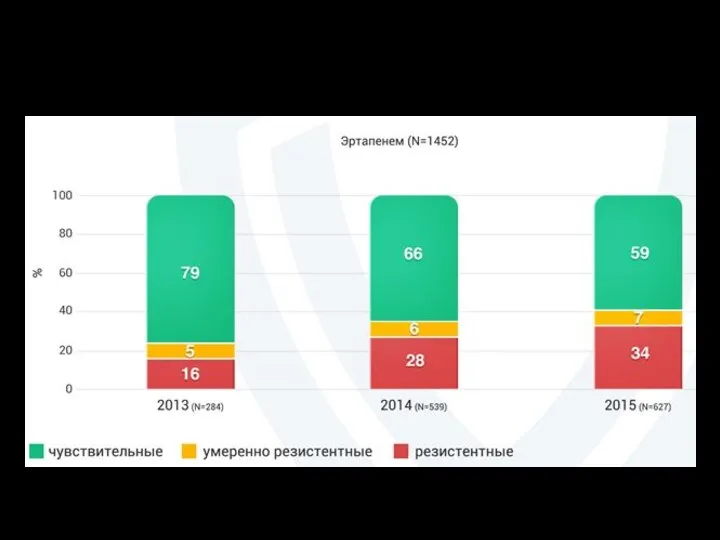
- 111. Динамика доли штаммов K. pneumoniae, резистентных к эртапенему map.antibiotic.ru
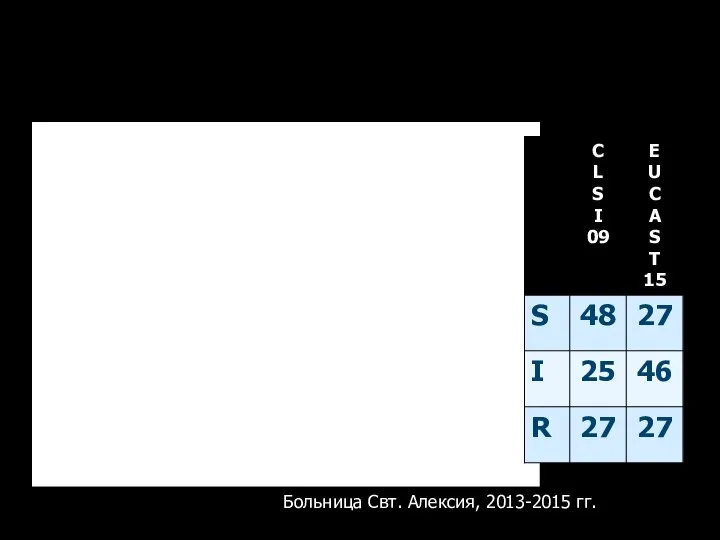
- 112. Распределение нозокомиальных штаммов K.pneumoniae по MПК имипенема Больница Свт. Алексия, 2013-2015 гг.
- 113. Больница Святителя Алексия, г. Москва
- 114. Резистентность P. aeruginosa-возбудителя НП в РФ* и США** *Нозокомиальная пневмония у взрослых. Российские национальные рекомендации 2016
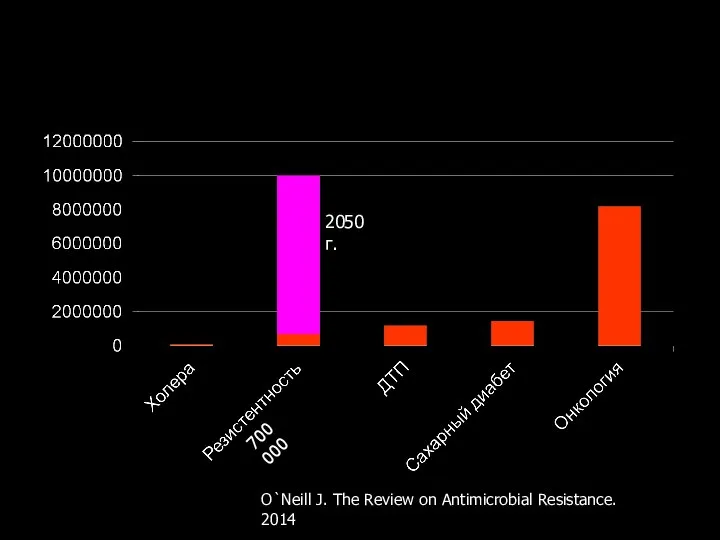
- 115. Ежегодное количество смертей 2050 г. 700 000 O`Neill J. The Review on Antimicrobial Resistance. 2014
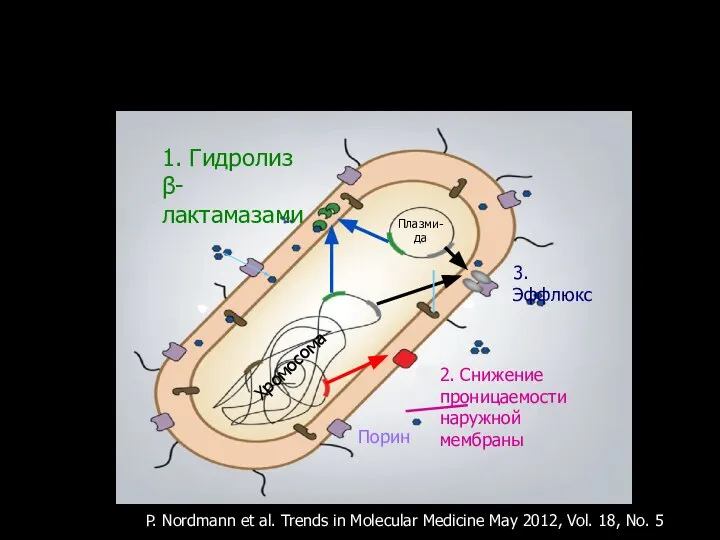
- 116. Механизмы устойчивости грамотрицательных бактерий к бета-лактамам 1. Гидролиз β-лактамазами Хромосома Плазми- да 3. Эффлюкс Порин 2.
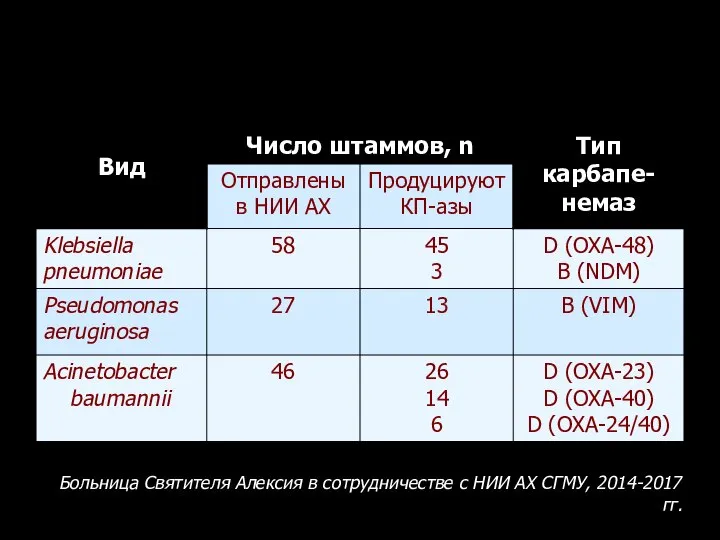
- 117. Механизмы резистентности к КП наших Гр (-) возбудителей Больница Святителя Алексия в сотрудничестве с НИИ АХ
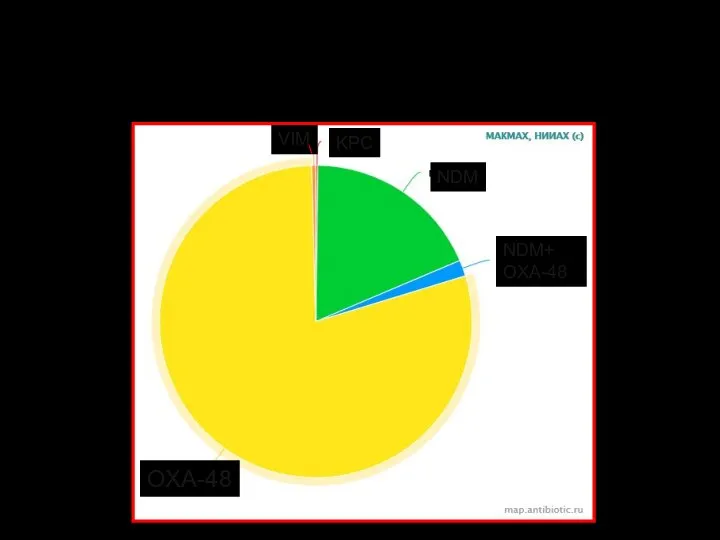
- 118. Распространенность карбапенемаз, продуцируемых Enterobacteriaceae, в РФ OXA-48 NDM+ OXA-48 NDM KPC VIM
- 119. Экспресс-метод ПЦР-диагностики бактериальных и вирусных инфекций Метод позволяет обнаружить в образце биоматериала ДНК MRSA C. difficile
- 120. Факторы риска инфицирования карбапенемазопродуцирующими бактериями Предшествующее применение карбапенемов Высокая распространенность карбапенемрезистентных возбудителей в отделении Поездка в
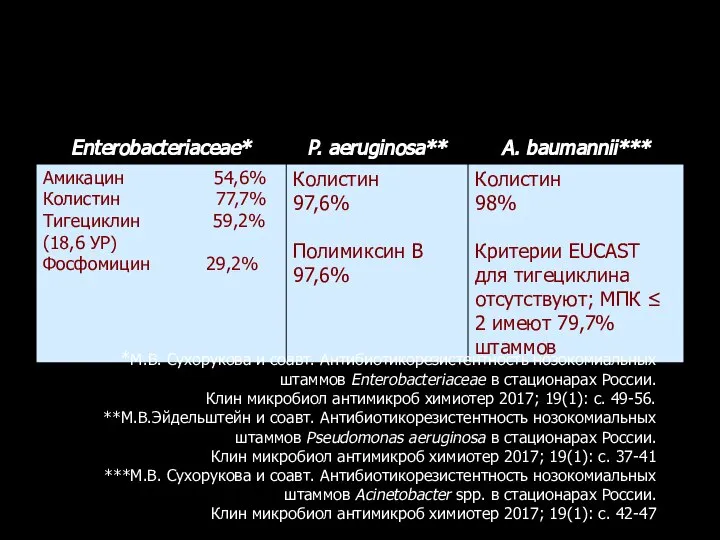
- 122. Чувствительность к АБП продуцентов карбапенемаз *М.В. Сухорукова и соавт. Антибиотикорезистентность нозокомиальных штаммов Enterobacteriaceae в стационарах России.
- 123. Тигециклин (глицилциклин) Связывается с 30S-субъединицей рибосом и нарушает синтез белка. Преодолевает активный эффлюкс и устойчивость рибосомальных
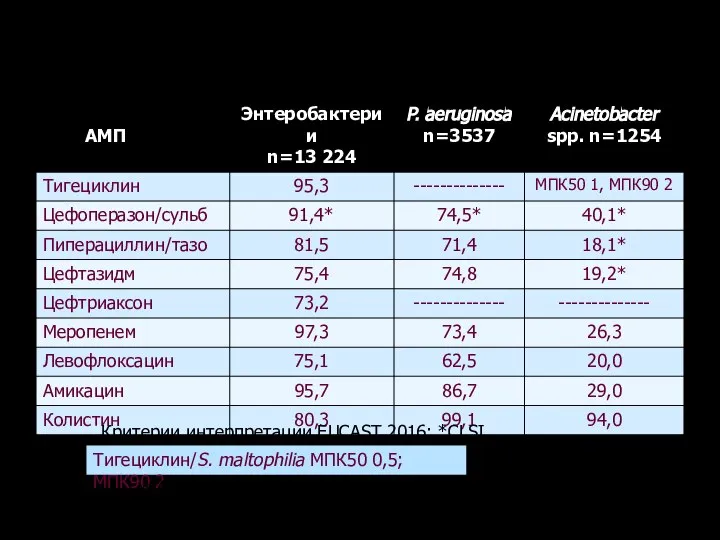
- 124. Чувствительность Гр(-) микроорганизмов к тигециклину и другим АМП (%) Критерии интерпретации EUCAST 2016; *CLSI 2016 Тигециклин/S.
- 125. Полимиксины Механизм действия: взаимодействие катионного пептида и (-) заряженного ЛПС, приводящее к дестабилизации мембраны и гибели
- 126. Karaiskos I. et al. Colistin: Still a lafesaver for the 21st century? Exp Op on Drug
- 127. Цефтазидим/авибактам препарат зарегистрирован в РФ в мае 2017 г. Авибактам – новый не β-лактамный ингибитор β-лактамаз
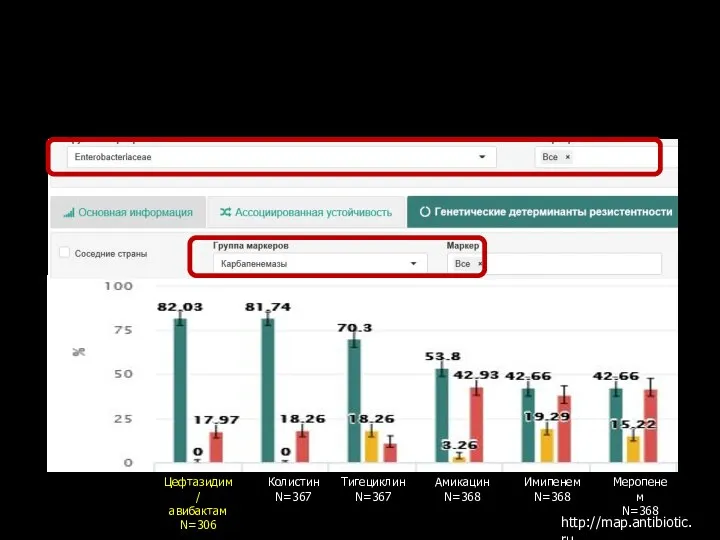
- 128. Активность цефтазидима/авибактама в отношении карбапенемазопродуцирующих энтеробактерий, выделенных в Российской Федерации (1997-2016 гг.) http://map.antibiotic.ru Цефтазидим/ авибактам N=306
- 129. Цефтазидим/авибактам Показания: Осложненные интраабдоминальные инфекции Осложненные инфекции мочевыводящих путей, включая пиелонефрит Госпитальная пневмония, включая пневмонию, связанную
- 130. Цефтазидим/авибактам Схема введения: 2-х часовая инфузия 2 г цефтазидима / 500 мг авибактама каждые 8 часов.
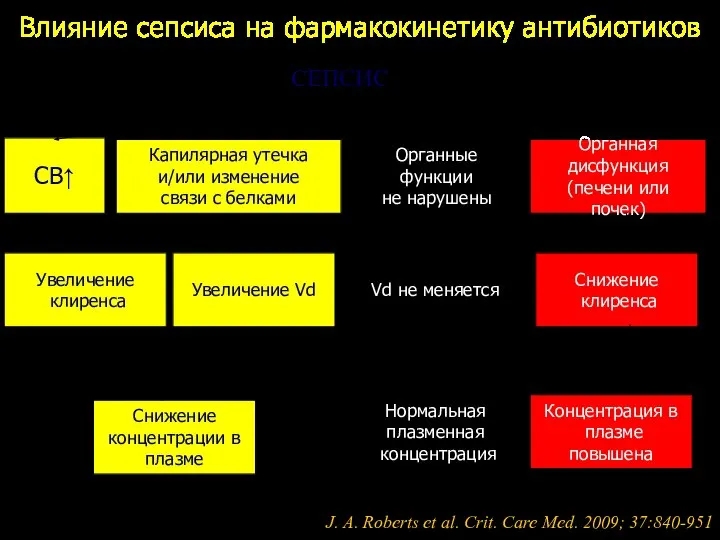
- 131. СЕПСИС СВ↑ Капилярная утечка и/или изменение связи с белками Органные функции не нарушены Органная дисфункция (печени
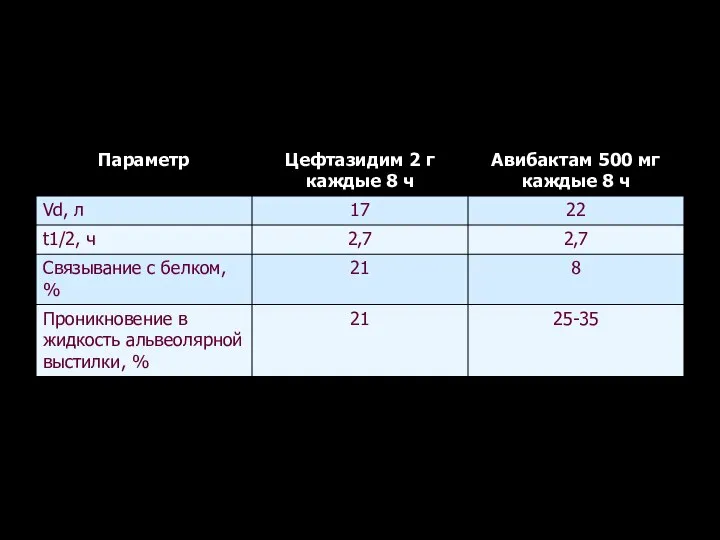
- 132. Фармакокинетика цефтазидима и авибактама Zasowski E.J. et al. Pharmacotherapy 2015; 35(8): 755-770
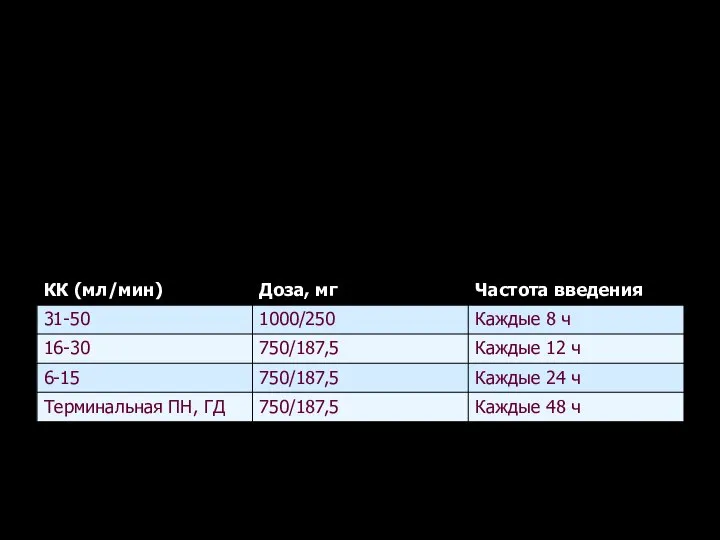
- 133. Дозирование цефтазидима/авибактама у особых популяций пациентов Пожилые пациенты Коррекция дозы не требуется Пациенты с почечной недостаточностью
- 134. REPROVE многоцентровое двойное слепое РКИ III фазы 23 страны 808 больных с нозокомиальной пневмонией, включая НПИВЛ
- 135. RECLAIM 1, 2, 3 Взрослые с оИАИ, n=1043 Цефтазидим/авибактам 2,5 г + метронидазол х 3 р.
- 136. RECAPTURE 1, 2 Взрослые с оИМВП, n=810 Цефтазидим/авибактам 2,5 г + vs Дорипенем 0,5 г х
- 137. Профиль безопасности цефтазидима/авибактама В 7 исследованиях II и III фазы клинических исследований безопасность оценивалась у 2024
- 138. Y. Carmeli et al. Цефтазидим/авибактам по сравнению с наилучшей доступной терапией у пациентов с оИМВП или
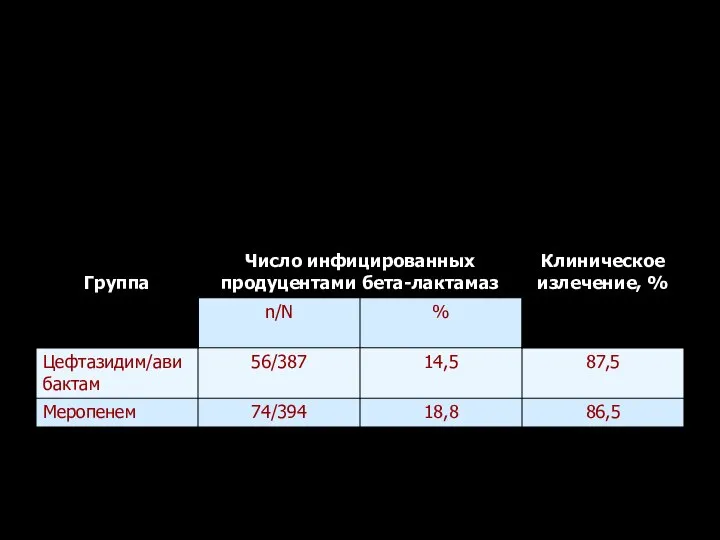
- 139. Клиническая эффективность цефтазидима/авибактама и меропенема у пациентов, инфицированных продуцентами бета-лактамаз (P. aeruginosa и Enterobacteriaceae) R.E. Mendes
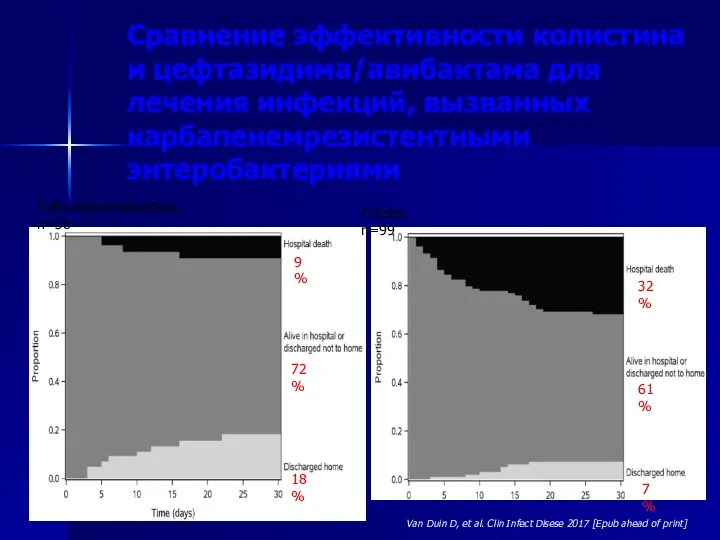
- 140. D. Van Duin et al. Colistin vs Ceftazidime-avibactam in the Treatment of Infections due to Carbapenem-Resistant
- 141. Сравнение эффективности колистина и цефтазидима/авибактама для лечения инфекций, вызванных карбапенемрезистентными энтеробактериями Ceftazidime-avibactam, n=38 Colistin, n=99 9%
- 142. Ограничения полимиксинов Эффективны лишь высокие дозы Недостаточная пенетрация в ткани Нефро- и нейротоксичность Риск суперинфицирования устойчивыми
- 143. 2017; 59: 118–123 Клиническая эффективность цефтазидима/авибактама в сравнении с другими активными препаратами для лечения бактериемии, вызванной
- 144. Результаты лечения цефтазидимом/ авибактамом и другими АМП
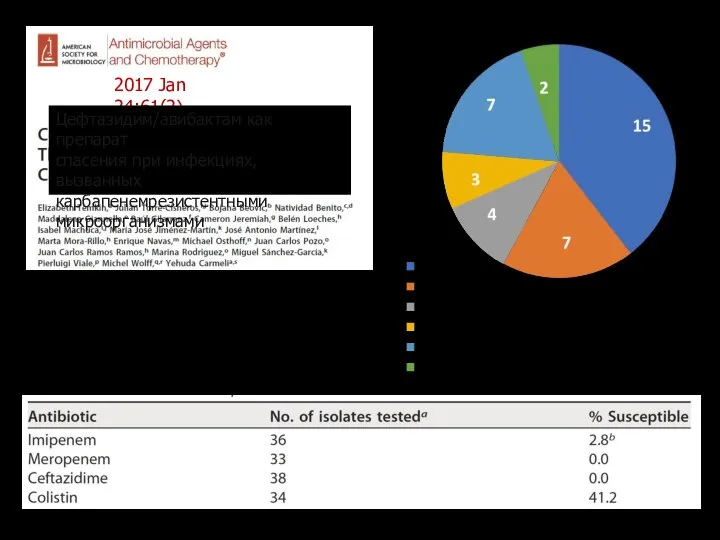
- 145. 2017 Jan 24;61(2) Цефтазидим/авибактам как препарат спасения при инфекциях, вызванных карбапенемрезистентными микроорганизмами
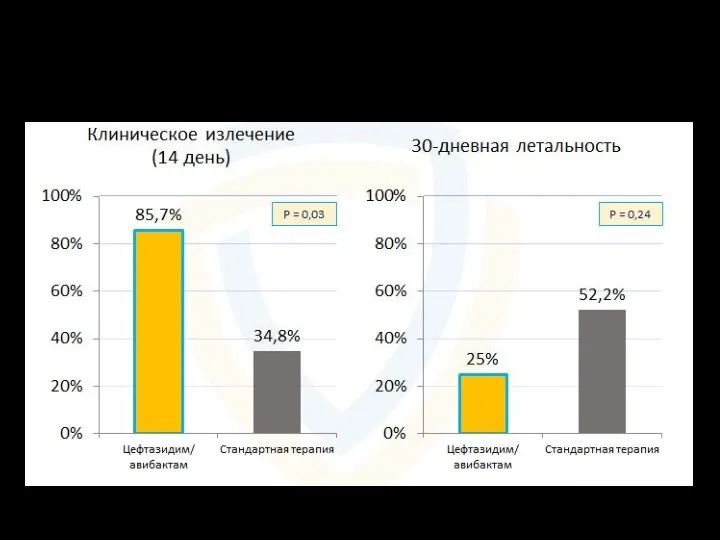
- 146. Результаты лечения получавших цефтазидим/авибактам (n=38) Клиническое излечение – 26 (68,4%) Клиническое улучшение – 6 (15,8%) Микробиологическая
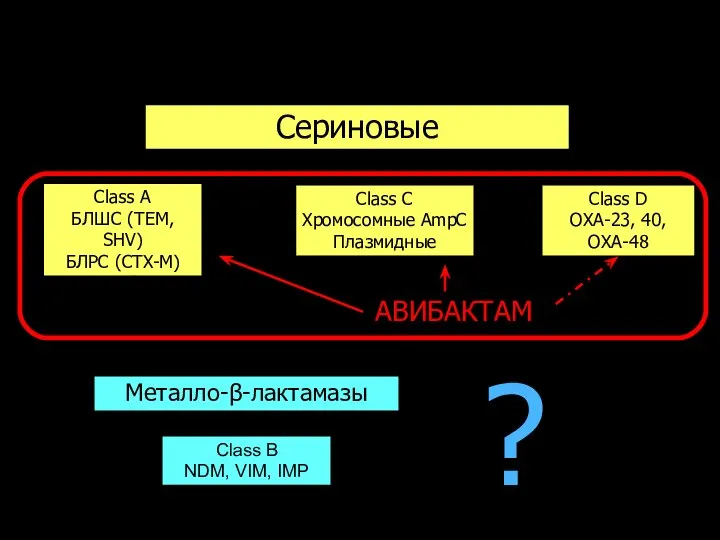
- 147. β-лактамазы Сериновые Class А БЛШС (TEM, SHV) БЛРС (CTX-M) KPC Class С Хромосомные AmpC Плазмидные Class
- 148. Бета-лактамы против бета-лактамаз
- 149. Какие антибиотики нужны в ОРИТ? Преодолевающие резистентность важнейших возбудителей С доказанной клинической эффективностью С широким спектром
- 150. Показания для назначения антимикробных препаратов в хирургии Периоперационная антибиотикопрофилактика Внебольничные инфекции Нозокомиальные инфекции
- 151. Основные направления применения антибиотиков в анестезиологии и интенсивной терапии Лечение внебольничной и нозокомиальной инфекции Профилактика Периоперционная
- 152. Новые рекомендации СКАТ как инструмент рационального применения антимикробных препаратов в стационаре и сдерживания антибиотикорезистентности XIX Российская
- 153. www.antimicrob.net Коллектив авторов – Члены Евразийского экспертного совета: Россия – 50 Азербайджан – 1 Армения –
- 154. www.antimicrob.net Список важнейших лекарств ВОЗ обновлен с новыми рекомендациями по антибиотикам Рекомендации по выбору антибиотиков при
- 155. Главные изменения, отмеченные в двух основных клинических рекомендациях Евразийские рекомендации 2016 В рекомендациях по АБТ выделять
- 156. www.antimicrob.net
- 157. Программа СКАТ при оказании стационарной медицинской помощи Клинические рекомендации Стратегическая цель Оптимизация применения АМП в стационарах
- 158. Неадекватная стартовая эмпирическая АБТ – рост летальности Использование АБП широкого спектра – рост устойчивости Оптимизация применения
- 159. Что нового в рекомендациях 2017 года? Данные о распространенности и клиническом значении нозокомиальных инфекций в стационарах
- 160. Стратификация госпитализированных пациентов по риску антибиотикорезистентности и инвазивного кандидоза Типы пациентов для выбора эмпирической терапии Тип
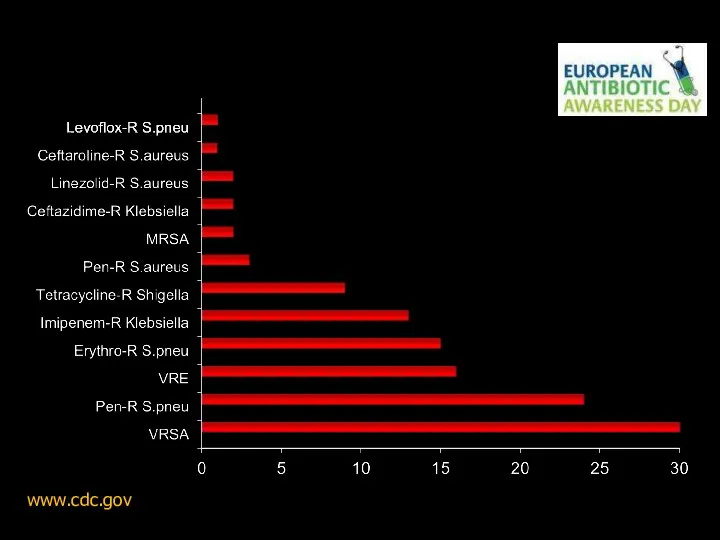
- 165. Время от начала применения антибиотика до появления резистентных штаммов Время, годы www.cdc.gov 18 ноября 2017 г.
- 168. Лечебное применение антибиотиков в интенсивной терапии Хирургический сепсис Раневой Ожоговый Ангиогенный Абдоминальный Перитонеальный Панкреатогенный Холангиогенный Интестиногенный
- 169. Микробиологическая структура нозокомиальных ангиогенных инфекций
- 170. Абсолютные показания к АБТ в хирургии Различные формы перитонита Деструктивный аппендицит Деструктивный холецистит Холангит с механической
- 171. Абсолютные показания к АБТ в хирургии Перфорация или некроз тонкой или толстой кишки различной этиологии (с
- 172. Антибактериальная профилактика/терапия при панкреонекрозе Панкреонекроз ─ абсолютное показание к СДЖКТ в сочетании с системным антибиотиком, действующим
- 174. Оптимальные режимы эмпирической антимикробной терапии нозокомиальных инфекций
- 175. Состояния, НЕ требующие длительной АБТ Острый аппендицит (без гангрены, перфорации, абсцедирования или перитонита) Острый холецистит (без
- 176. Ситуации, при которых НЕ показана антибактериальная терапия/профилактика Имплантация внутрисосудистых инфузионных катетеров Катетеризация мочевого пузыря Дренирование плевральной
- 177. Методология СДЖКТ Устранение гастроэнтерогенного источника патологической бактериальной контаминации и (ре)инфицирования Минимальное воздействие на колонизационную резистентность организма,
- 178. Селективная деконтаминация желудочно-кишечного тракта (СДЖКТ) Основная направленность метода – профилактика распространения бактерий и их токсинов из
- 179. Показания к СДЖКТ Абдоминальный сепсис при распространенном перитоните Тяжелый сепсис и полиорганная недостаточность (любой этиологии) Тяжелая
- 180. Рекомендуемые режимы СДЖКТ Аминогликозиды (тобрамицин, гентамицин) или Фторхинолоны (норфлоксацин, ципрофлоксацин, пефлоксацин) Полимиксин Амфотерицин В или Флуконазол
- 181. Эффективность СДЖКТ Влияние на частоту осложнений (2 метанализа рандомизированных исследований: D`Amico R. et al., 1998; Nathens
- 182. Эффективность СДЖКТ у пациентов с абдоминальным сепсисом Контрольная группа, n=190 Группа исследования, n=240 Снижение частоты развития
- 183. Антибактериальная профилактика/ терапия при панкреонекрозе Инфекционные осложнения развиваются у 40-70% больных Источник инфицирования ─ условнопатогенная флора
- 184. Оптимальные режимы антибиотикопрофилактики Плановые операции на толстой кишке – показана подготовка кишечника, направленная на удаление его
- 185. Принципы антибактериальной профилактики Антибиотик необходимо вводить за 30-60 мин до разреза кожи Продолжительность профилактического применения антибиотиков
- 186. Оптимальные режимы антибиотикопрофилактики «Чистые» и «условно чистые» операции - цефалоспорин I (цефазолин) или II поколения (цефуроксим)
- 188. Частота инфекционных осложнений в области операции и показания к антибиотикопрофилактике в зависимости от индекса риска
- 189. Ангиогенная инфекция у хирургических больных (blood stream infection) Инфекционные осложнения, связанные с длительной катетеризацией сосудов и
- 190. Инфекционные осложнения, связанные с имплантацией инородного тела в сердечно-сосудистую систему - «синдром инфекции инородного тела» (трансплантация
- 191. Ангиогенная инфекция у хирургических больных (blood stream infection) (продолжение) Нозокомиальный эндокардит Инфицированный флеботромбоз («Ловушка для микроорганизмов»)
- 192. Лечение ангиогенных инфекционных осложнений Устранение очага инфекции - катетера при катетерной инфекции, внутрисосудистого устройства при неконтролируемом
- 193. Трудности лечения НИ Больные с НИ – самые тяжелые пациенты стационара (APACHE II>15, ожидаемая летальность >25-50%)
- 194. Показания для назначения комбинированной терапии крайне тяжелые инфекции, тяжелый сепсис и септический шок, когда необходимо срочно
- 195. Показания к комбинированной АБТ в абдоминальной хирургии Полимикробная этиология патологического процесса Распространенный перитонит Тяжелый сепсис и
- 196. Преимущества антимикробной монотерапии уменьшение риска непрогнозируемого антагонизма антибиотиков; снижение риска взаимодействия с другими лекарственными препаратами; уменьшение
- 197. Возможности монотерапии в абдоминальной хирургии Карбапенемы Цефалоспорины IV поколения Защищенные цефалоспорины III (цефоперазон/сульбактам) Фторхинолоны (пефлоксацин, левофлоксацин,
- 198. Средства, непригодные для эмпирической терапии внутрибрюшной инфекции Цефалоспорины I и II поколения Пенициллин Антистафилококковые пенициллины Ампициллин
- 199. Критерии достаточности АБТ Снижение температуры до нормальных или субнормальных цифр (не менее двух суток) Стойкий регресс
- 200. Длительность АБТ При неосложненных формах внутрибрюшной инфекции длительность АБТ не превышает 5 - 7 дней Длительная
- 201. Ошибки АБТ хирургической инфекции “Слепое” назначение повторных длительных курсов антибиотиков с их периодической заменой пациентам с
- 202. Ошибки АБТ хирургической инфекции Необоснованное увеличение продолжительности АБТ опасность развития резистентности (особенно при длительном применении субоптимальных
- 203. Ошибки АБТ хирургической инфекции Необоснованное применение препаратов резерва в качестве эмпирического режима Использование заведомо низких концентраций
- 204. Деэскалация – максимально широкий спектр АМТ на старте с возможным переходом на целенаправленную терапию на основании
- 205. Госпитальный формуляр антибиотиков Необходимо строгое обоснование при назначении: Препаратов с широчайшим спектром (имипенем/циластатин) – риск роста
- 206. Формуляр антимикробных препаратов * - есть таблетированные формы Защищенные аминопенициллины* Цефалоспорины I-IV поколений Цефаперазон/ сульбактам Карбапенемы
- 207. Циклическая ротация антибиотиков Определение Периодическая замена режимов стартовой эмпирической терапии инфекций в ОРИТ Обоснование Восстановление активности
- 208. Кандидоз Candida spp. занимают IV место среди возбудителей нозокомиальной инфекции в ОИТ По данным NNIS (США)
- 209. Кандидоз Системный кандидоз сопровождается высокой летальностью Летальность при кандидемии составляет 25-60% Летальность при кандидозном сепсисе с
- 210. Инфекционные осложнения в абдоминальной хирургии Частота развития после плановых операций - 6% после экстренных операций -
- 211. Факторы, способствующие увеличению частоты грибковой нозокомиальной инфекции Использование антибиотиков широкого спектра Применение эффективных методов химиотерапии Усиленное
- 213. Кандидозная инфекция при панкреонекрозе Инвазивный кандидоз – 37% Развитие кандидоза – в 4 раза увеличивает летальность
- 214. Системные резервуары грибков рода кандида
- 215. Патогенез системного кандидоза Гипотензия Ишемия Нарушение питания и метаболизма Стероиды Циклоспорин Избыточное размножение Candida spp. в
- 216. Патогенез системного кандидоза Эндогенное инфицирование (особенно Candida albicans) Экзогенное инфицирование (передача от других больных или персонала)
- 217. Кандидозная инфекция у хирургических больных Колонизация Candida – выделение Сandida spp. из любого биологического материала (кроме
- 218. Кандидозная инфекция у хирургических больных Интраабдоминальный кандидоз включает интраабдоминальные абсцессы или перитонит, вызванный Candida spp. Интраабдоминальный
- 219. Клинические и лабораторные признаки инвазивного кандидоза Гипертермия (сохраняющаяся, несмотря на применение антибактериальной терапии) Гистологические признаки грибковой
- 220. Клинические и лабораторные признаки инвазивного кандидоза Многофокусная колонизация Candida (в различных анатомических зонах) у больных, имеющих
- 222. Кандидозный эндофтальмит
- 223. Диссеминированный кандидоз
- 224. Диссеминированный кандидоз Язвенные поражения тонкой кишки, вызванные Candida albicans
- 225. Диссеминированный кандидоз Поражение почек Candida
- 226. Направления антимикотической терапии Профилактическая терапия «Упреждающая» терапия Эмпирическая терапия Целенаправленная терапия
- 227. Профилактическая антимикотическая терапия Показания Больные в ОИТ при наличии 3 факторов риска Определенные категории: перитонит панкреатит
- 228. «Упреждающая» антимикотическая терапия Показания Патологическая колонизация: выделение Candida из 2 или более фокусов Цель Профилактика инвазивной
- 229. Эмпирическая антимикотическая терапия Показания сепсис и ПОН обоснованные подозрения в отношении микоза Цель снижение летальности Целенаправленная
- 230. Флюконазол (дифлюкан, Pfizer) Высокая активность в отношении большинства Candida spp. В/в и пероральная формы Биодоступность после
- 231. Лекарственные формы Дифлюкана Внутрь капсулы Внутривенно капельно раствор
- 233. Фармакокинетический профиль Дифлюкан Высокая биодоступность – 90% Быстрое, независимое от приёма пищи всасывание Элиминация через почки
- 234. Фармакокинетический профиль Дифлюкан Хорошее проникновение в ткани и жидкости: слюна мокрота ликвор перитонеальная жидкость моча ткани
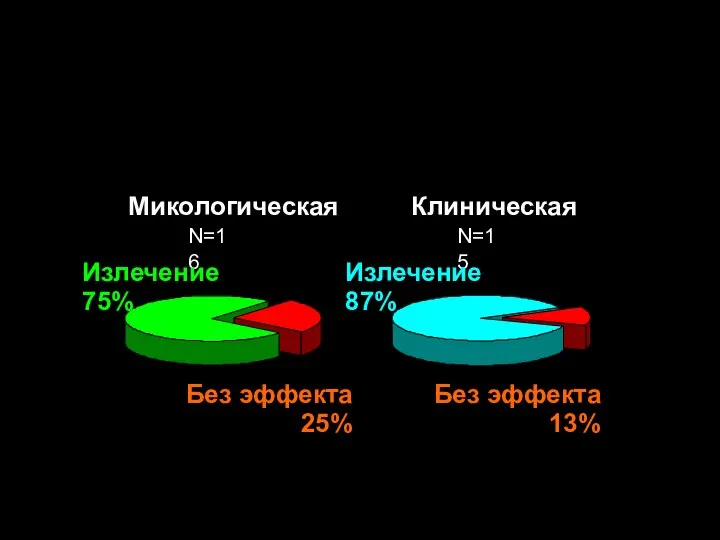
- 235. Микологическая Клиническая N=16 N=15 Излечение 75% Излечение 87% Без эффекта 25% Без эффекта 13% Эффективность Дифлюканапри
- 236. Амфотерицин В Активное полиеновое антифунгальное средство Токсичность: лихорадка, тошнота, рвота, гипотензия, нефротоксичность (снижается при применении пентоксифиллина).
- 237. Инвазивный кандидоз у хирургических больных Риск развития резистентности и колонизации C. non-albicans (krusei, glabrata) вследствие профилактики
- 238. Профилактика инвазивного кандидоза у хирургических больных Эффективная тактика (доказательства II уровня; 2 RCT) Флуконазол предотвращает развитие
- 239. Профилактика инвазивного кандидоза Эффективность Флуконазол 400 мг/сутки (Pelz R.K. et al., Ann. Surg. 2001. 233:542-548) Хирургические
- 241. Режими селективной деконтаминации желудочно-кишечного тракта
- 242. Показания к профилактическому (упреждающему) назначению антимикотических средств (флуконазол) Панкреонекроз и оперативные вмешательства на поджелудочной железе Перфорация
- 243. “Всякий, кто пьет это средство, выздоравливает, ...исключая тех, кому оно не помогает, и они умирают.... Поэтому
- 244. Профилактика флуконазолом у хирургических больных в критических состояниях Мета-анализ (2005 г.) 4 RCT n=626 Дозы флуконазола:
- 245. Инвазивные Грибковые Инфекции
- 246. Возрастание Актуальности Инвазивных Грибковых Инфекций: Аспергиллез Частота существенно возросла Рост числа иммуноскомпрометированных пациентов Рост числа инвазивных
- 247. Возрастание Актуальности Инвазивных Грибковых Инфекций: Кандидоз Серьезные грибковые инфекции – подъем роста Инвазивные Candida инфекции На
- 248. C. glabrata 16% C. albicans 54% C. parapsilosis 15% C. tropicalis 8% C. krusei 2% other
- 249. National Epidemiology of Mycosis Survey (NEMIS) was a prospective, multicenter study conducted at 6 US sites
- 251. Механизм Действия Существующих Противогрибковых Препаратов
- 252. Механизм Действия: Амфотерицин B Связывается со стеролом - эргостеролом клеточной мембраны гриба, в результате чего изменяется
- 253. Механизм Действия: Азолы Являются ингибиторами CYP450 3A- зависимой С 14-α-деметилазы гриба, в результате чего происходит Истощение
- 254. Новый Механизм Действия: Каспофунгин Каспофунгин – первый представитель нового класса антимикотиков – ингибиторов синтеза глюкана (эхинокандинов)
- 255. Новый Механизм Действия: Каспофунгин β (1,3)-D-глюкан жизненно необходим для целостности клеточной стенки многих грибов, включая Aspergillus
- 256. Мишени Воздействия Некоторых Антимикотиков Адаптировано из Andriole VT J Antimicrob Chemother 1999;44:151–162; Graybill JR et al
- 257. Механизмы Действия Существующих Препаратов – Взаимосвязь с Эффективностью Адаптировано из Andriole VT J Antimicrob Chemother 1999;44:151–162;
- 258. Механизмы действия существующих антимикотиков и их влияние на переносимость Амфотерицин В активно действует на клетки как
- 259. Активность каспофунгина In Vitro
- 260. Каспофунгин: спектр активности in vitro в отношении Aspergillus spp. Высокая активность in vitro в отношении многих
- 262. Скачать презентацию
































































































































































































































 Бронхоэктатическая болезнь у детей
Бронхоэктатическая болезнь у детей Балалардағы артериальды гипертензияның клиникалық белгілері
Балалардағы артериальды гипертензияның клиникалық белгілері Аноректальные пороки
Аноректальные пороки Массаж при сколиозе. Выбор приёмов в зависимости от тонуса мышц пациента
Массаж при сколиозе. Выбор приёмов в зависимости от тонуса мышц пациента Аюрведа: 5 шагов к здоровью. 1 день
Аюрведа: 5 шагов к здоровью. 1 день Маниакально-депрессивный психоз (биполярное аффективное расстройство)
Маниакально-депрессивный психоз (биполярное аффективное расстройство) Денсаулықпен байланысты өмір сапасы
Денсаулықпен байланысты өмір сапасы Гестозы. Классификация
Гестозы. Классификация Нормирование труда в здравоохранении
Нормирование труда в здравоохранении Le bloc opératoire
Le bloc opératoire Острый лейкоз
Острый лейкоз Частная психология
Частная психология Лечение экзо- и эндоцервицитов, ассоциированных с неспецифической микстинфекцией нижнего отдела гениталий у женщин
Лечение экзо- и эндоцервицитов, ассоциированных с неспецифической микстинфекцией нижнего отдела гениталий у женщин Эмбриологические аспекты программы ЭКО
Эмбриологические аспекты программы ЭКО Аптечка доврачебной помощи
Аптечка доврачебной помощи Алкоголизм и его влияние на развитие здоровой личности
Алкоголизм и его влияние на развитие здоровой личности Выявление факторов, влияющих на ожирение
Выявление факторов, влияющих на ожирение Медики в годы Великой Отечественной войны
Медики в годы Великой Отечественной войны Неотложные состояния в педиатрии
Неотложные состояния в педиатрии Защитно-приспособительные реакции при гипоксии
Защитно-приспособительные реакции при гипоксии Врачебная тактика при острой лихорадке неясного происхождения
Врачебная тактика при острой лихорадке неясного происхождения Этиопатогенез зубочелюстных аномалий
Этиопатогенез зубочелюстных аномалий Алыптасу кезеңіндегі (бозбалалық, бойжеткендік) негізгі проблемалар және оның шешу жолдары
Алыптасу кезеңіндегі (бозбалалық, бойжеткендік) негізгі проблемалар және оның шешу жолдары Кровотечения на фоне менопаузальной гормональной терапии (МГТ)
Кровотечения на фоне менопаузальной гормональной терапии (МГТ) Предмет, задачи и методы патологии. Понятие о болезни
Предмет, задачи и методы патологии. Понятие о болезни Безопасная беременность
Безопасная беременность Гипертоническая болезнь
Гипертоническая болезнь Сестринский уход при физиологической беременности
Сестринский уход при физиологической беременности