Содержание
- 2. ПАЦИЕНТКА, 57 ЛЕТ( 1964 ГР.) Клинический случай Основной/Клинический диагноз: С 56. Рак яичников рТ3сN0М0, IIIС стадия
- 3. ПАЦИЕНТКА, 57 ЛЕТ В феврале 2020г. по поводу увеличения живота в объеме обследовалась по месту жительства.
- 4. ПАЦИЕНТКА, 57 ЛЕТ с 07.04.2020г. по 30.07.2020г. 6 курсов неоадъювантной химиотерапии по схеме: паклитаксел 175 мг
- 5. ПАЦИЕНТКА, 57 ЛЕТ 10-11.2020г: 2 курса адъювантной химиотерапии по схеме: паклитаксел 175 мг / м2 в
- 6. ПАЦИЕНТКА, 57 ЛЕТ Решением консилиума от 23.12.2020г: пациентке рекомендовано лечение препаратом Линпарза® (олапариб) по 400 мг
- 7. Вопрос №1 Какие нежелательные явления чаше ожидаются при приеме олапариба? 1. тошнота/рвота, усталость, анемия. 2. полинейропатии,
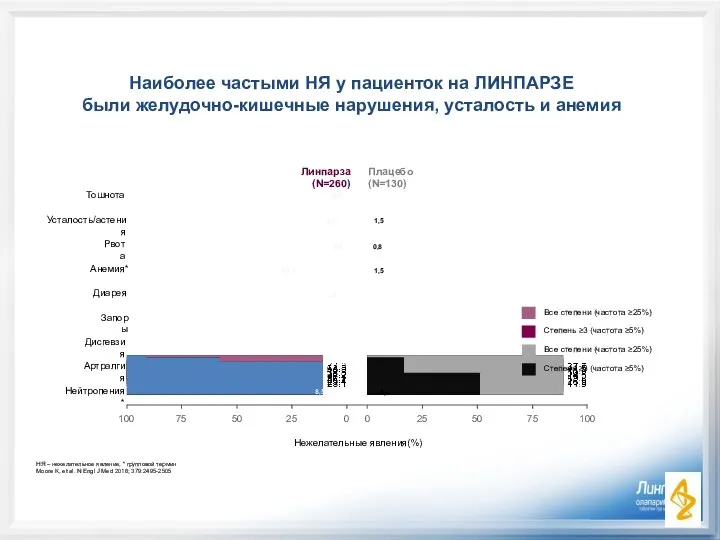
- 8. Наиболее частыми НЯ у пациенток на ЛИНПАРЗЕ были желудочно-кишечные нарушения, усталость и анемия Линпарза (N=260) Плацебо
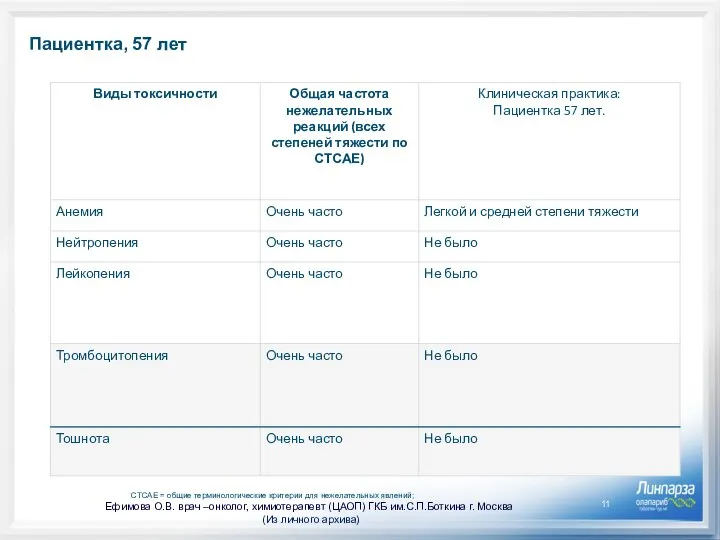
- 9. ПАЦИЕНТКА, 57 ЛЕТ Нежелательные явления: Первые 3 месяца лечение переносила с гематологической токсичностью в виде анемии
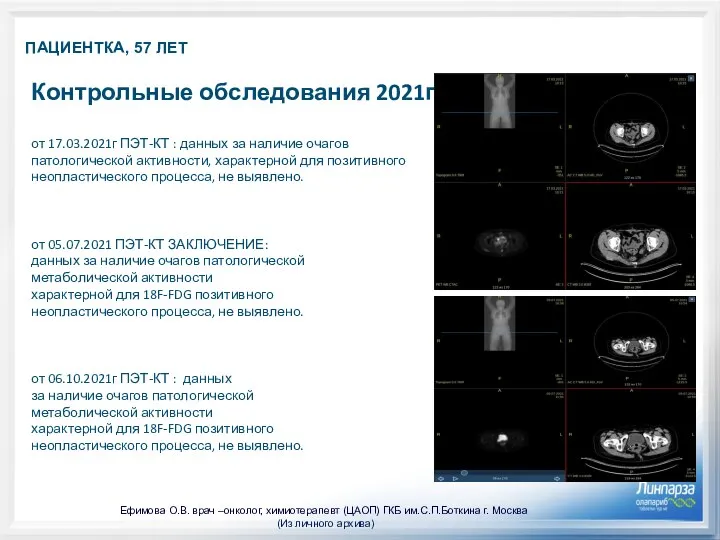
- 10. ПАЦИЕНТКА, 57 ЛЕТ Контрольные обследования 2021год: от 17.03.2021г ПЭТ-КТ : данных за наличие очагов патологической активности,
- 11. Пациентка, 57 лет Ефимова О.В. врач –онколог, химиотерапевт (ЦАОП) ГКБ им.С.П.Боткина г. Москва (Из личного архива)
- 12. Выводы по клиническому случаю Пациентка, 41 год Ефимова О.В. врач –онколог, химиотерапевт (ЦАОП1) ГКБ им.С.П.Боткина г.
- 13. Вопрос №2 Насколько в % снижается риск прогрессирования или смерти при приеме Линпарзы в 1-ой линии
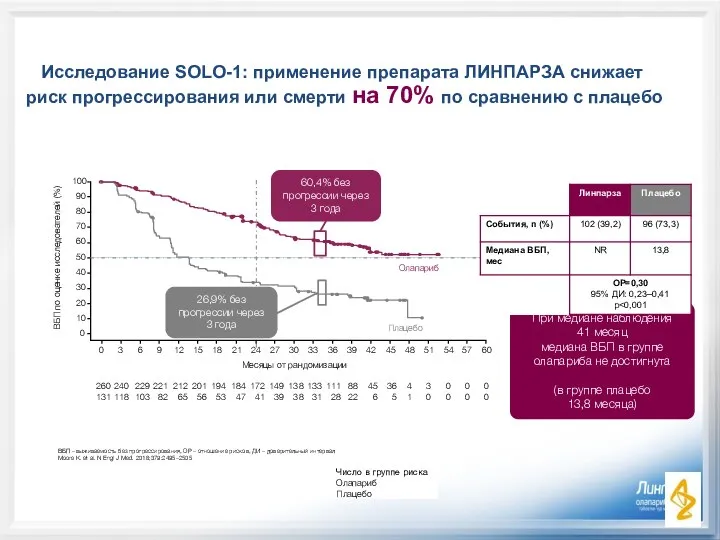
- 14. Исследование SOLO-1: применение препарата ЛИНПАРЗА снижает риск прогрессирования или смерти на 70% по сравнению с плацебо
- 16. Скачать презентацию









 Диуретики. Проблема - задержка жидкости
Диуретики. Проблема - задержка жидкости Сложная ортопедическая обувь. Алгоритм действий врача КОАП ОРТЕКА
Сложная ортопедическая обувь. Алгоритм действий врача КОАП ОРТЕКА The treatment of rheumatic endocarditis
The treatment of rheumatic endocarditis Синдромы, связанные с аномалиями в системе аутосом
Синдромы, связанные с аномалиями в системе аутосом Туберкулезная волчанка
Туберкулезная волчанка Кандиломатоз перианальной области
Кандиломатоз перианальной области Амбулаторная кардиореабилитация
Амбулаторная кардиореабилитация Резидуальная шизофрения
Резидуальная шизофрения Фармакотерапия в сестринской практике. Применение лекарственных средств
Фармакотерапия в сестринской практике. Применение лекарственных средств Заболевания щитовидной железы и беременность
Заболевания щитовидной железы и беременность Қант диабеті(ҚД) ІІ типі қосарланған созылмалы жүрек жетіспеушілгі (СЖЖ) бар науқастарға стандартты емнің әсері
Қант диабеті(ҚД) ІІ типі қосарланған созылмалы жүрек жетіспеушілгі (СЖЖ) бар науқастарға стандартты емнің әсері Стан ліпідного обміну
Стан ліпідного обміну Болезни почек и мочевого пузыря
Болезни почек и мочевого пузыря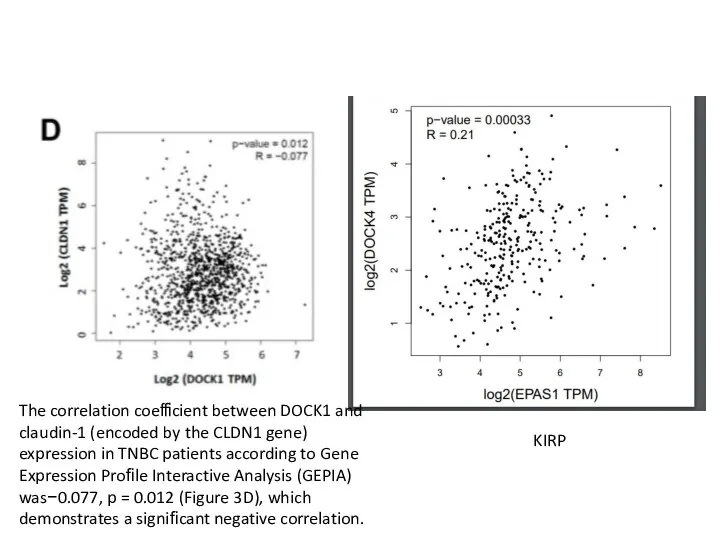 The correlation coe cient between DOCK1 and claudin-1 (encoded by the CLDN1 gene)
The correlation coe cient between DOCK1 and claudin-1 (encoded by the CLDN1 gene) Школа здоровья для беременных. Как себя вести
Школа здоровья для беременных. Как себя вести Бруцелла. Бруцеллез. Микробиология
Бруцелла. Бруцеллез. Микробиология Стрептококк
Стрептококк Меры социальной поддержки медицинских работников Липецкой области
Меры социальной поддержки медицинских работников Липецкой области Термическая травма. Ожоги
Термическая травма. Ожоги Заманауи фармакотерапиядағы дәлелді медицинаның рөлі. Мәселелік дәрілерге түсінік
Заманауи фармакотерапиядағы дәлелді медицинаның рөлі. Мәселелік дәрілерге түсінік Травмы. Виды травм
Травмы. Виды травм Натуральное жаропонижающее Флю стоп+
Натуральное жаропонижающее Флю стоп+ Эпидемиологическая характеристика сальмонеллезов в России
Эпидемиологическая характеристика сальмонеллезов в России Влияние радиационного фона на здоровье человека
Влияние радиационного фона на здоровье человека Биопсия при проведении УЗИ
Биопсия при проведении УЗИ Асептические и дезинфицирующие средства
Асептические и дезинфицирующие средства Медицина катастроф. Понятия и определения
Медицина катастроф. Понятия и определения Антибиотикотерапия
Антибиотикотерапия