Содержание
- 2. * Основоположники иммунологии В области иммунологии работали и работают многие тысячи учёных. Мы называем лишь пять
- 3. Основоположники иммунологии ЛУИ ПАСТЕР (1822 – 1895) Рядом блестящих экс-периментов показал, что различными воздействи-ями можно ослабить
- 4. Основоположники иммунологии РОБЕРТ КОХ (1843 – 1910) Внёс огромный вклад в микробиологию и им-мунологию. Применил иммерсионный
- 5. Основоположники иммунологии ИЛЬЯ ИЛЬИЧ МЕЧНИКОВ (1845 – 1916) Основоположник срав-нительно-эволюционного метода в биологии и эво-люционной теории
- 6. Основоположники иммунологии ПАУЛЬ ЭРЛИХ (1854 – 1915) Основоположник хи-миотерапии. Синтези-ровал первый химио-терапевтический пре-парат для лечения си-филиса
- 7. * ОПРЕДЕЛЕНИЕ ПОНЯТИЙ (по Р.В.Петрову) Антигены - это вещества, несущие признаки генетически чужеродной для организма инфор-мации,
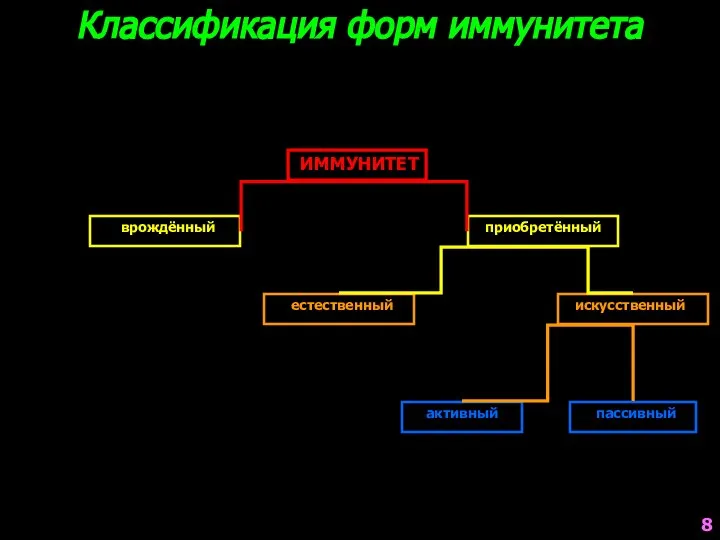
- 8. Классификация форм иммунитета ИММУНИТЕТ естественный искусственный активный пассивный врождённый приобретённый 8
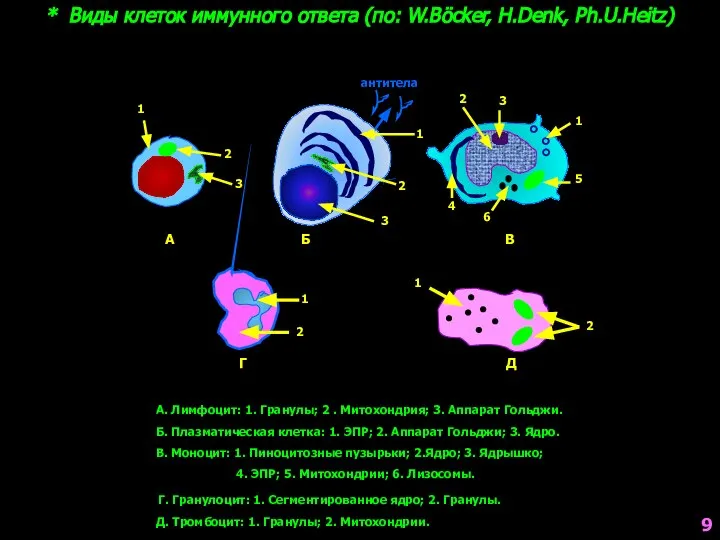
- 9. * Виды клеток иммунного ответа (по: W.Böcker, H.Denk, Ph.U.Heitz) А. Лимфоцит: 1. Гранулы; 2 . Митохондрия;
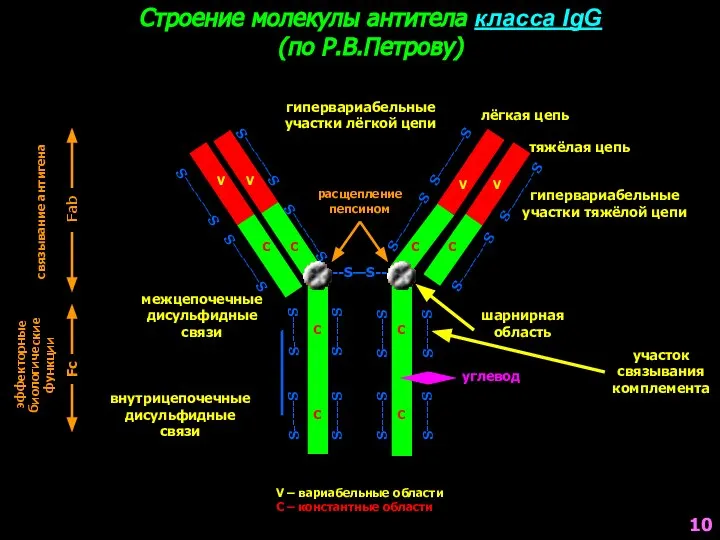
- 10. Строение молекулы антитела класса IgG (по Р.В.Петрову) --S—S-- S--------S S--------S S-----S S-----S S--------S S--------S S--------S S--------S
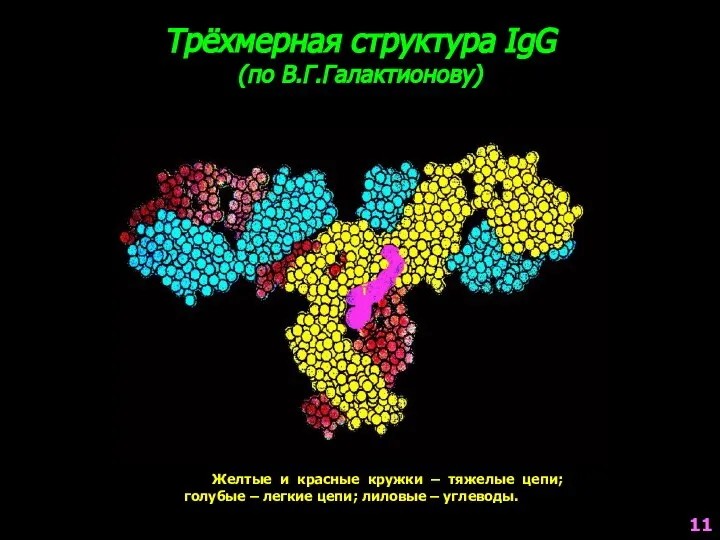
- 11. Трёхмерная структура IgG (по В.Г.Галактионову) Желтые и красные кружки – тяжелые цепи; голубые – легкие цепи;
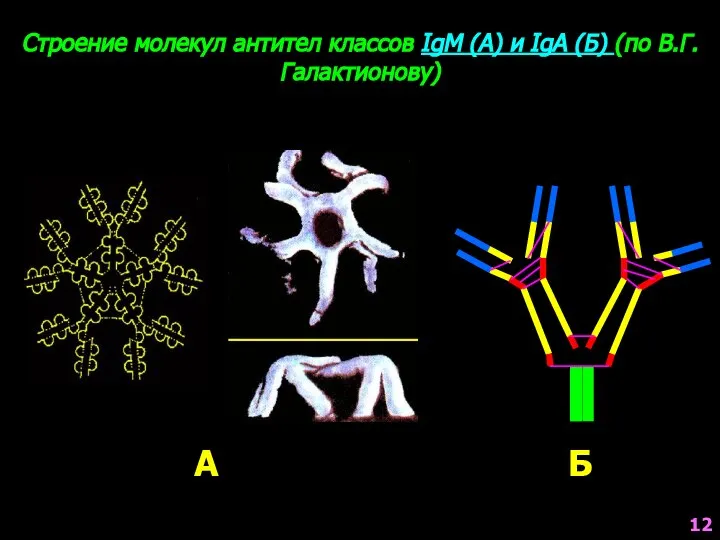
- 12. Строение молекул антител классов IgM (А) и IgA (Б) (по В.Г.Галактионову) А Б 12
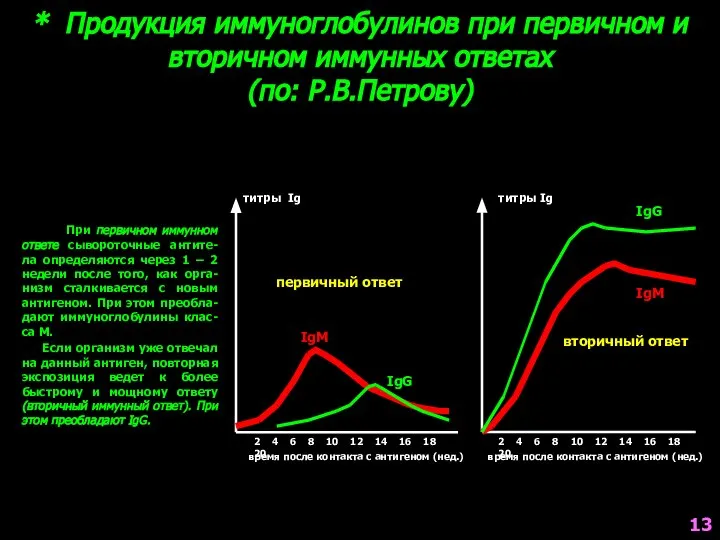
- 13. * Продукция иммуноглобулинов при первичном и вторичном иммунных ответах (по: Р.В.Петрову) При первичном иммунном ответе сывороточные
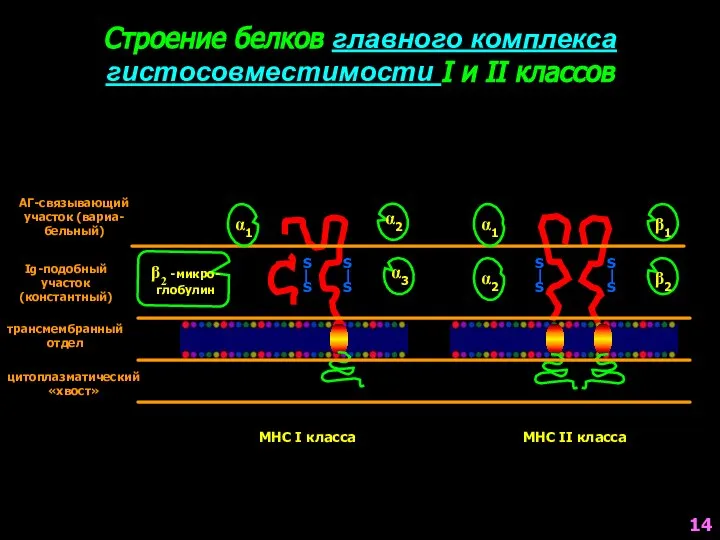
- 14. Строение белков главного комплекса гистосовместимости I и II классов S S S S S S S
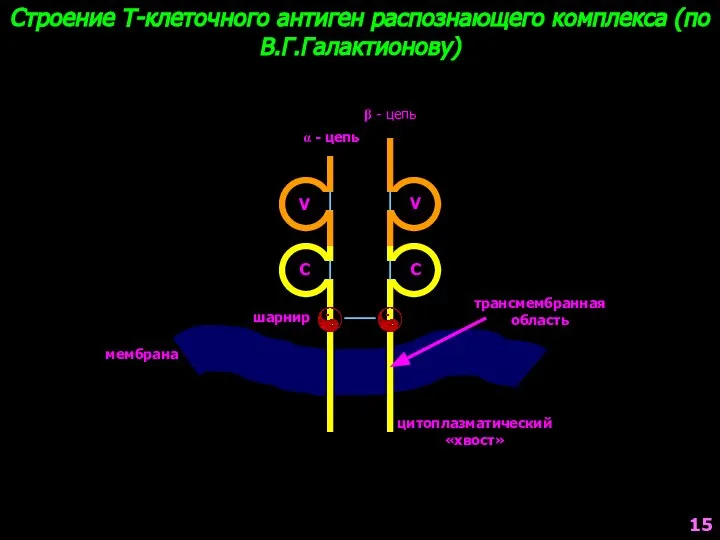
- 15. Строение Т-клеточного антиген распознающего комплекса (по В.Г.Галактионову) α - цепь β - цепь V V C
- 16. А АПК – антиген-презентирующая клетка (макрофаг) А – процессированный антиген МНС I/II – главный комплекс гистосовместимости
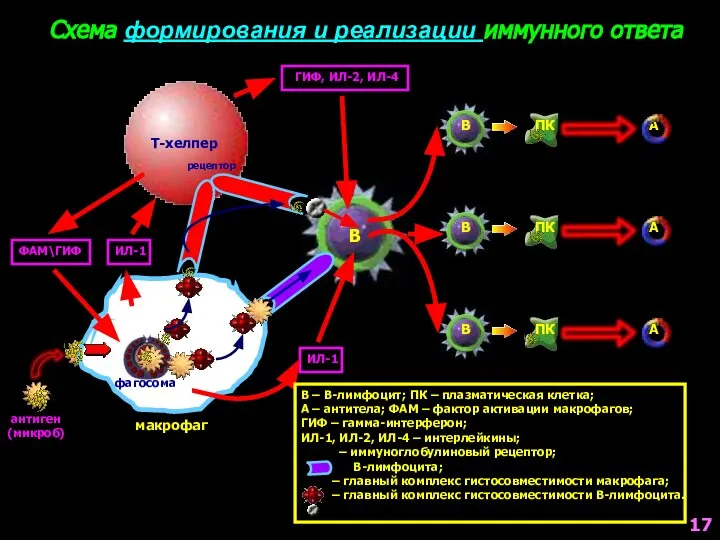
- 17. Схема формирования и реализации иммунного ответа В В В В ПК ПК ПК А А А
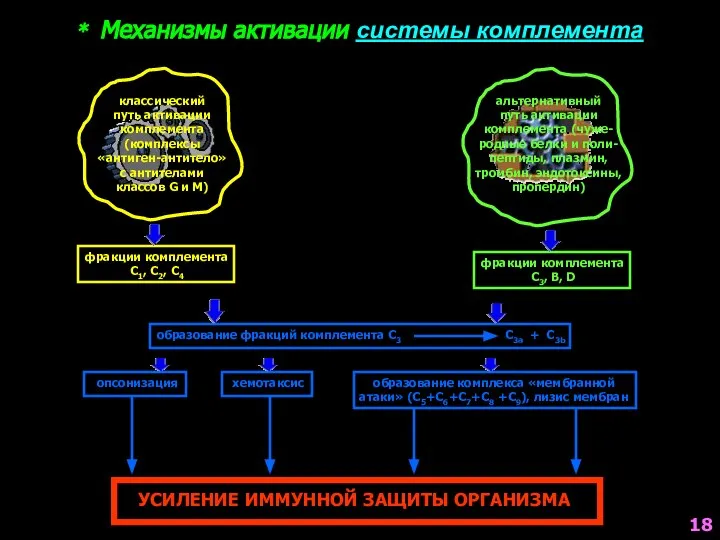
- 18. * Механизмы активации системы комплемента альтернативный путь активации комплемента (чуже- родные белки и поли- пептиды, плазмин,
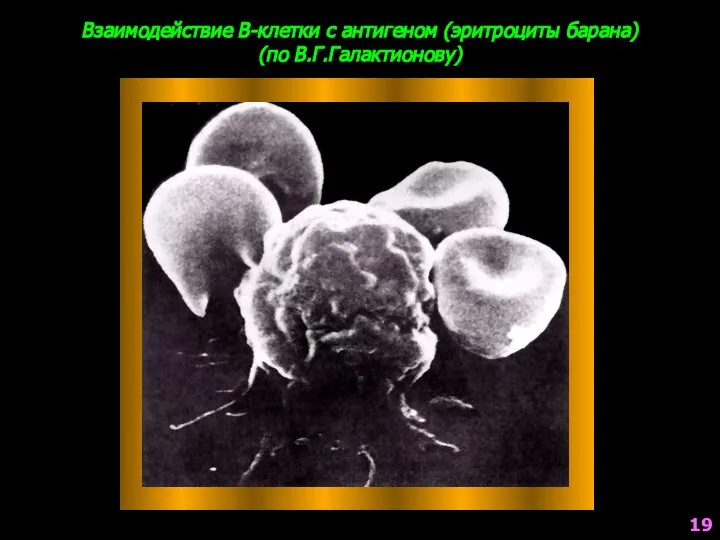
- 19. Взаимодействие В-клетки с антигеном (эритроциты барана) (по В.Г.Галактионову) 19
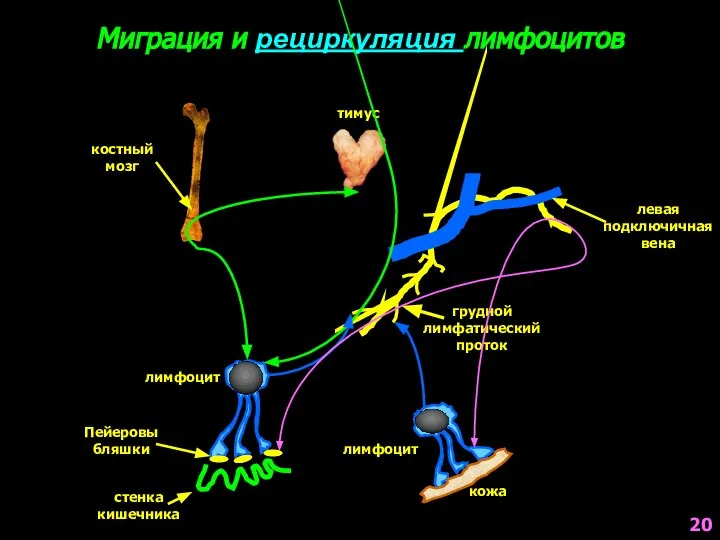
- 20. Миграция и рециркуляция лимфоцитов костный мозг тимус лимфоцит Пейеровы бляшки стенка кишечника лимфоцит кожа левая подключичная
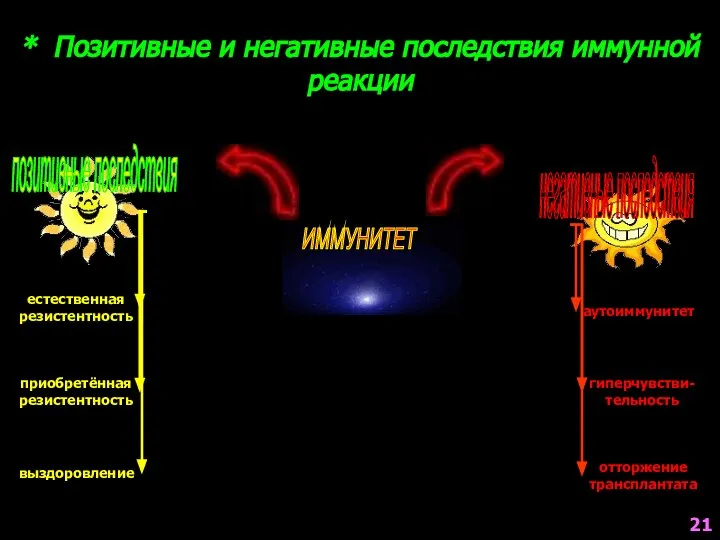
- 21. * Позитивные и негативные последствия иммунной реакции ИММУНИТЕТ позитивные последствия негативные последствия естественная резистентность приобретённая резистентность
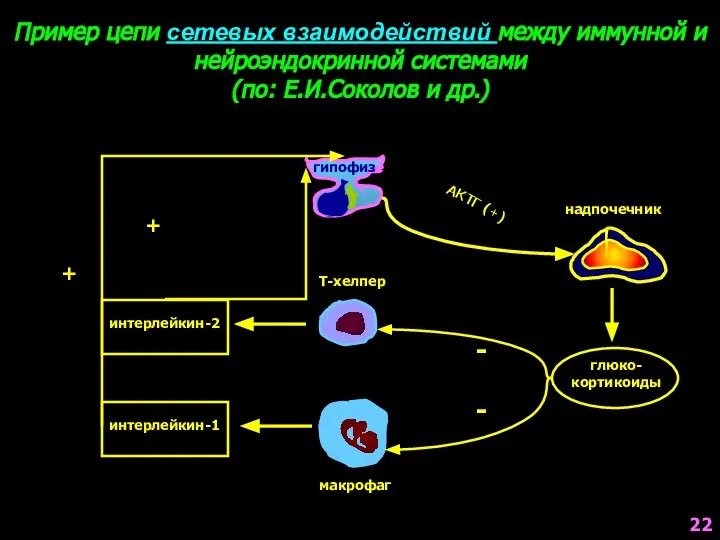
- 22. Пример цепи сетевых взаимодействий между иммунной и нейроэндокринной системами (по: Е.И.Соколов и др.) гипофиз надпочечник Т-хелпер
- 23. Главными проблемами трансплантационного иммунитета являются РХПТ и РТПХ. РХПТ – «реакция: хозяин против трансплантата», заключающаяся в
- 24. Великие трансплантологи Владимир Петрович Демихов 1916 - 1998 Кристиан Барнард 1922 - 2001 В 1946 году
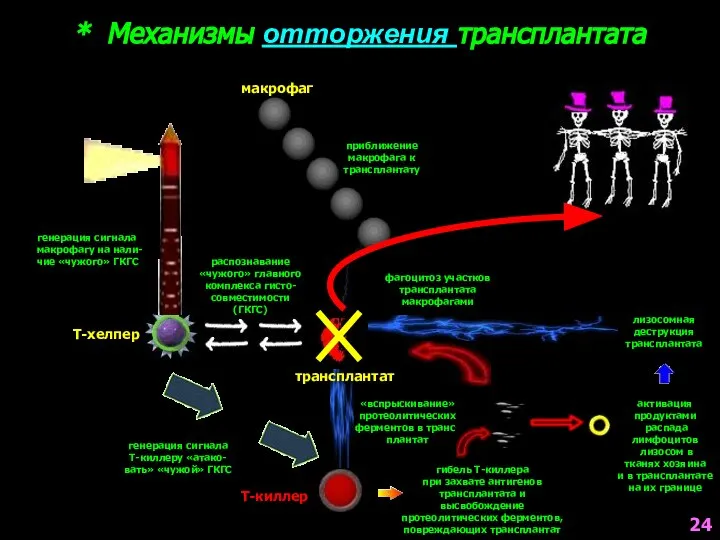
- 25. * Механизмы отторжения трансплантата Т-хелпер распознавание «чужого» главного комплекса гисто- совместимости (ГКГС) макрофаг генерация сигнала макрофагу
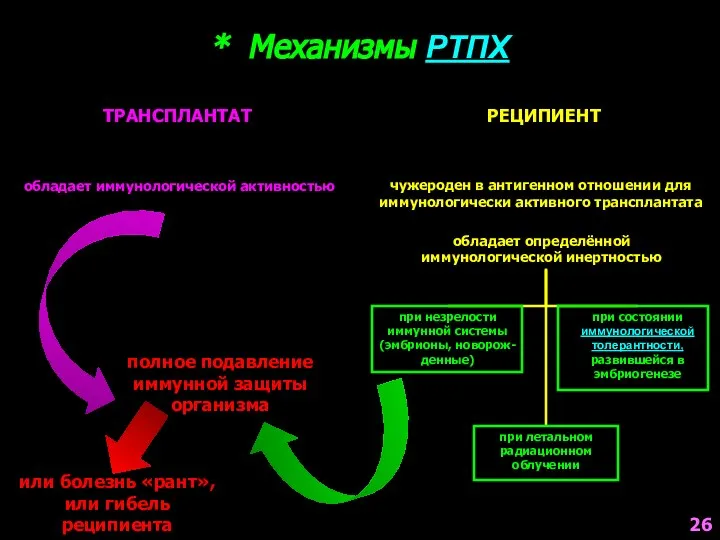
- 26. * Механизмы РТПХ ТРАНСПЛАНТАТ РЕЦИПИЕНТ обладает иммунологической активностью чужероден в антигенном отношении для иммунологически активного трансплантата
- 27. Иммунодефицитные состояния Иммунодефицитные состояния (иммунодефици-ты) – это, в основном, генетически обусловленные дефекты системы иммунитета, ведущие к
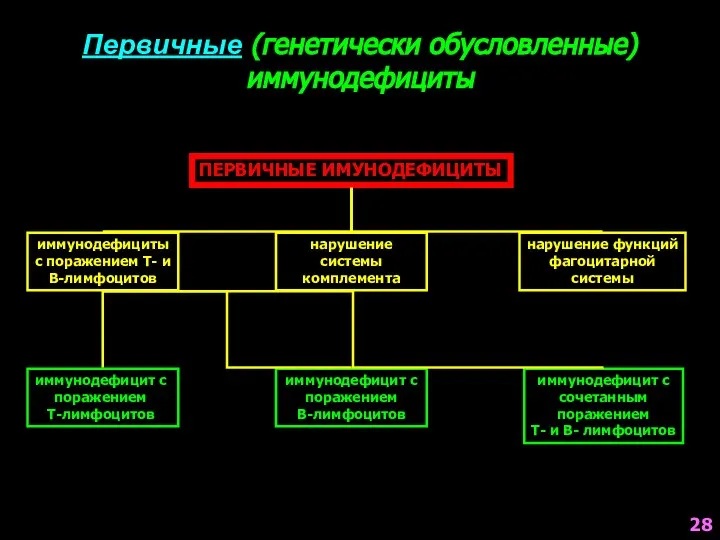
- 28. Первичные (генетически обусловленные) иммунодефициты ПЕРВИЧНЫЕ ИМУНОДЕФИЦИТЫ иммунодефициты с поражением Т- и В-лимфоцитов нарушение системы комплемента нарушение
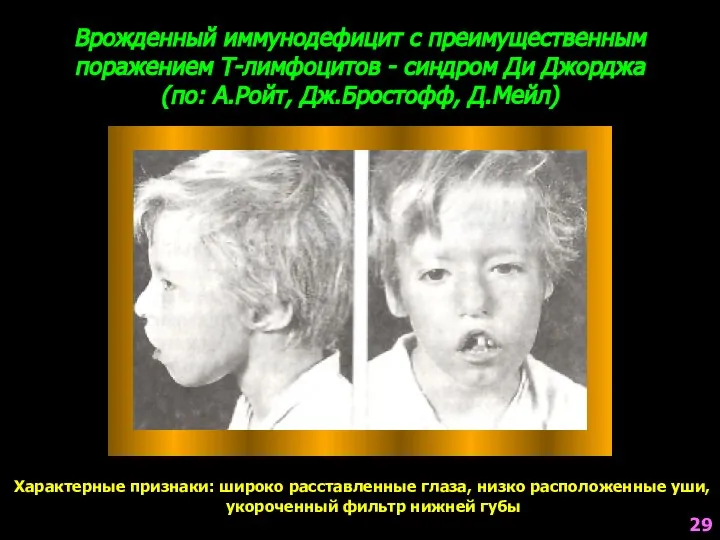
- 29. Врожденный иммунодефицит с преимущественным поражением Т-лимфоцитов - синдром Ди Джорджа (по: А.Ройт, Дж.Бростофф, Д.Мейл) Характерные признаки:
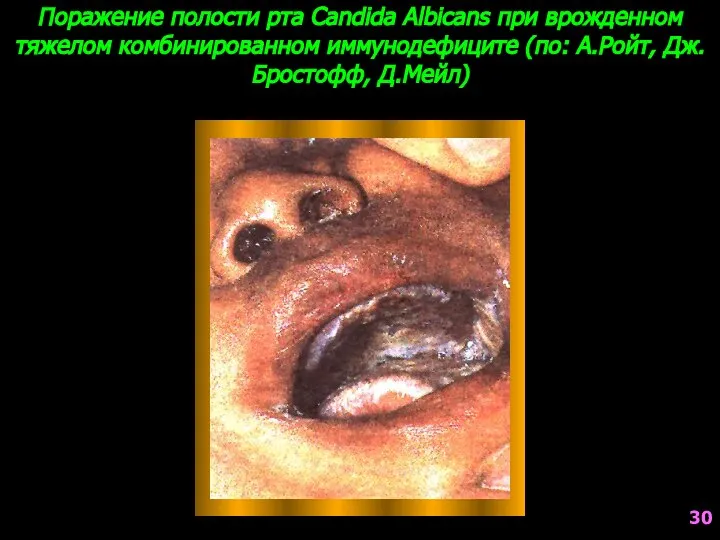
- 30. Поражение полости рта Candida Albicans при врожденном тяжелом комбинированном иммунодефиците (по: А.Ройт, Дж.Бростофф, Д.Мейл) 30
- 31. Синдром приобретенного иммунодефицита СПИД Возбудителем СПИДа является ретровирус, назван-ный вирусом иммунодефицита человека (ВИЧ), ассо-циированный с лимфоаденопатией
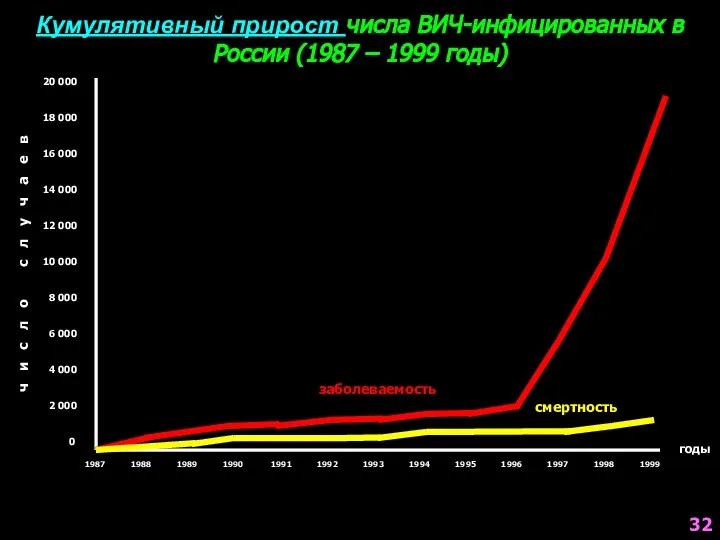
- 32. Кумулятивный прирост числа ВИЧ-инфицированных в России (1987 – 1999 годы) 20 000 18 000 16 000
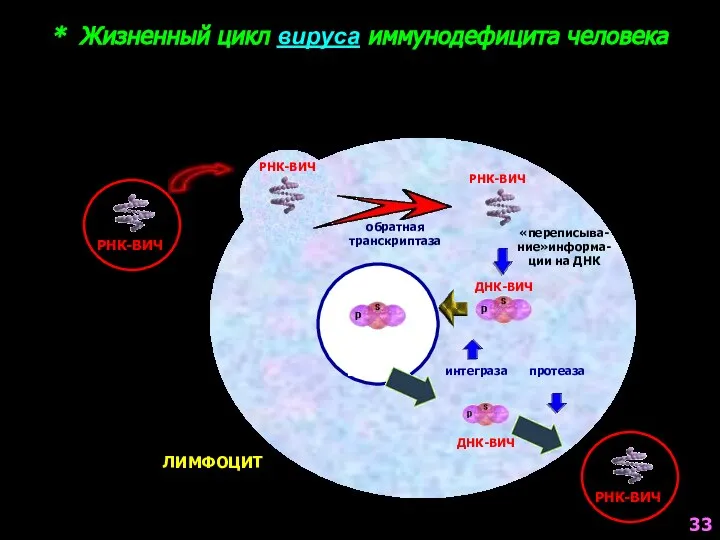
- 33. * Жизненный цикл вируса иммунодефицита человека РНК-ВИЧ обратная транскриптаза РНК-ВИЧ ЛИМФОЦИТ РНК-ВИЧ ДНК ДНК-ВИЧ «переписыва- ние»информа-
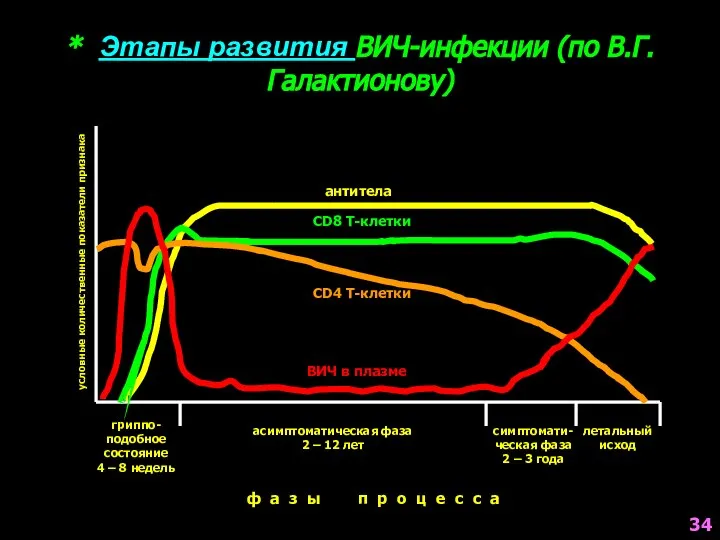
- 34. * Этапы развития ВИЧ-инфекции (по В.Г.Галактионову) условные количественные показатели признака гриппо- подобное состояние 4 – 8
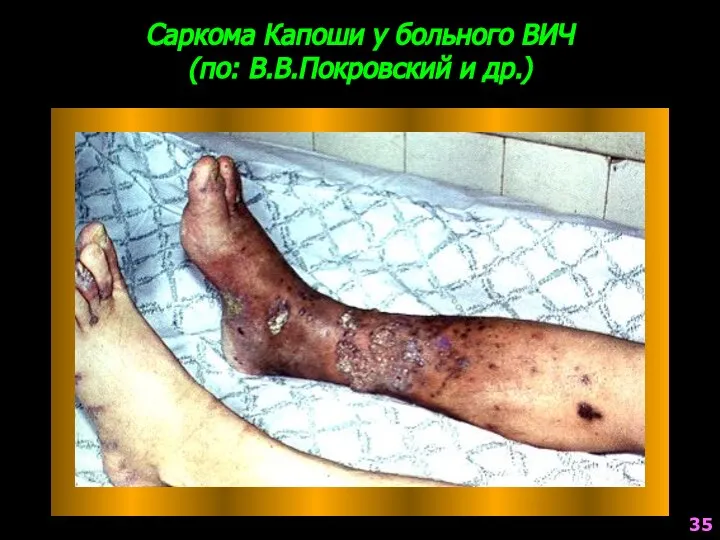
- 35. Саркома Капоши у больного ВИЧ (по: В.В.Покровский и др.) 35
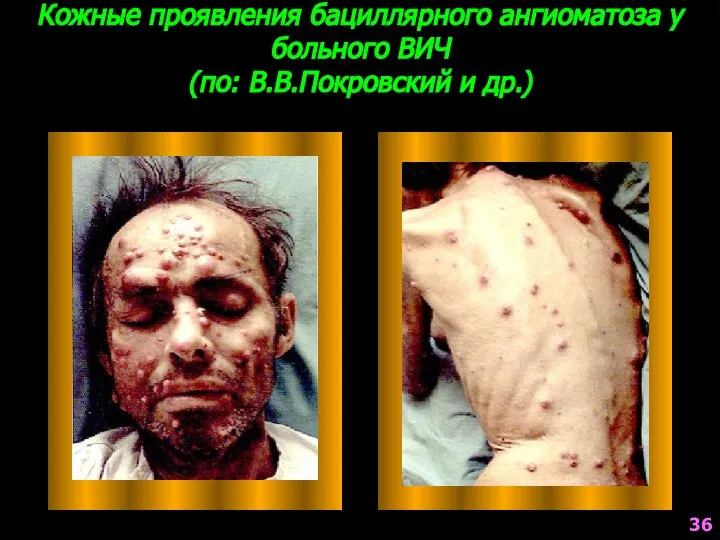
- 36. Кожные проявления бациллярного ангиоматоза у больного ВИЧ (по: В.В.Покровский и др.) 36
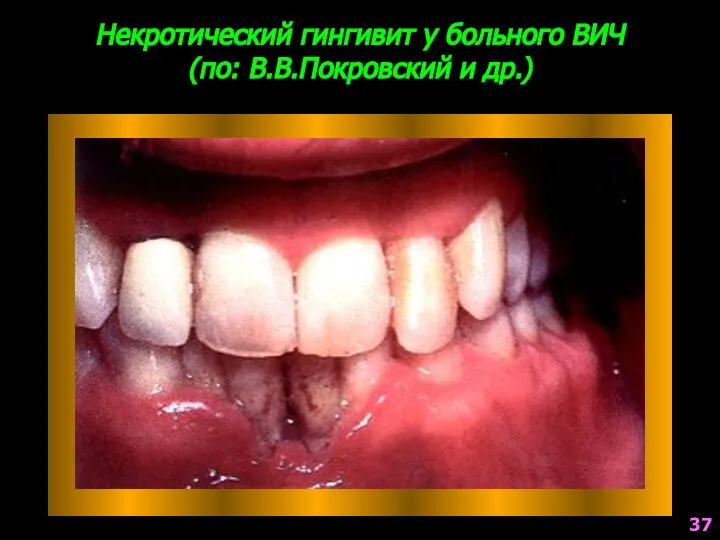
- 37. Некротический гингивит у больного ВИЧ (по: В.В.Покровский и др.) 37
- 39. Скачать презентацию











 Эпилепсия. Психические расстройства, обусловленные повреждением головного мозга. Умственная отсталость
Эпилепсия. Психические расстройства, обусловленные повреждением головного мозга. Умственная отсталость Психологическое сопровождение суицидентов - оценка суицидального риска в условиях психиатрического стационара
Психологическое сопровождение суицидентов - оценка суицидального риска в условиях психиатрического стационара Медицинские карты
Медицинские карты Острый аппендицит. Панкреатит
Острый аппендицит. Панкреатит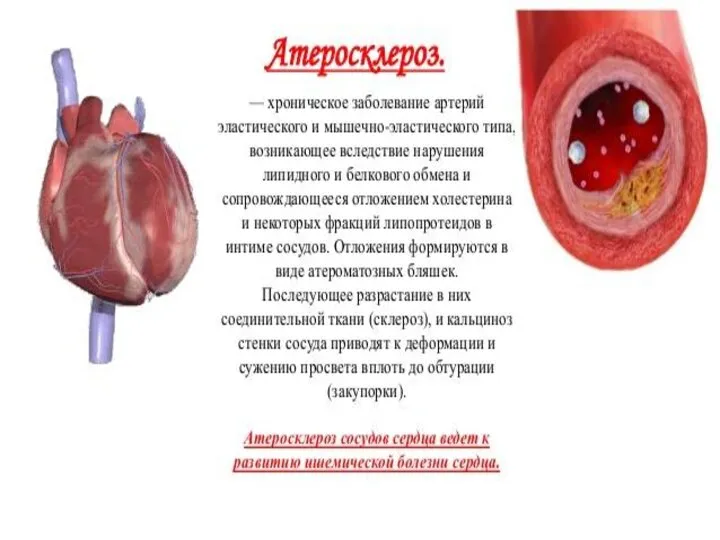 Атеросклероз. Факторы риска
Атеросклероз. Факторы риска Entamoeba Histolytica
Entamoeba Histolytica Шаблон презентации - 2022 врачи
Шаблон презентации - 2022 врачи Синдром Ангельмана. Синдром счастливой куклы
Синдром Ангельмана. Синдром счастливой куклы Воспалительные заболевания органов малого таза. Препараты с противовоспалительным и антиишемическим действием
Воспалительные заболевания органов малого таза. Препараты с противовоспалительным и антиишемическим действием Физиотерапевтические и иные процедуры в санаторно-курортном лечении
Физиотерапевтические и иные процедуры в санаторно-курортном лечении مسعف في كل بيت
مسعف في كل بيت Формы дислалии, критерии их выделения
Формы дислалии, критерии их выделения Ветряная оспа у детей
Ветряная оспа у детей Лучевая семиотика при заболеваниях зубочелюстной системы. 2 часть
Лучевая семиотика при заболеваниях зубочелюстной системы. 2 часть Свойства санитайзеров
Свойства санитайзеров Соединительная, костная и зубные ткани. Дентин
Соединительная, костная и зубные ткани. Дентин А-В блокада второй степени
А-В блокада второй степени Медициналық мекемелер 2 ге бөлінеді. Амбулаториялық. Статционарлық
Медициналық мекемелер 2 ге бөлінеді. Амбулаториялық. Статционарлық Використання ялин, сосен та хвої після новорічних свят
Використання ялин, сосен та хвої після новорічних свят Синдром Марфана
Синдром Марфана Инфекционные заболевания
Инфекционные заболевания Дислипидемия у детей с синдромом системной воспалительной реакции
Дислипидемия у детей с синдромом системной воспалительной реакции Центр народной медицины Республики Тыва. Опыт работы
Центр народной медицины Республики Тыва. Опыт работы Наркотические анальгетики
Наркотические анальгетики 15 минут о прирученных вирусах
15 минут о прирученных вирусах Изоантигенная несовместимость крови матери и плода
Изоантигенная несовместимость крови матери и плода Научная деятельность И.П. Павлова
Научная деятельность И.П. Павлова Диета больных сахарным диабетом
Диета больных сахарным диабетом