Слайд 2
приказом Министерства здравоохранения РФ от 26 октября 2015 г. №751н
"Об утверждении

правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность"
Слайд 3Основные положения.
Лекарственные средства и лекарственные вещества, независимо от источника их поступления, подвергаются

приемочному контролю в соответствии с требованиями приказа.
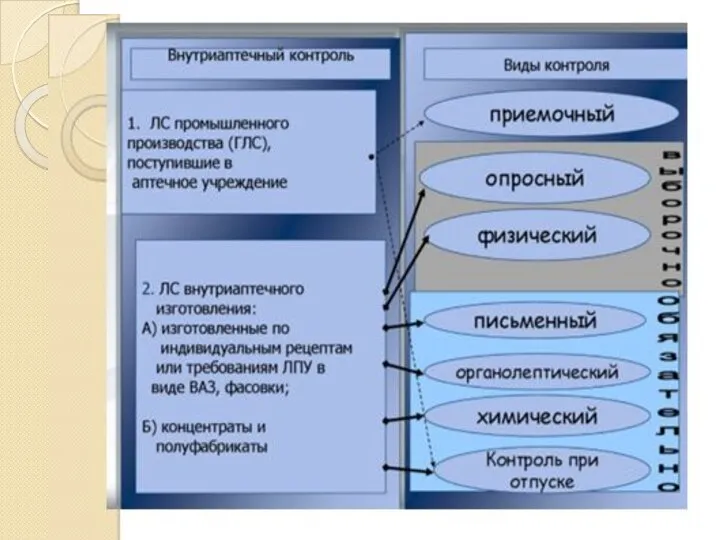
Все лекарственные средства, изготовленные в аптеках (в том числе гомеопатических) по индивидуальным рецептам или требованиям лечебных организаций, в виде внутриаптечной заготовки, фасовки, а также концентраты и полуфабрикаты подвергаются внутриаптечному контролю: письменному, органолептическому и контролю при отпуске - обязательно;
опросному и физическому - выборочно;
химическому - в соответствии с требованиями приказа.
Слайд 6Провизору, назначенному на должность для выполнения контроля качества лекарственных средств, изготовляемых в

аптеках (далее "провизор-аналитик"), необходимо владеть всеми видами внутриаптечного контроля.
Руководителю аптеки и его заместителям следует обеспечить условия выполнения всех видов контроля.
Провизору-аналитику, впервые назначенному на должность, необходимо пройти курс стажировки в территориальной контрольно-аналитической лаборатории.
Слайд 8Для проведения химического контроля качества лекарственных средств, изготовляемых в аптеках, должно быть

оборудовано специальное рабочее место, оснащенное типовым набором оборудования, приборами и реактивами, а также обеспечено нормативными документами, справочной литературой.
Слайд 9Результаты контроля качества лекарственных средств регистрируются в журналах.
Все журналы должны быть прошнурованы,

страницы в них пронумерованы, заверены подписью руководителя и печатью аптеки.
Срок хранения журналов - один год.
Отчет о работе по контролю качества лекарственных средств, изготовленных в аптеке, составляется по итогам за год и направляется в территориальную контрольно-аналитическую лабораторию по определенной форме.
Слайд 19Письменный контроль
При изготовлении лекарственных форм по рецептам и требованиям лечебных организаций

заполняются паспорта письменного контроля.
В паспорте должны быть указаны:
дата изготовления, номер рецепта (номер лечебной организации, название отделения), наименование взятых лекарственных веществ и их количества, число доз, подписи изготовившего, расфасовавшего и проверившего лекарственную форму.
В случае изготовления лекарственной формы практикантом ставится подпись лица, ответственного за производственную практику.








































 Типы кожи. Тест по косметологии
Типы кожи. Тест по косметологии Онкогенез, этапы канцерогенеза. Антиканцерогенные механизмы
Онкогенез, этапы канцерогенеза. Антиканцерогенные механизмы В ГБУЗ Ставропольская ЦРБ проводится вакцинация от COVID-19, г. Тольятти
В ГБУЗ Ставропольская ЦРБ проводится вакцинация от COVID-19, г. Тольятти Нормальная рентгенанатомия легких
Нормальная рентгенанатомия легких Желчекаменная болезнь
Желчекаменная болезнь Заболевания органов зрения
Заболевания органов зрения Гомеостаз. Состав, свойства и функции крови. Группы крови, резус-фактор
Гомеостаз. Состав, свойства и функции крови. Группы крови, резус-фактор Студенческое научное общество Будущий Московский хирург
Студенческое научное общество Будущий Московский хирург Фитотерапия
Фитотерапия Терапевтическая практика в Медицинском университете Харбина
Терапевтическая практика в Медицинском университете Харбина Современное представление о физиологии лимфотока и методы его изучения
Современное представление о физиологии лимфотока и методы его изучения Что делать в условиях пандемии коронавируса?
Что делать в условиях пандемии коронавируса? Физическая реабилитация при посттравматическом артрите у спортсменов пауэрлифтеров
Физическая реабилитация при посттравматическом артрите у спортсменов пауэрлифтеров Gynekologinen irtosolututkimus
Gynekologinen irtosolututkimus Экспертиза временной нетрудоспособности при заболеваниях внутренних органов
Экспертиза временной нетрудоспособности при заболеваниях внутренних органов Понятие об эпидемическом процессе Часть 1
Понятие об эпидемическом процессе Часть 1 Медициналық қызметтерді көрсету, дәрілік заттар, медициналық мақсаттағы бұйымдар
Медициналық қызметтерді көрсету, дәрілік заттар, медициналық мақсаттағы бұйымдар Синдром повреждения и беременность
Синдром повреждения и беременность топ аан нижней конечности
топ аан нижней конечности Микробиологическая-диагностика эшерихиозов
Микробиологическая-диагностика эшерихиозов Коронавирус – пандемия сегодняшнего дня
Коронавирус – пандемия сегодняшнего дня Опухоли пищевода
Опухоли пищевода Психопатия. Диагностические критерии
Психопатия. Диагностические критерии Таз с анатомической и акушерской точек зрения
Таз с анатомической и акушерской точек зрения Из чего сделаны наши девчонки?! Женщина-загадка
Из чего сделаны наши девчонки?! Женщина-загадка Потокзависимая вазодилатация
Потокзависимая вазодилатация Омаров
Омаров Санаторий Сосны в Республике Беларусь
Санаторий Сосны в Республике Беларусь