в світі1
Феринжект® добре вивчений в
рандомізованих клінічних дослідженнях2-28
Широкий досвід застосування у пацієнтів1
29
8 663
> 12 мільйонів
Спонсорованих компанією, опублікованих рандомізованих інтервенційних клінічних досліджень1-28
Пацієнта отримували Феринжект® в цих 29 дослідженнях1-28
Пацієнто-років застосування
з моменту запуску1
22. Hussain I, et al. Anemia 2013;2013:169107
23. Ponikowski P et al. Eur Heart J 2015;36:657–68
24. Van Veldhuisen DJ et al. Circulation 2017;136:1374–83
25. Seid MH, et al. Anemia 2017;2017:9642027
26. Breymann C et al. Arch Gynecol Obstet 2017;296(6):1229–34
27. Trenkwalder C et al. Movement Disorders 2017;32(10):1478–82
28. Boomershine CS et al. Rheumatol Ther. 2018;5:271-281
1. Vifor Pharma DOF. June 2020
2. Geisser P, Banké-Bochita J. Arzneim Forsch 2010;60(6a):362–72
3. Evstatiev R et al. Clin Gastroenterol Hepatol 2013;11:269–77
4. Evstatiev R et al. Gastroenterology 2011;141:846–53
5. Onken JE et al. Nephrol Dial Transplant 2013;0:1–12
6. Onken JE et al. Transfusion 2014;54:306–15
7. Breymann C et al. Int J Gynecol Obstet 2008;101:67–73
8. Favrat B et al. PLoS ONE 2014;9(4):e94217
9. Qunibi WY et al. Nephrol Dial Transplant 2011;26:1599–1607
10. Seid MH et al. Am J Obstet Gynecol 2008;199:435.e1–435.e7
11. Van Wyck DB et al. Transfusion 2009;49:2719–28
12. Van Wyck DB et al. Obstet Gynecol 2007;110:267–78
13. Anker SD et al. NEJM 2009;361:2436–48
14. Bailie GR. Arzneim Forsch 2010;60(6a):386–98
15. Charytan C et al. Nephrol Dial Transplant 2013;28:953–64
16. Hedenus M et al. Med Oncol 2014;31:302
17. Macdougall IC et al. Nephrol Dial Transplant 2014;0:1–10
18. Kulnigg S et al. Am J Gastroenterol 2008;103:1182–92
19. Kulnigg-Dabsch S et al. In!amm Bowel Dis 2013;19:1609–16
20. Allen RP et al. Sleep Med 2011;12(9):906–13
21. Barish CF, et al. Anemia 2012;2012:172104








 Тромбоэмболия легочной артерий. Классификация и постановка диагноза
Тромбоэмболия легочной артерий. Классификация и постановка диагноза Репродуктивные органы
Репродуктивные органы Организация первой помощи при занятиях спортом
Организация первой помощи при занятиях спортом Вирусные диареи
Вирусные диареи Симптомы и синдромы при заболеваниях желудка. Хронический гастрит, язва желудка и 12-перстной кишки
Симптомы и синдромы при заболеваниях желудка. Хронический гастрит, язва желудка и 12-перстной кишки Когнитивные расстройства.Реабилитация
Когнитивные расстройства.Реабилитация ОСНОВЫ ЛОГОПЕДИИ база
ОСНОВЫ ЛОГОПЕДИИ база Способы иммобилизации и переноски пострадавшего
Способы иммобилизации и переноски пострадавшего Онкогенез, этапы канцерогенеза. Антиканцерогенные механизмы
Онкогенез, этапы канцерогенеза. Антиканцерогенные механизмы Термическая травма. Ожоги
Термическая травма. Ожоги Ящур
Ящур Сахарный диабет кошек
Сахарный диабет кошек Патофизиология ФАП
Патофизиология ФАП КУРСОР. Конференция для обмена научными данными и клиническим опытом
КУРСОР. Конференция для обмена научными данными и клиническим опытом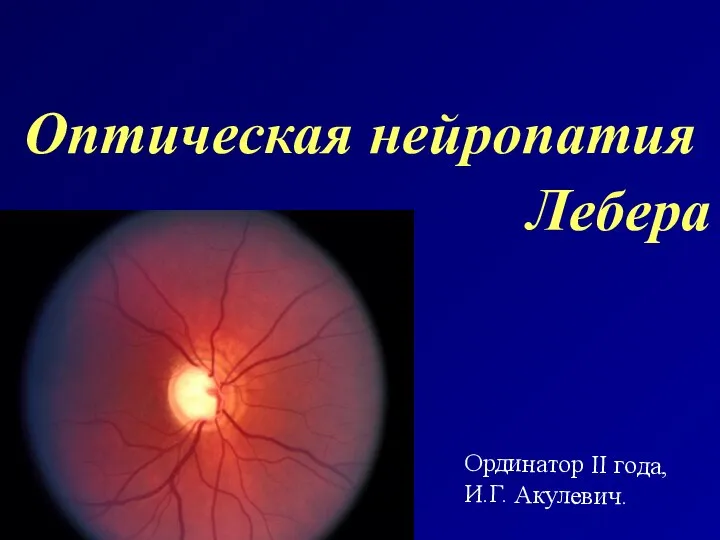 Оптическая нейропатия Лебера
Оптическая нейропатия Лебера Экспресс-тестирование совместимости крови донора и реципиента
Экспресс-тестирование совместимости крови донора и реципиента Роль альфафетопротеина и УЗИскрининга в постановке диагноза в гастроэнтерологии. Методы диагностики и лечения
Роль альфафетопротеина и УЗИскрининга в постановке диагноза в гастроэнтерологии. Методы диагностики и лечения Узлы в хирургии
Узлы в хирургии Микробиологическая диагностика коклюша и паракоклюша
Микробиологическая диагностика коклюша и паракоклюша Спирты. Алкоголь и потомство
Спирты. Алкоголь и потомство Индивидуальная и клубная работа с получателями услуг
Индивидуальная и клубная работа с получателями услуг Медицинская аптечка первой помощи
Медицинская аптечка первой помощи Фармация – дорога в жизнь
Фармация – дорога в жизнь Анатомия и МР-семиотика структур коленного сустава
Анатомия и МР-семиотика структур коленного сустава Правда о биосимилярах
Правда о биосимилярах Применение имплантируемых регистраторов ритма сердца у больных с синкопальными состояниями неясной этиологии
Применение имплантируемых регистраторов ритма сердца у больных с синкопальными состояниями неясной этиологии Гипонатриемия физической нагрузки
Гипонатриемия физической нагрузки Хельсинкская декларация
Хельсинкская декларация