Содержание
- 2. ЛЕКАРСТВЕННЫЕ СРЕДСТВА Оригинальные Инновационные Брендовые Воспроизведенные Дженерики Генерики Биоаналоги Копии и т.д.
- 3. «Оригинальный» или «инновационный» ЛП (бренд) Ранее неизвестный и впервые выпущенный на рынок фирмой-разработчиком лекарственный препарат, прошедший
- 4. Воспроизведеныый препарат или дженерик (от англ. generic – родовой) Непатентованный лекарственный препарат, являющийся воспроизведением оригинального препарата,
- 5. Права больных В 2004 году ВОЗ приняла резолюцию, провозгласившую приоритетной задачей увеличение безопасности лечения. Этим решением
- 6. Права больных Информированное согласие предполагает, в том числе, право пациента знать какие препараты (оригинальные или воспроизведенные)
- 7. Приказ Минздрава России от 20 декабря 2012 года N 1175н "Об утверждении порядка назначения и выписывания
- 8. Доля дженериков в объеме лекарственных препаратов на фармацевтическом рынке Россия 61-90 % Франция – 50 %
- 9. Рынок дженериков в России Некоторые оригинальные препараты имеют огромное количество дженериков: Более 100 дженериков нифедипина 120
- 10. Дженерики в РФ низкого качества Субстанции из мало доступных для контроля стран (Китай, Индия) Поставки через
- 11. Влияние дженериков низкого качества на здоровье популяции Резистентность бактерий, вирусов и грибов к антимикробным препаратам Хронизация
- 12. Влияние дженериков низкого качества на здоровье популяции Австралия, 2003 г.: 250 000 побочных эффектов ЛС 50
- 13. Опасность лечения некачественными ЛП Вероятность несчастного случая вследствие авиакатастрофы - 1:3 000 000 Вследствие лечения -
- 14. Как отличить дженерики от оригинальных препаратов В России отсутствуют источники информации, позволяющие идентифицировать дженерики, присутствующие на
- 15. R & D компании Bayer GlaxoSmithKline Pfizer MSD Sanofi-Aventis Bristol-Myers Squibb Novartis Schering-Plough Abbott Novo Nordisk
- 16. Стоимость оригинальных препаратов Стоимость оригинальных препаратов значительно выше, чем дженериков. Фирмы-разработчики формируют более высокие цены на
- 17. Стоимость оригинальных препаратов На создание оригинального препарата требуется от 800 млн. до 1,5 млрд. долларов Только
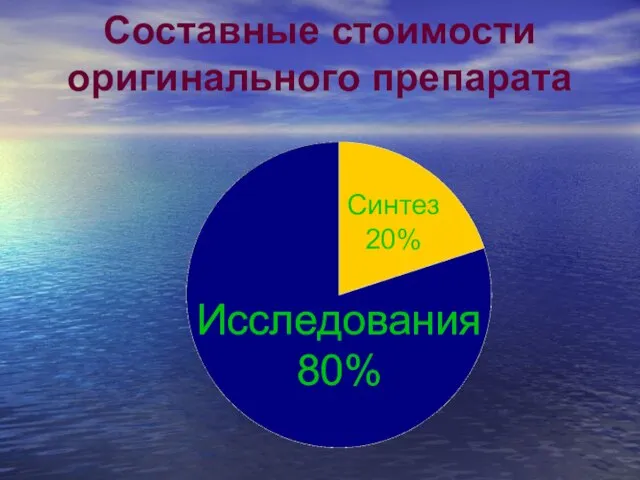
- 18. Составные стоимости оригинального препарата Исследования 80% Синтез 20%
- 19. Стоимость дженериков При производстве дженериков 50 % стоимости составляет активная субстанция Для снижения цены конечного продукта
- 20. Оригинальные препараты От синтеза нового лекарственного вещества до срока окончания действия патента проходит в среднем 35-40
- 21. Оригинальные препараты Первый этап – доклинические исследования (фармакологические, аналитические, фармакокинетические, биофармацевтические, технологические и др.) Второй этап
- 22. Оригинальные препараты Разрабатываются, изучаются и производятся в соответствии с требованиями международных стандартов - - Правила GLP
- 23. Правила GLP Определяют условия и процесс проведения доклинических исследований, включающий планирование, выполнение, контроль и регистрацию, позволяя
- 24. Клинические исследования В первой фазе устанавливают: переносимость безопасность фармакокинетические и фармакодинамические характеристики терапевтическое действие исследуемого лекарственного
- 25. Клинические исследования Целью второй фазы является доказать клиническую эффективность лекарственного средства при испытании на группе пациентов
- 26. Клинические исследования В третьей фазе определяют: эффективность и безопасность лекарственного средства устанавливают характер и частоту побочных
- 27. Клинические исследования Четвертая фаза клинических испытаний проводится после получения разрешения на медицинское применение препарата. Устанавливают новые
- 28. Правила GMP Единая система требований по организации технологических процессов и контрольных испытаний промежуточных и конечных продуктов
- 29. Основной принцип GMP «Избегать дефектов, а не обнаруживать их в готовой продукции»
- 30. Суть правил GMP Делать все как положено (согласно нормативной документации) Не допускать загрязнений Использовать только качественные
- 31. Правила GMP Соблюдение этих требований является гарантией того, что лекарственное средство Изготовлено в соответствии с его
- 32. Внедрение стандартов GMP в России В РФ 525 отечественных фармацевтических предприятий, из них только 10 соответствуют
- 33. GMP в России (2010 год) Из 1100 фармпредприятий 10 % оборудованы в соответствии со стандартами GMP
- 34. Фармпредприятия в РФ, работающие по стандартам GMP «Нижфарм» «Хемофарм» «Макиз-Фарма» «Петровакс-Фарм» «Сотекс» ЗиО-Здоровье (ГК Actavis) Из
- 35. Фармпредприятия в РФ, имеющие участки, оборудованные по стандартам GMP «Фармстандарт» «Верофарм» Из доклада Е.А.Тельновой на конференции
- 36. GMP в России Приказ Минпромторга России от 14 июня 2013 г. № 916 «ОБ УТВЕРЖДЕНИИ ПРАВИЛ
- 37. Дженерики Термин дженерик возник в 70-е годы ХХ века В то время дженерики должны были называться
- 38. Дженерики Сегодня по внешним признакам отличить оригинальный препарат от дженерика невозможно В Бразилии для распознавания дженерика
- 39. Полная информация о ЛП на рынке США Сведения о лекарственных препаратах общедоступны В Интернете - таблицы
- 40. “Orange Book” Кодом «А» обозначены дженерики, которые можно использовать наравне с оригинальными препаратами (терапевтически эквивалентны и
- 41. “Orange Book” Кодом «В» обозначены дженерики, которые нельзя считать терапевтически эквивалентными оригинальному препарату Соколов А.В. и
- 42. Оригинальные препараты и дженерики Для оценки качества, эффективности, безопасности и адекватной замены установлены три вида эквивалентности:
- 43. Фармацевтическая эквивалентность Фармацевтически эквивалентные лекарственные препараты содержат одинаковые активные ингредиенты в одинаковой лекарственной форме, предназначены для
- 44. Биоэквивалентность Биоэквивалентные лекарственные препараты – это фармацевтически эквивалентные или фармацевтически альтернативные препараты, обладающие сопоставимой биологической доступностью,
- 45. Биологическая доступность «Биологическая доступность – это степень, в которой лекарственное вещество всасывается из места введения в
- 46. Показатели биодоступности максимальная концентрация активной субстванции в плазме крови (Сmax) время достижения этой концентрации в крови
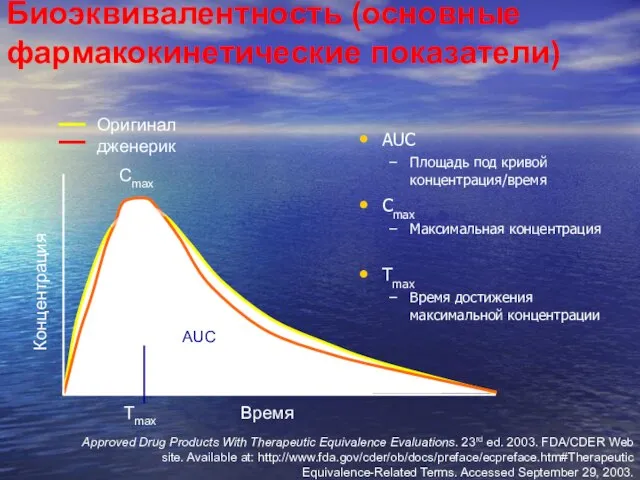
- 47. Биоэквивалентность (основные фармакокинетические показатели) AUC Площадь под кривой концентрация/время Cmax Максимальная концентрация Tmax Время достижения максимальной
- 48. Биоэквивалентность Препараты считаются биоэквивалентными, если границы доверительного интервала дженерика в 90 % случаев для Cmax находятся
- 49. Биоэквивалентность В России в 2004 г. утверждены правила «Проведение качественных исследований биоэквивалентности лекарственных средств» Содержание действующего
- 50. Правила регистрации дженериков в РФ упрощены. Не учитываются: Состав вспомогательных веществ Содержание токсичных примесей Содержание продуктов
- 51. В 2000 году проведена проверка биоэквивалентности по стандартам Американской фармакопеи ного 40 дженериков кларитромицина из 13
- 52. Кларитромицин и его дженерики Результаты проверки: из 70 % дженериков действующее вещество высвобождалось значительно медленнее 20
- 53. Биоэквивалентность – это не гарантия, а предположение терапевтической эквивалентности и безопасности ЛП
- 54. Терапевтическая эквивалентность Терапевтическая эквивалентность, согласно Европейским и Американским определениям, предусматривает кроме сходного фармакинетического профиля еще и
- 55. Терапевтическая эквивалентность Дженерик терапевтически эквивалентен другому препарату, если он по результатам клинических исследований обладает такой же
- 56. Терапевтическая эквивалентность В 1998 году FDA был опубликован проект правил оценки терапевтической эквивалентности дженериков. Было предложено
- 57. Опрос врачей в Израиле 61 % врачей назначают дженерики, исходя из экономических соображений 73 % считают,
- 58. Биологические препараты (высокомолекулярные соединения) Биосимиляры (Biosimilar) Каждый биопрепарат (гормоны, вакцины, ферменты, факторы свертывания крови и пр.)
- 59. ФАРМАЦЕВТИЧЕСКИЕ ФАКТОРЫ Физическое состояние ЛВ (размер частиц, форма кристаллов, наличие или отсутствие заряда на поверхности частиц
- 60. Технологические или производственные процессы Очистка Сушка Измельчение Перекристаллизация Способ грануляции Давление прессования таблеток Плотность масс в
- 61. Вспомогательные вещества Растворители Основы для мазей Основы для суппозиториев Основы для присыпок Основы для разбавления порошков
- 62. Вспомогательные вещества Вещества для покрытий Поверхностно-активные вещества Вещества, увеличивающие вязкость Вещества, сохраняющие влажность Корригирующие вещества Красители
- 63. Типы взаимодействия в системе ЛВ – вспомогательное вещество Образование водородных связей Силы Ван-дер-Ваальса Ковалентные связи Т.С.Кондратьева
- 64. Результат взаимодействия между лекарственными и вспомогательными веществами Реакции комплексообразования Реакции адсорбции Оказывают влияние на: биологическую доступность;
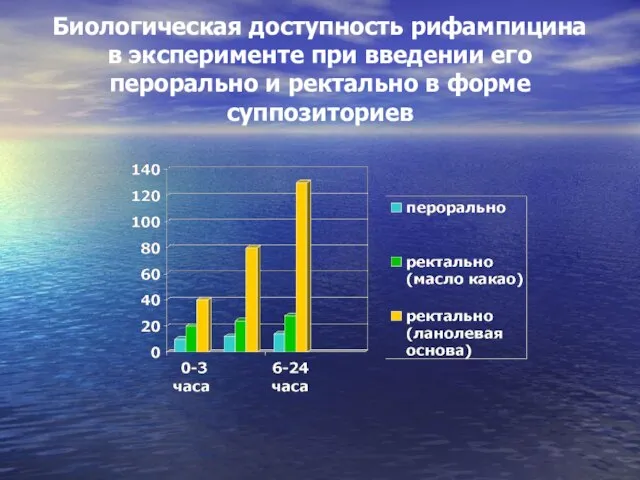
- 65. Биологическая доступность рифампицина в эксперименте при введении его перорально и ректально в форме суппозиториев
- 66. Единственный оригинальный флуконазол, рекомендованный ВОЗ для лечения кандидозного вульвовагинита (молочницы)5
- 67. Формы выпуска Дифлюкана Дифлюкан капсулы 150 мг №1, №4 и № 12 Дифлюкан капсулы 50 мг
- 68. Дифлюкан В процессе изучения Дифлюкана было проведено 28 клинических испытаний в 19 странах мира приняли участие
- 69. Дженерики Дифлюкана (30) Дифлузол Микофлюкан Медофлюкон Фунголон Нофунг Флукозан Проканазол Флукомицид Флюмикон Флуконазол-Верте Флузол Флуконазол-КФ Флукозид
- 70. Дженерики Дифлюкана в РФ Дифлазон (KRKA, Словения) Флюкостат (Фармстандарт, Россия) Микосист (Gedeon Richter, Венгрия) Флуконазол (Hemofarm,
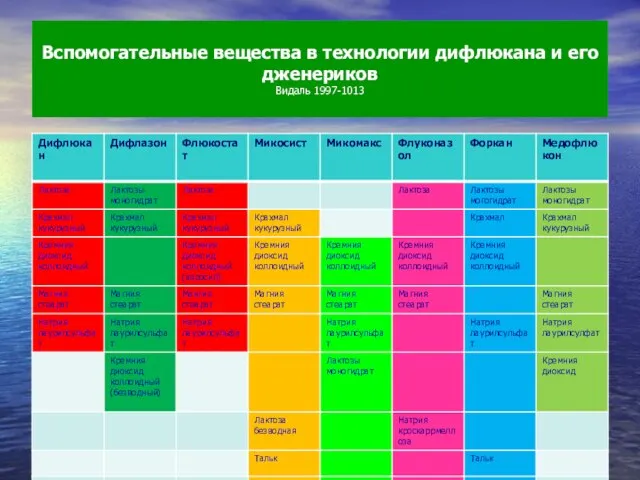
- 71. Вспомогательные вещества в технологии дифлюкана и его дженериков Видаль 1997-1013
- 72. Сравнение фунгицидной активности различных препаратов, содержащих флуконазол (in vitro ) НИИ медицинской микологии им.П.Н.Кашкина, С.Петербург Метод
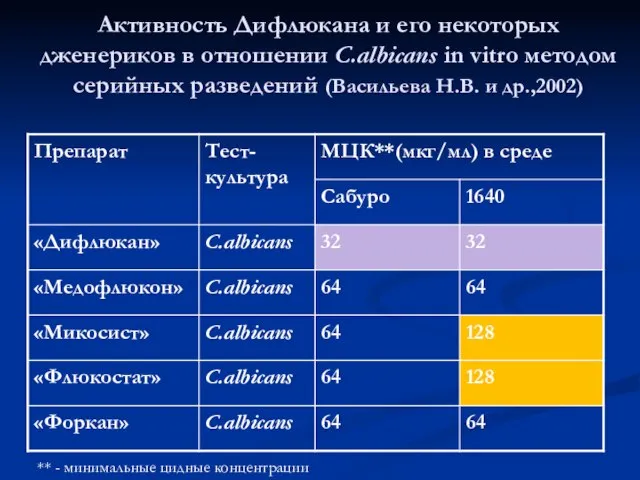
- 73. Активность Дифлюкана и его некоторых дженериков в отношении C.albicans in vitro методом серийных разведений (Васильева Н.В.
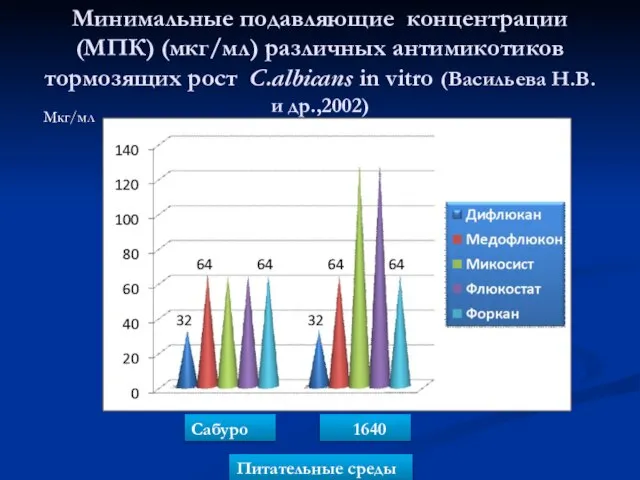
- 74. Минимальные подавляющие концентрации (МПК) (мкг/мл) различных антимикотиков тормозящих рост C.albicans in vitro (Васильева Н.В. и др.,2002)
- 75. Оценка эффективности Дифлюкана и его дженериков в опытах in vitro НИИ вакцин и сывороток им. И.И.
- 76. Музейные штаммы дрожжей Candida albicans (ВКПМ Y-3108) Candida glabrata (КБП 3049) Candida рarapsilosis (КБП 3050) Эксперименты
- 77. Метод измерения зон ингибиции роста дрожжей (Луночно-диффузионный метод, МУК 4.2. 1890-04)
- 78. Дифлюкан и дженерики Во всех случаях была установлена наибольшая активность Дифлюкана – оригинального препарата Т.М.Желтикова, А.М.
- 79. Дифлюкан®. Фармакоэкономика. Цель : изучение клинической и экономической эффективности Дифлюкана и некоторых его дженериков при лечении
- 80. Фармакоэкономическое исследование Дизайн исследования: проспективное, сравнительное, рандомизированное. В исследование вошло 330 пациенток, которые были разделены на
- 81. Результаты клинической эффективности: Критерий: отсутствие каких-либо жалоб, клинических симптомов и нормализация лабораторных показателей. у 98,4% пациенток,
- 82. Цена в аптеках г.Москвы различных препаратов, содержащих флуконазол (150 мг) на 19.11.13 www.aptekamos.ru
- 83. Сроки годности капсул Дифлюкана и его дженериков Дифлюкан – 5 лет Флюкостат – 2 года Микосист
- 85. Скачать презентацию












































































 Содержание Концепции компетентностно- ориентированного образования и меры по ее реализации
Содержание Концепции компетентностно- ориентированного образования и меры по ее реализации Архангельск, тренинг промоутеров
Архангельск, тренинг промоутеров Проект – презентация«Город Николаевск – на – Амуре»
Проект – презентация«Город Николаевск – на – Амуре» wellies a rubber
wellies a rubber Зотова Ирина, родилась на Юге России. Аспирантка Российской Академии Государственной Службы. Кафедра Акмеологии и психологии проф
Зотова Ирина, родилась на Юге России. Аспирантка Российской Академии Государственной Службы. Кафедра Акмеологии и психологии проф Эмоциональный интеллект. Развитие ребенка - развитие семьи
Эмоциональный интеллект. Развитие ребенка - развитие семьи Новый программный продукт для предприятий электроэнергетики!
Новый программный продукт для предприятий электроэнергетики! Номинация проекта: «Математическое моделирование реальных процессов в природе и обществе»
Номинация проекта: «Математическое моделирование реальных процессов в природе и обществе» Формирование метапредметных компетенций школьников в урочной и внеурочной деятельности
Формирование метапредметных компетенций школьников в урочной и внеурочной деятельности 1-2 Software
1-2 Software Стажировка в Высшей медицинской школе Ганновера (Германия)
Стажировка в Высшей медицинской школе Ганновера (Германия) Oriflame. Вырасти от старшего менеджера до директора
Oriflame. Вырасти от старшего менеджера до директора 39 лет итальянской красоты от природы 1972В Пиенце (Тоскания, Италия) открывается лавка, торгующая лечебными травами под названием Botte
39 лет итальянской красоты от природы 1972В Пиенце (Тоскания, Италия) открывается лавка, торгующая лечебными травами под названием Botte Опыт внедрения системы Офис-кайдзен в ТЭЦ ОАО Иркутскэнерго
Опыт внедрения системы Офис-кайдзен в ТЭЦ ОАО Иркутскэнерго Extra sport club
Extra sport club Культура и быт России в XVII веке
Культура и быт России в XVII веке Осуществление системного подхода к формированию мыслительных умений и навыков в процессе преподавания физики
Осуществление системного подхода к формированию мыслительных умений и навыков в процессе преподавания физики Композиция и сюжет в изобразительном искусстве
Композиция и сюжет в изобразительном искусстве Плоскость. Прямая. Луч.
Плоскость. Прямая. Луч. ВНЕУРОЧНАЯ ДЕЯТЕЛЬНОСТЬКАК СОСТАВЛЯЮЩАЯФедерального государственногообразовательного стандарта НОВОГО ПОКОЛЕНИЯ
ВНЕУРОЧНАЯ ДЕЯТЕЛЬНОСТЬКАК СОСТАВЛЯЮЩАЯФедерального государственногообразовательного стандарта НОВОГО ПОКОЛЕНИЯ Презентация на тему COLOURS
Презентация на тему COLOURS  МАСС-СПЕКТРОМЕТРИЯ В ПРОТЕОМНЫХ ИССЛЕДОВАНИЯХ
МАСС-СПЕКТРОМЕТРИЯ В ПРОТЕОМНЫХ ИССЛЕДОВАНИЯХ Магнитогорский государственный технический университет им. Г.И. Носова. Институт строительства архитектуры и искусства. Дизайн
Магнитогорский государственный технический университет им. Г.И. Носова. Институт строительства архитектуры и искусства. Дизайн Презентация на тему Диагностика эффективности внеурочной деятельности
Презентация на тему Диагностика эффективности внеурочной деятельности  Инструментальный ансамбль Путешествуем с гитарой. Итоги учебного года 2019-2020
Инструментальный ансамбль Путешествуем с гитарой. Итоги учебного года 2019-2020 Учтивость в словах и обращениях современного школьника.
Учтивость в словах и обращениях современного школьника. Приёмы работы с картиной
Приёмы работы с картиной Сотовый телефон : за и против
Сотовый телефон : за и против