Содержание
- 2. С Е Л Е Н
- 3. Se, «селен», химический элемент с атомным номером 34, атомная масса 78,96. Природный селен состоит из шести
- 4. Последовательной ионизации 9,752, 21,2, 32,0, 42,9 и 68,3 эВ. Расположен в VIA группе в 4 периоде
- 5. История открытия Селен был открыт в 1817 шведским химиком Й. Я. Берцелиусом в шламах свинцовых камер
- 6. Нахождение в природе Селен редкий, рассеянный элемент. Содержание в земной коре 1,4·10–5% по массе. Селениды почти
- 7. Получение Основные источники селена — пыль, образующаяся при обжиге селенсодержащих сульфидов и шламы свинцовых камер. После
- 8. Селеновая кислота при нагревании с соляной кислотой восстанавливается до селенистой кислоты. Затем через полученный раствор селенистой
- 9. Для очистки селен далее сжигают в кислороде, насыщенном парами дымящей азотной кислоты HNO3. При этом сублимируется
- 10. Селен — серый, с металлическим блеском хрупкий неметалл. Физические свойства
- 11. Физические свойства При атмосферном давлении существует несколько десятков модификаций селена. Наиболее стабилен серый селен, g-Se, с
- 12. Физические свойства Из растворов селена в CS2 выделены три модификации красного кристаллического: селена с моноклинной решеткой;
- 13. Физические свойства При восстановлении селенистой кислоты или быстром охлаждении паров селена образуется аморфный красный селен. От
- 14. Химические свойства Селен химически активен. При нагревании на воздухе сгорает с образованием бесцветного кристаллического SeO2: Se
- 15. Химические свойства Со фтором , хлором и бромом селен реагирует при комнатной температуре. С иодом селен
- 16. Химические свойства С неокисляющими и разбавленными кислотами селен не взаимодействует. С концентрированной серной кислотой селен взаимодействует
- 17. Химические свойства При кипячении в щелочных растворах селен диспропорционирует: 3Se + 6KOH = K2SeO3 + 2K2Se
- 18. Химические свойства Если селен кипятят в щелочном растворе, через который пропускают воздух или кислород, то образуются
- 19. Химические свойства Селен взаимодействует с сульфидами и полисульфидами с образованием тиоселенидов. При нагревании селена с растворами
- 20. Химические свойства Сильные окислители ( озон О3, фтор F2) окисляют селен до Se+6: Se + O3
- 21. Применение Аморфный Se входит в состав светочувствительных слоев в ксерографии и лазерных принтерах. Серый Se применяется
- 22. Физиологическое действие Микроэлемент (массовая доля в организме 10–5–10–7%). В организм человека селен поступает с пищей (55–110
- 23. Физиологическое действие В малых количествах селен должен содержаться в пище цыплят, телят, ягнят и кроликов. Селен
- 24. Физиологическое действие Селен способен предохранять организм от отравления ртутью и кадмием, так как связывает их. Существует
- 26. Скачать презентацию























 Основные направления инвестирования в Российской Федерации
Основные направления инвестирования в Российской Федерации  Учебная дисциплина. Психология
Учебная дисциплина. Психология Ачинск – город с историей
Ачинск – город с историей Презентация на тему Государства и народы доколумбовой Америки
Презентация на тему Государства и народы доколумбовой Америки  Сочинение с элементами описания внутреннего состояния по картине Н. Богданова-Бельского «У дверей школы»
Сочинение с элементами описания внутреннего состояния по картине Н. Богданова-Бельского «У дверей школы» Откройте для себя здоровую, юную кожу
Откройте для себя здоровую, юную кожу ПРАВАЧЕЛОВЕКА
ПРАВАЧЕЛОВЕКА Принципы организации судебной власти
Принципы организации судебной власти « У нас много замечательных и любимых не только нами, но и всем миром, писателей. Чехов занимает одно из первых мест среди них ». К. А.
« У нас много замечательных и любимых не только нами, но и всем миром, писателей. Чехов занимает одно из первых мест среди них ». К. А.  Музыкальная живопись и живописная музыка. Импрессионизм.
Музыкальная живопись и живописная музыка. Импрессионизм. Установка для повторного нанесения покрытия на аноды компании Каустик
Установка для повторного нанесения покрытия на аноды компании Каустик Rome Model United Nations Rome International Careers
Rome Model United Nations Rome International Careers  История Российского самодержавия
История Российского самодержавия Добро пожаловать на час общения «Поговорим о любви»
Добро пожаловать на час общения «Поговорим о любви» Технология моделирования в начальной школе Сложным является сообщение учащимся знаний, так как их объем из года в год увеличивает
Технология моделирования в начальной школе Сложным является сообщение учащимся знаний, так как их объем из года в год увеличивает Рациональное питание. Расчет меню
Рациональное питание. Расчет меню Планета дорог
Планета дорог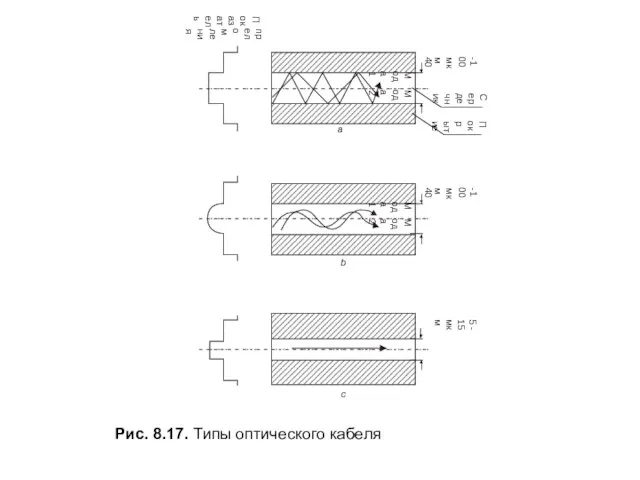 Рис. 8.17. Типы оптического кабеля
Рис. 8.17. Типы оптического кабеля Обширный информационный сервис по Европейскому Союзу, странам Европы и актульным событиям, происходящим в Европе
Обширный информационный сервис по Европейскому Союзу, странам Европы и актульным событиям, происходящим в Европе Идеал человеческого единства
Идеал человеческого единства Конкурс «Роялти – педагогу новатору»
Конкурс «Роялти – педагогу новатору» Современное состояние классовой борьбы в Австралии и Новой Зеландии
Современное состояние классовой борьбы в Австралии и Новой Зеландии Фото_Чек_лист_08_09_2022_ПВЗ_Октябрьское_поле
Фото_Чек_лист_08_09_2022_ПВЗ_Октябрьское_поле Причастия действительные и страдательные
Причастия действительные и страдательные Презентация на тему Природная зона тайги
Презентация на тему Природная зона тайги Multilayer model in optics. New analitic results.
Multilayer model in optics. New analitic results. Синтаксическая стилистика
Синтаксическая стилистика Презентация на тему Совесть и раскаяние (4 класс)
Презентация на тему Совесть и раскаяние (4 класс)