Содержание
- 2. 2. РЕАКЦИИ ЗАМЕЩЕНИЯ АЛКАНОВ. Механизм реакций 2.1 Галогенирование Общая cхема: R-H + X2 R-X + HX
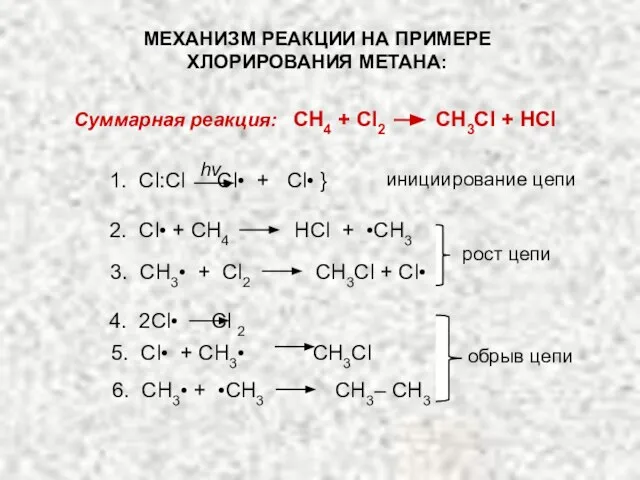
- 3. МЕХАНИЗМ РЕАКЦИИ НА ПРИМЕРЕ ХЛОРИРОВАНИЯ МЕТАНА: Суммарная реакция: CH4 + Cl2 CH3Cl + HCl 1. Cl:Cl
- 4. Хлорирование метана – цепная реакция, т.е. реакция, включающая ряд стадий, каждая из которых гене-рирует реакционноспособную частицу,
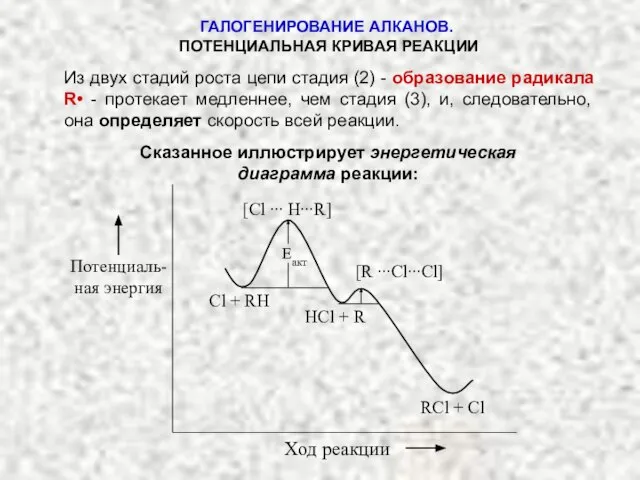
- 5. ГАЛОГЕНИРОВАНИЕ АЛКАНОВ. ПОТЕНЦИАЛЬНАЯ КРИВАЯ РЕАКЦИИ Из двух стадий роста цепи стадия (2) - образование радикала R•
- 6. ОРИЕНТАЦИЯ ПРИ ГАЛОГЕНИРОВАНИИ: Проблема ориентации возникает всякий раз, когда реагент может атаковать различные по реакционной способности
- 7. ОРИЕНТАЦИЯ ПРИ ГАЛОГЕНИРОВАНИИ: Поскольку скоростьопределяющей стадией является стадия образования промежуточного алкильного радикала R•, направление реакции, т.
- 8. Как общее правило можно принять: ОРИЕНТАЦИЯ ПРИ ГАЛОГЕНИРОВАНИИ: «Реакция идет тем легче, чем легче образуются характеризующие
- 9. Ряд изменения устойчивости радикалов: третичный > вторичный > первичный Отсюда следует, что легче всего замещение атомов
- 10. Примечание: Сказанное не означает, однако, что количество изо-пропилхлорида, образующегося в реакции хлорирования пропана будет в 3
- 11. 2. Нитрование алканов разб. HNO3 при нагревании ( Коновалов 1888г.) 1. HO-NO2 HO• + •NO2 t0
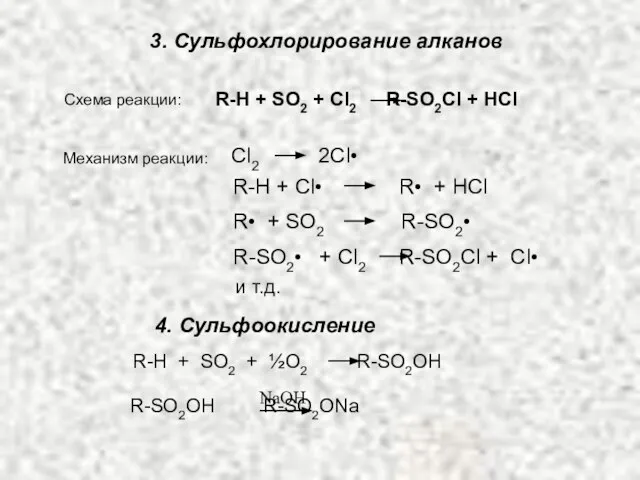
- 12. 3. Сульфохлорирование алканов Схема реакции: R-H + SO2 + Cl2 R-SO2Cl + HCl Сl2 2Cl• R-H
- 13. РЕАКЦИЯ СУЛЬФОХЛОРИРОВАНИЯ Реакция сульфохлорирования алканов впервые была использована в Германии в 1939-1940 гг. для получения заменителей
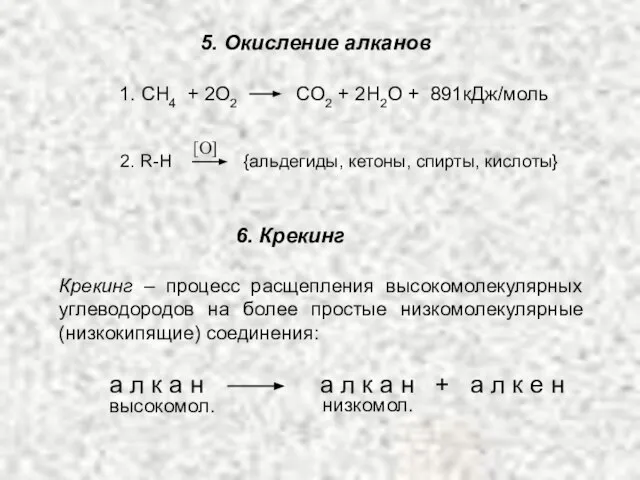
- 14. 5. Окисление алканов 1. СH4 + 2O2 CO2 + 2H2O + 891кДж/моль [O] 2. R-H {альдегиды,
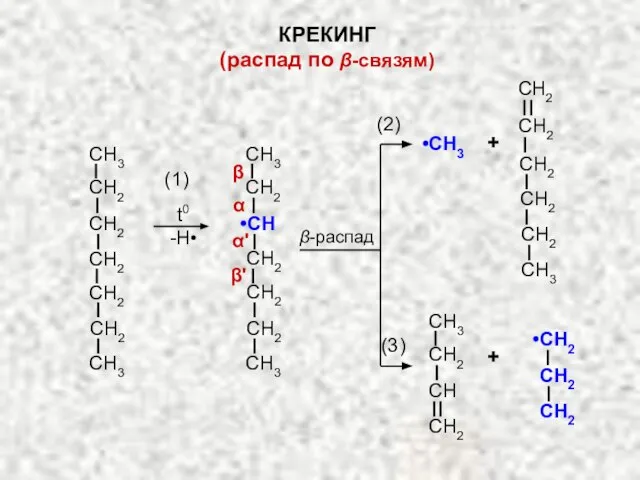
- 15. t0 -H• β-распад •CH3 + + (1) (2) (3) КРЕКИНГ (распад по β-связям)
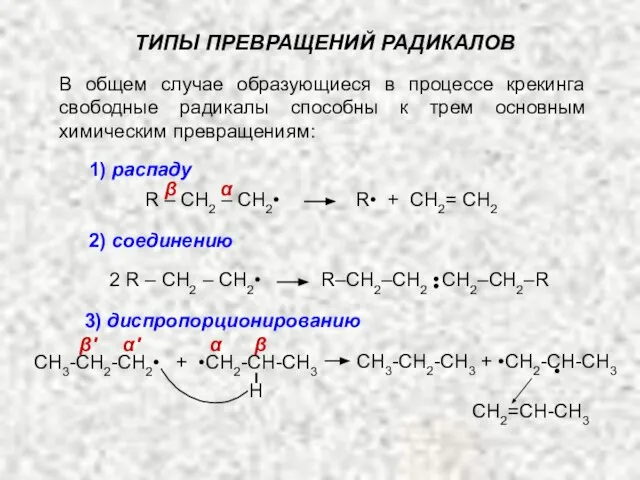
- 16. В общем случае образующиеся в процессе крекинга свободные радикалы способны к трем основным химическим превращениям: ТИПЫ
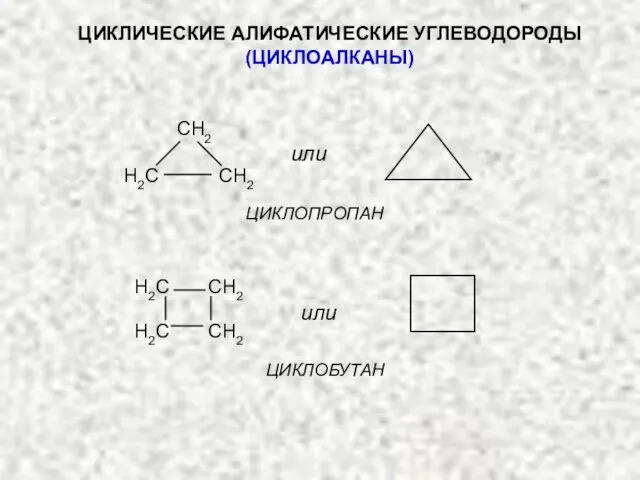
- 17. ЦИКЛИЧЕСКИЕ АЛИФАТИЧЕСКИЕ УГЛЕВОДОРОДЫ (ЦИКЛОАЛКАНЫ) или H2C CH2 H2C CH2 или ЦИКЛОПРОПАН ЦИКЛОБУТАН
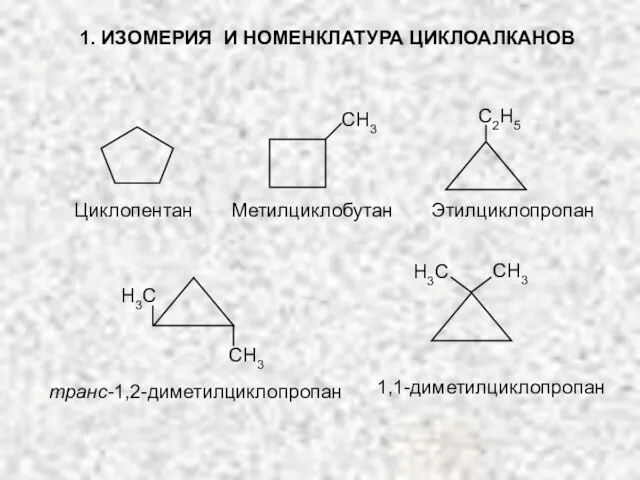
- 18. 1. ИЗОМЕРИЯ И НОМЕНКЛАТУРА ЦИКЛОАЛКАНОВ СH3 С2H5 Циклопентан Метилциклобутан Этилциклопропан СH3 H3С H3С СH3 транс-1,2-диметилциклопропан 1,1-диметилциклопропан
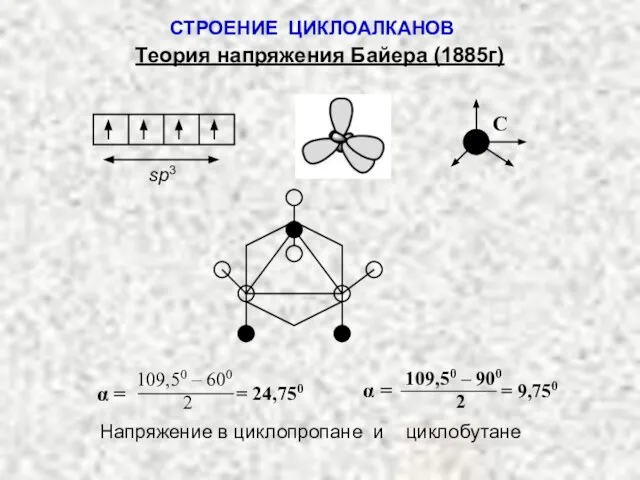
- 19. СТРОЕНИЕ ЦИКЛОАЛКАНОВ Теория напряжения Байера (1885г) sp3 C 109,50 – 600 2 α = = 24,750
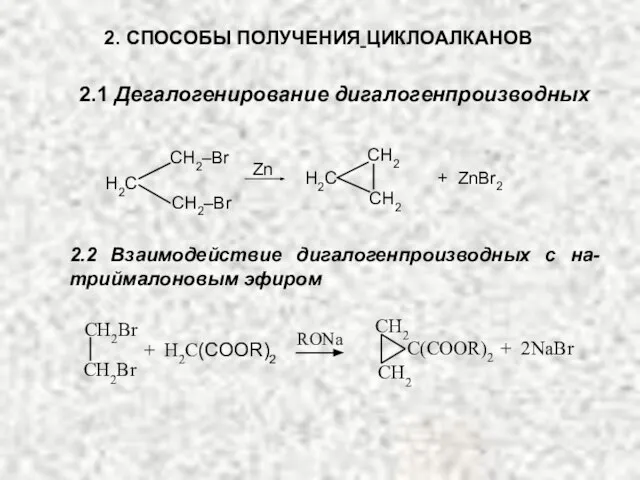
- 20. 2. СПОСОБЫ ПОЛУЧЕНИЯ ЦИКЛОАЛКАНОВ 2.1 Дегалогенирование дигалогенпроизводных H2С СH2–Br СH2–Br H2С СH2 СH2 Zn + ZnBr2
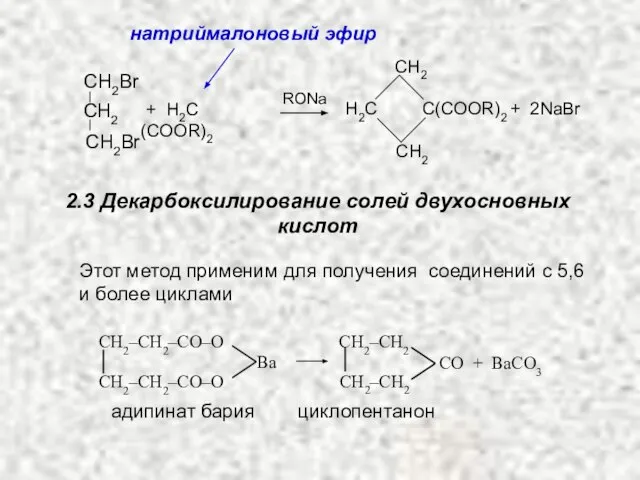
- 21. СH2 СH2 H2С С(COOR)2 + 2NaBr + H2С(COOR)2 RONa СH2Br СH2Br СH2 натриймалоновый эфир 2.3 Декарбоксилирование
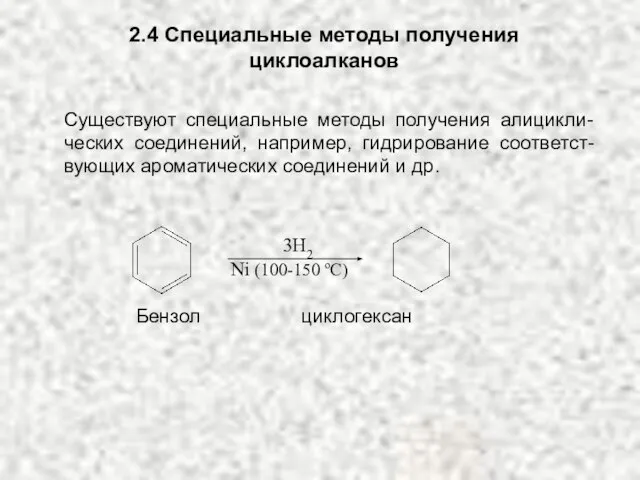
- 22. 2.4 Специальные методы получения циклоалканов 3H2 Ni (100-150 oC) Существуют специальные методы получения алицикли-ческих соединений, например,
- 23. 3. ФИЗИЧЕСКИЕ СВОЙСТВА ЦИКЛОАЛКАНОВ Циклические соединения обычно имеют более высокую температуру кипения и плавления и большую
- 24. 3. ХИМИЧЕСКИЕ СВОЙСТВА ЦИКЛОАЛКАНОВ Химические свойства циклоалканов зависят от величины цикла. Соединения с малым размером (3-,4-членные)
- 25. Гидрирование СH2–СН2 СH2–СН2 CH2 + H2 СН3–СН2–СН2-CH2–СН3 Pd 300 oC Пятичленный цикл разрывается только при высоких
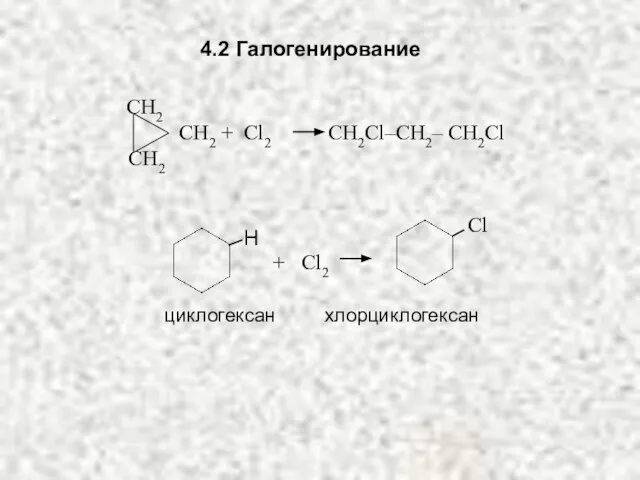
- 26. 4.2 Галогенирование СH2 СH2 СН2 + Cl2 CH2Cl–CH2– CH2Cl Сl H + Cl2 циклогексан хлорциклогексан
- 27. 4.3 Действие галогеноводородов СH2 СH2 СН–R + HBr R–CHBr–CH2– CH3 Циклопропан и его гомологи реагируют с
- 28. ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ. ПРИМЕНЕНИЕ Циклопропан – газообразное вещество с т.кип. –34 оС получают в промышленном масштабе обработкой
- 30. Скачать презентацию














 Игровая зависимость
Игровая зависимость Групповой психоанализ
Групповой психоанализ О РАБОТЕ СЕКЦИИ ПРОМЫШЛЕННОЙ ЭКОЛОГИИ И РАЦИОНАЛЬНОГО ПРИРОДОПОЛЬЗОВАНИЯ ПО ВОПРОСАМ ВОДОПОЛЬЗОВАНИЯ В ОРЕНБУРГСКОЙ ОБЛАСТИ
О РАБОТЕ СЕКЦИИ ПРОМЫШЛЕННОЙ ЭКОЛОГИИ И РАЦИОНАЛЬНОГО ПРИРОДОПОЛЬЗОВАНИЯ ПО ВОПРОСАМ ВОДОПОЛЬЗОВАНИЯ В ОРЕНБУРГСКОЙ ОБЛАСТИ Animals in the ABC
Animals in the ABC План реализации проекта
План реализации проекта Константин Симонов
Константин Симонов Презентация на тему Малые тела солнечной системы
Презентация на тему Малые тела солнечной системы Заповеди любви
Заповеди любви Вальдорфская школа
Вальдорфская школа Во что верят люди? Религия. Тема №2
Во что верят люди? Религия. Тема №2 Тициан. Жизнь и творчество.. Жизнь Тициана: Жизнь Тициана:ТИЦИАН (1476/77 –1576), венецианский живописец эпохи Возрождения. Родился в гор
Тициан. Жизнь и творчество.. Жизнь Тициана: Жизнь Тициана:ТИЦИАН (1476/77 –1576), венецианский живописец эпохи Возрождения. Родился в гор Йо-йо
Йо-йо Привет, Весна!
Привет, Весна! Совместная маркетинговая программа «Сервис Плюс» для партнеров
Совместная маркетинговая программа «Сервис Плюс» для партнеров Кровотечения. Первая медицинская помощь
Кровотечения. Первая медицинская помощь Предпрофильная подготовка
Предпрофильная подготовка Проект: Юный проповедник 2017
Проект: Юный проповедник 2017 Металлургический комплекс России
Металлургический комплекс России Право + Защита прав людей, живущих с ВИЧ
Право + Защита прав людей, живущих с ВИЧ Грин стар
Грин стар Грамматика со смешариками
Грамматика со смешариками Эпоха ХХ века - эра великих людей и изобретений
Эпоха ХХ века - эра великих людей и изобретений Презентация на тему Исторический обзор садово-паркового искусства
Презентация на тему Исторический обзор садово-паркового искусства Авиация Советского Союза
Авиация Советского Союза Элетронная таблица Excel
Элетронная таблица Excel Гороскоп первоклассника
Гороскоп первоклассника Модели смертности
Модели смертности «Государственно-частное партнерство: региональный аспект»
«Государственно-частное партнерство: региональный аспект»