Содержание
Слайд 2Химический анализ качества природной воды
Задача №6. Имеется 10 л раствора, содержащий 200
Химический анализ качества природной воды
Задача №6. Имеется 10 л раствора, содержащий 200

мг CaSO4 и 100 мг MgSO4 . Требуется определить общую жесткость раствора
( Жобщ. ) в мг-экв/л.
Решение: И так, требуется определить раствора Жобщ.
в мг-экв/л. Поэтому необходимо вычислить эквивалентные массы этих соединений с последующим вычислением числа экв. (n CaSO4 , n MgSO4 ):
ЭCaSO4 =(40+96)/2=68 мг/мг-экв
ЭMgSO4 =(24+96)/2=60 мг/мг-экв
Данные соединения растворены в 10 л воды и, соответственно, в 1 л воды их будет в 10 раз меньше (20 мг/л CaSO4 и 10 мг/л MgSO4).
И, окончательно, Жобщ. = n CaSO4 + n MgSO4 = (20 мг/л CaSO4 )/68мг/мг-экв + (10 мг/л MgSO4 )/60мг/мг-экв = (0,29 +0,17)=0,46 мг-экв/л.
( Жобщ. ) в мг-экв/л.
Решение: И так, требуется определить раствора Жобщ.
в мг-экв/л. Поэтому необходимо вычислить эквивалентные массы этих соединений с последующим вычислением числа экв. (n CaSO4 , n MgSO4 ):
ЭCaSO4 =(40+96)/2=68 мг/мг-экв
ЭMgSO4 =(24+96)/2=60 мг/мг-экв
Данные соединения растворены в 10 л воды и, соответственно, в 1 л воды их будет в 10 раз меньше (20 мг/л CaSO4 и 10 мг/л MgSO4).
И, окончательно, Жобщ. = n CaSO4 + n MgSO4 = (20 мг/л CaSO4 )/68мг/мг-экв + (10 мг/л MgSO4 )/60мг/мг-экв = (0,29 +0,17)=0,46 мг-экв/л.
Слайд 3Задачи по физико-химической очистке
воды
Задача №7. Имеется 0,1 и 0,01 м раствор
Задачи по физико-химической очистке
воды
Задача №7. Имеется 0,1 и 0,01 м раствор

НСI. Требуется вычислить рН этих растворов.
Решение: Запишем уравнение диссоциации соляной кислоты и концентрации ионов и молекул кислоты для первого и второго растворов :
НСI = Н+ + СI –
0,1 г-моль/л 0,1 г-ион/л 0,1 г-ион/л
0,01 г-моль/л 0,01 г-ион/л 0,01 г-ион/л
Из определения величины рН запишем следующее выражение и подставим численные значения концентрации ионов водорода:
рН= -Lg [ Н+ ( г-ион/л) ] = -Lg [0,1]= -Lg [10-1] = 1, для первого р-ра и
рН= -Lg [ Н+ ( г-ион/л) ] = -Lg [0,01]= -Lg [10-2] = 2, для второго р-ра.
Решение: Запишем уравнение диссоциации соляной кислоты и концентрации ионов и молекул кислоты для первого и второго растворов :
НСI = Н+ + СI –
0,1 г-моль/л 0,1 г-ион/л 0,1 г-ион/л
0,01 г-моль/л 0,01 г-ион/л 0,01 г-ион/л
Из определения величины рН запишем следующее выражение и подставим численные значения концентрации ионов водорода:
рН= -Lg [ Н+ ( г-ион/л) ] = -Lg [0,1]= -Lg [10-1] = 1, для первого р-ра и
рН= -Lg [ Н+ ( г-ион/л) ] = -Lg [0,01]= -Lg [10-2] = 2, для второго р-ра.
- Предыдущая
Минералов СеменСледующая -
Мир птиц. Тест Изучение движения тела по окружности под действием сил упругости и тяжести
Изучение движения тела по окружности под действием сил упругости и тяжести Молекулярная физика. Ученые и их открытия
Молекулярная физика. Ученые и их открытия Презентация на тему Радиация и ее влияние на человека
Презентация на тему Радиация и ее влияние на человека  Недомолвки в теории и недостатки в практике регистрации частичных разрядов
Недомолвки в теории и недостатки в практике регистрации частичных разрядов Фотоэффект. Самостоятельная работа
Фотоэффект. Самостоятельная работа Работа электрического тока
Работа электрического тока Корпускулярно-волновой дуализм
Корпускулярно-волновой дуализм Плотность. Решение задач
Плотность. Решение задач Презентация на тему Паровая машина. Паровой двигатель Уатта
Презентация на тему Паровая машина. Паровой двигатель Уатта  Кіріспе. Термодинамикалық жүйе, процесс және тепе-теңдік
Кіріспе. Термодинамикалық жүйе, процесс және тепе-теңдік Метрология
Метрология Импульс. Закон сохранения импульса
Импульс. Закон сохранения импульса Геометрическая оптика. (Лекция 6)
Геометрическая оптика. (Лекция 6) Преобразование диаграммы условного напряжения - деформация в диаграмму истинного напряжения - деформация в программе Abaqus
Преобразование диаграммы условного напряжения - деформация в диаграмму истинного напряжения - деформация в программе Abaqus Типы соединений потребителей тока
Типы соединений потребителей тока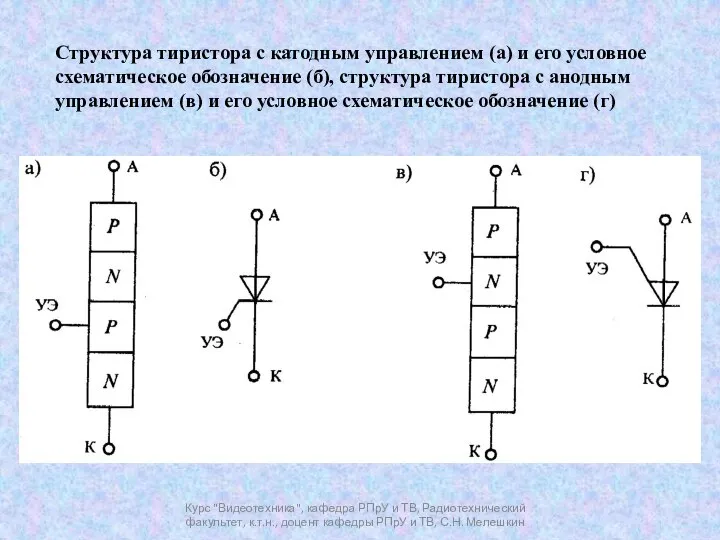 Тиристор
Тиристор Идеальный газ в МКТ
Идеальный газ в МКТ Напряженность электростатического поля
Напряженность электростатического поля Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Электрический заряд. Строение атома
Электрический заряд. Строение атома Сила пара
Сила пара Квантовые свойства электромагнитного излучения
Квантовые свойства электромагнитного излучения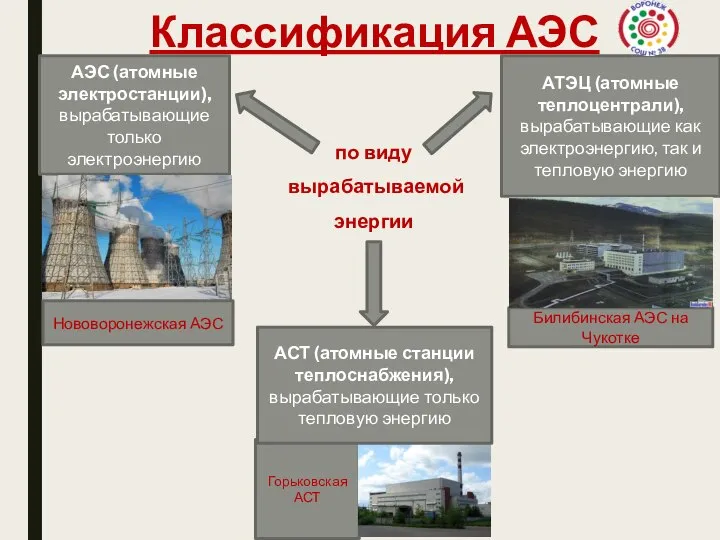 Классификация АЭС
Классификация АЭС Слайды по физике
Слайды по физике Перфора́тор
Перфора́тор Классификации тормозов
Классификации тормозов Течь жидкости ГУР
Течь жидкости ГУР Инфразвук. инфразвуковые волны
Инфразвук. инфразвуковые волны