Содержание
- 2. АЛКАНЫ Получение, нахождение в природе и применение алканов ВПЕРЕД НАЗАД
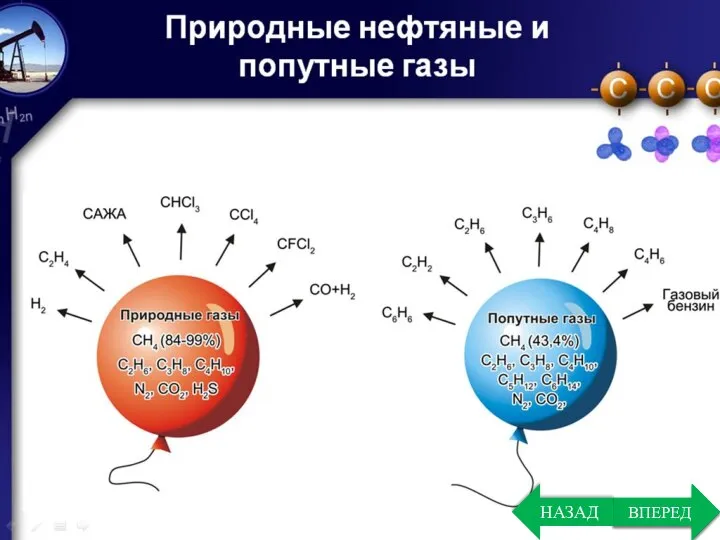
- 3. ВПЕРЕД Газообразные алканы получают из природного и попутного нефтяных газов; Жидкие и твердые – из нефти.
- 4. ВПЕРЕД Рудничный газ состоит из МЕТАНА Природный газ на 95% состоит из метана МЕТАН называют ещё
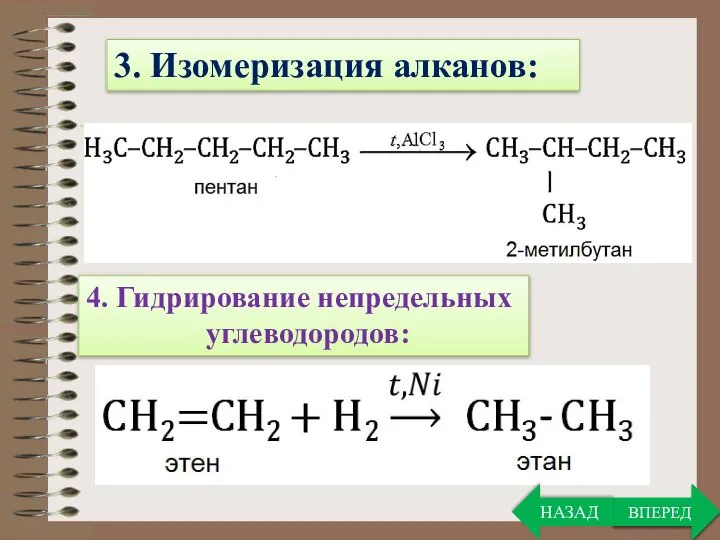
- 5. ВПЕРЕД 3. Изомеризация алканов: 4. Гидрирование непредельных углеводородов: ВПЕРЕД НАЗАД
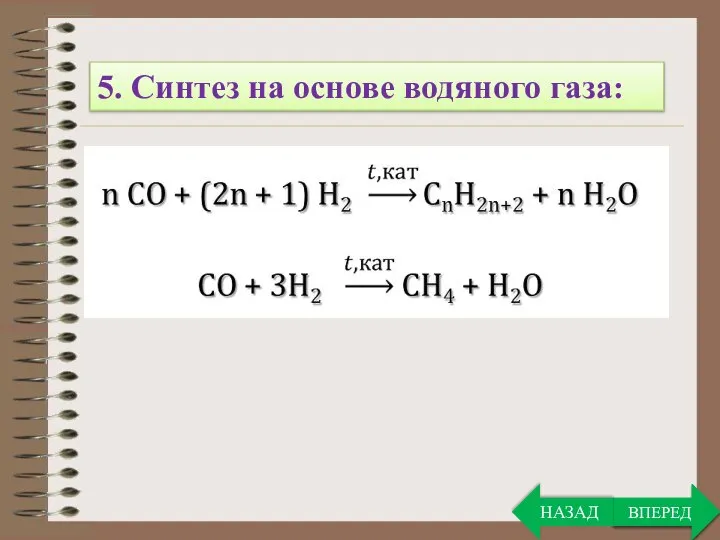
- 6. ВПЕРЕД 5. Синтез на основе водяного газа: ВПЕРЕД НАЗАД
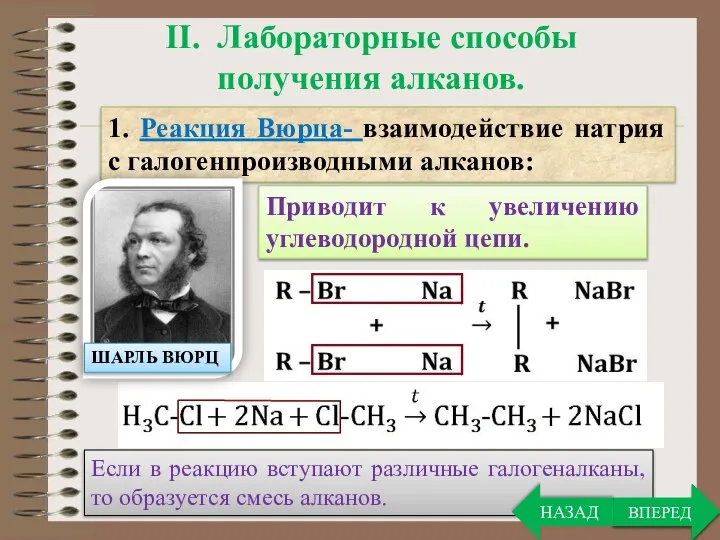
- 7. Если в реакцию вступают различные галогеналканы, то образуется смесь алканов. ВПЕРЕД II. Лабораторные способы получения алканов.
- 8. ВПЕРЕД 2. Реакция Дюма - сплавление солей карбоновых кислот со щелочью.
- 9. 3. Синтез Кольбе - электролиз солей карбоновых кислот. 4. Гидролиз карбидов металлов. Al4C3 + 12H2O →
- 10. Применение АЛКАНОВ ВПЕРЕД НАЗАД
- 11. Применение алканов Газообразные АЛКАНЫ (метан и пpопан-бутановая смесь) используются в качестве ценного ТОПЛИВА. Жидкие УГЛЕВОДОPОДЫ составляют
- 12. тетрахлорметан – растворитель, для гашения пламени; фтор-, хлор- углеводороды (фреоны) – хладагенты, производство аэрозолей, производство тефлона.
- 13. ВПЕРЕД Метан– получение сажи для типографской краски, резины, синтез водорода, производство ацетилена, формальдегида. Применение алканов ВПЕРЕД
- 14. ВПЕРЕД Нахождение в природе АЛКАНОВ ВПЕРЕД НАЗАД
- 15. ВПЕРЕД Нахождение в природе Основные источники алканов – нефть и природный газ. Метан составляет основную массу
- 16. ВПЕРЕД ВПЕРЕД НАЗАД
- 17. В природе широко распространены также газовые гидраты алканов, в основном метана, они залегают в осадочных породах
- 18. Твердые алканы встречаются в природе в виде залежей горного воска – озокерита, в восковых покрытиях листьев,
- 19. АЛКЕНЫ Получение и применение алканов ВПЕРЕД НАЗАД
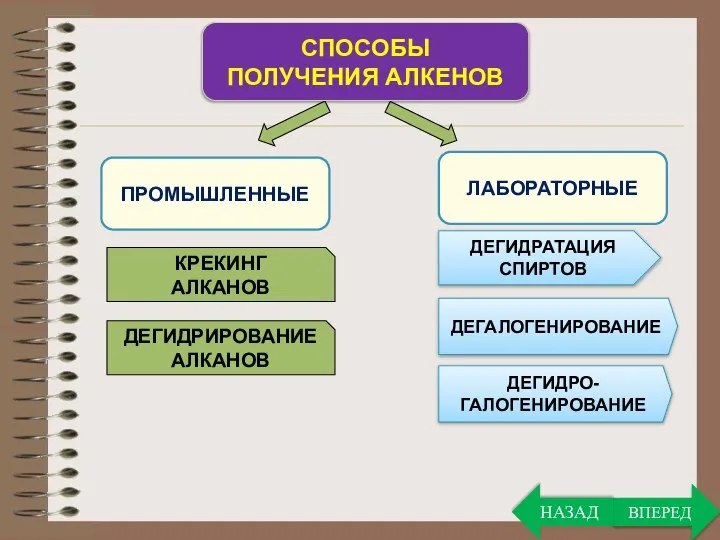
- 20. ПРОМЫШЛЕННЫЕ СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ ЛАБОРАТОРНЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ДЕГИДРАТАЦИЯ СПИРТОВ ДЕГАЛОГЕНИРОВАНИЕ ДЕГИДРО- ГАЛОГЕНИРОВАНИЕ ВПЕРЕД НАЗАД
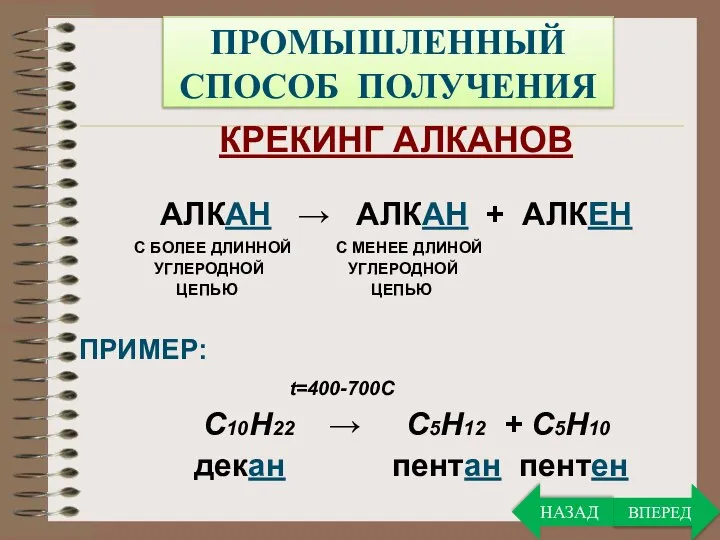
- 21. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ КРЕКИНГ АЛКАНОВ АЛКАН → АЛКАН + АЛКЕН С БОЛЕЕ ДЛИННОЙ С МЕНЕЕ ДЛИНОЙ
- 22. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД ПРИМЕР: Ni, t=500C Н3С - СН3
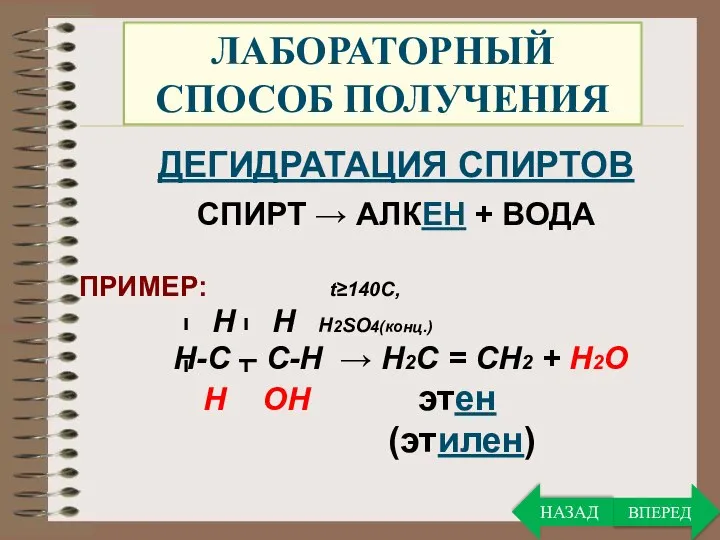
- 23. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА ПРИМЕР: t≥140C, Н Н Н2SO4(конц.) Н-С
- 24. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГАЛОГЕНИРОВАНИЕ ПРИМЕР: t Н2С – СН2 + Zn → Н2С = СН2 +
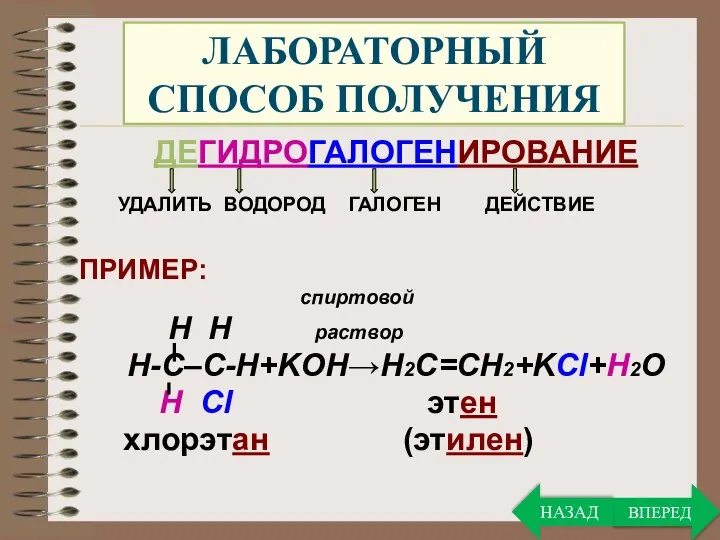
- 25. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ ПРИМЕР: спиртовой H H раствор Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O Н Cl
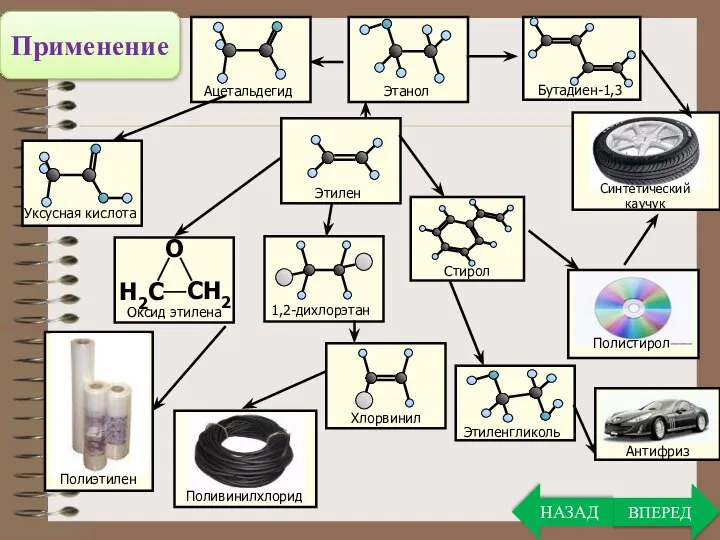
- 26. Применение ВПЕРЕД НАЗАД
- 27. Применение алкенов ВПЕРЕД НАЗАД
- 28. АЛКИНЫ Получение и применение алканов ВПЕРЕД НАЗАД
- 29. Получение АЛКИНОВ 1) В промышленности ацетилен получают высокотемпературным пиролизом метана. 1500ºС 2CH4 → HC≡CH + 3H2
- 30. 4) Алкины можно получить дегидрогалогенированием дигалогенопроизводных парафинов. Атомы галогена при этом могут быть расположены как у
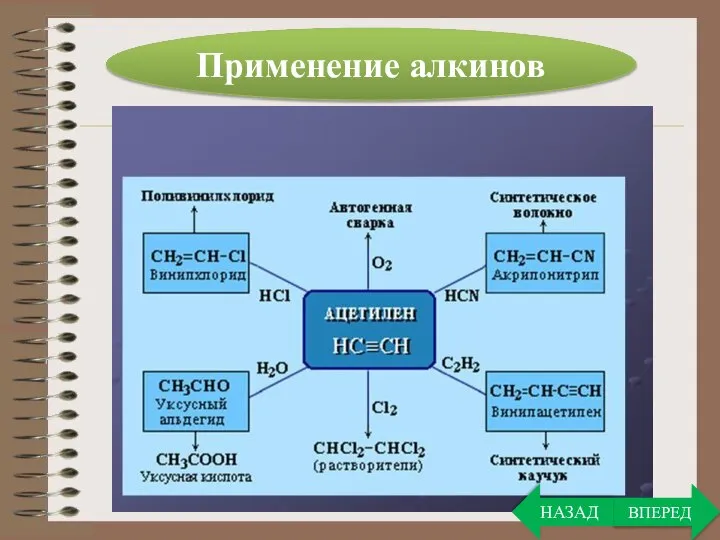
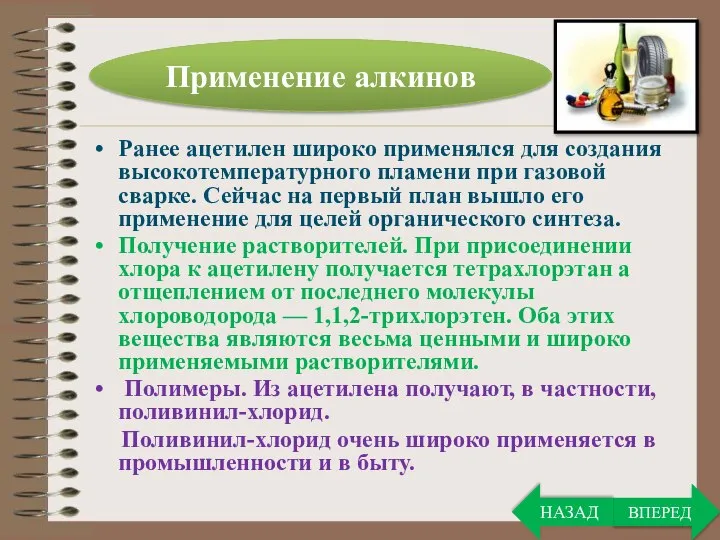
- 31. Применение алкинов ВПЕРЕД НАЗАД
- 32. Ранее ацетилен широко применялся для создания высокотемпературного пламени при газовой сварке. Сейчас на первый план вышло
- 34. Скачать презентацию




















 Изучение процесса замерзания воды
Изучение процесса замерзания воды Газ тәрізді өнімдер бромды сутек
Газ тәрізді өнімдер бромды сутек Виды изомерии. Углеводороды
Виды изомерии. Углеводороды Порядковый номер элемента. Изотопы
Порядковый номер элемента. Изотопы Презентация на тему Типы химических реакций
Презентация на тему Типы химических реакций  Подготовка проб товаров к анализу. Химико-аналитический контроль
Подготовка проб товаров к анализу. Химико-аналитический контроль Отчет по ПП 03.01. Лаборант химического анализа
Отчет по ПП 03.01. Лаборант химического анализа Общие представления об электрохимических технологиях
Общие представления об электрохимических технологиях Влияние метилового спирта на организм человека
Влияние метилового спирта на организм человека Реализация примерной адаптированной основной общеобразовательной программы по предмету Химия
Реализация примерной адаптированной основной общеобразовательной программы по предмету Химия Типы кристаллических структур Автор Могилевская А.Е. Санкт-Петербург. ГБОУ СОШ№535
Типы кристаллических структур Автор Могилевская А.Е. Санкт-Петербург. ГБОУ СОШ№535 Карбонат калия K2CO3
Карбонат калия K2CO3 Распределение электронов в атомах
Распределение электронов в атомах Правила ТБ при работе в кабинете химии. Приёмы обращения с лабораторным оборудованием
Правила ТБ при работе в кабинете химии. Приёмы обращения с лабораторным оборудованием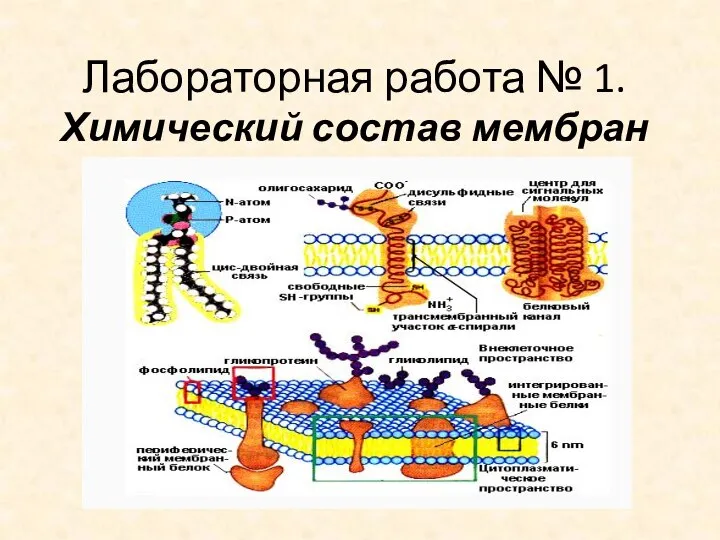 Химический состав мембран. Лабораторная работа № 1
Химический состав мембран. Лабораторная работа № 1 Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов Химическая реакция в потоке в одномерном случае. Уравнение неразрывности
Химическая реакция в потоке в одномерном случае. Уравнение неразрывности Магний для растений
Магний для растений Лабораторное оборудование. Тесты
Лабораторное оборудование. Тесты Простые вещества - неметаллы
Простые вещества - неметаллы Содержание варианта ЕГЭ
Содержание варианта ЕГЭ Основные классы неорганических соединений. Гидроксиды
Основные классы неорганических соединений. Гидроксиды Простые и сложные вещества (8 класс)
Простые и сложные вещества (8 класс) Простые вещества – металлы. Общие физические свойства металлов
Простые вещества – металлы. Общие физические свойства металлов Кислоты с металлами
Кислоты с металлами Побочная подгруппа VII группы периодической системы
Побочная подгруппа VII группы периодической системы Спирты. Понятие о спиртах
Спирты. Понятие о спиртах Презентация на тему Строение атома
Презентация на тему Строение атома