Содержание
- 2. АЛЮМИНИЙ. Нахождение в природе Алюмосиликаты: Глина – Al2O3*nSiO2*mH2O Бокситы – Al2O3*nH2O
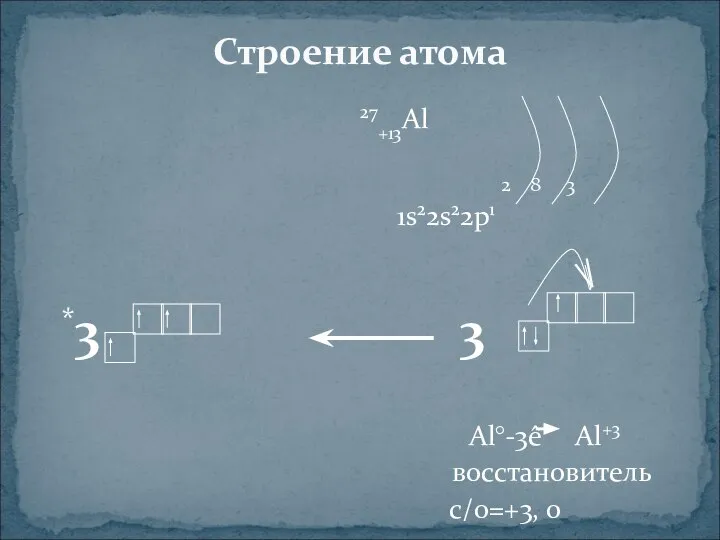
- 3. 27+13Al 2 8 3 1s22s22p1 *3 3 Al°-3ê Al+3 восстановитель с/о=+3, 0 Строение атома
- 4. ФИЗИЧЕСКИЕ СВОЙСТВА Al-серебристо-белый металл Мягкий, пластичный (легко вытягивается в проволоку и раскатывается в листы), легкий (плотность
- 5. ХИМИЧЕСКИЕ СВОЙСТВА Al – активный металл. На воздухе всегда покрыт пленкой Al2O3. Поэтому при обычных условиях
- 6. ВЗАИМОДЕЙСТВИЕ С ПРОСТЫМИ ВЕЩЕСТВАМИ При обычных условиях Взаимодействие с кислородом: 4Al+ 3O2 =2Al2O3 +Q Взаимодействие с
- 7. Взаимодействие с водой (очищенный от оксидной пленки) 2 Al +6H2O=2Al(OH)3 +3H2 Взаимодействует с растворами кислот 2Al
- 8. Алюминий при обычных условиях не взаимодействует с концентрированными H2SO4и HNO3 (он пассивируется),но при нагревании реакция возможна
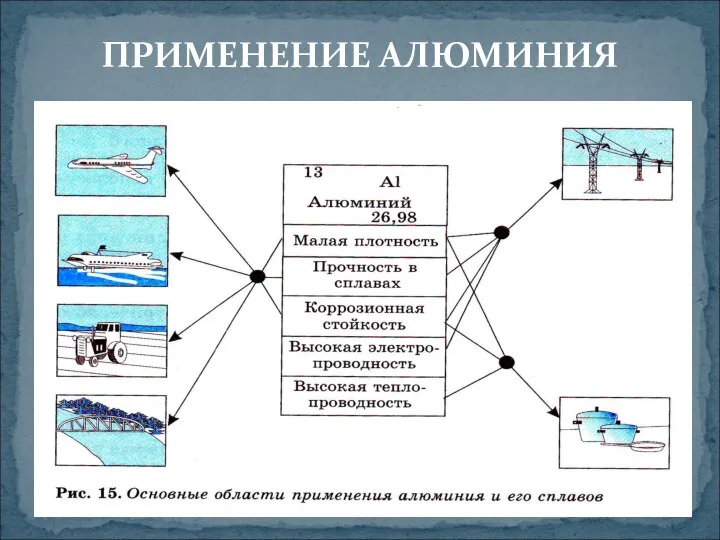
- 9. ПРИМЕНЕНИЕ АЛЮМИНИЯ
- 11. Скачать презентацию






 Алкины
Алкины Презентация на тему Кристаллическая решетка
Презентация на тему Кристаллическая решетка  Фосфорные удобрения
Фосфорные удобрения Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Substanță chimică
Substanță chimică Уравнение материального баланса технологического процесса. (Лекция 3)
Уравнение материального баланса технологического процесса. (Лекция 3) Ориентация полимеров
Ориентация полимеров Язык естествознания. Химия
Язык естествознания. Химия Коштовне каміння
Коштовне каміння Буферлік жүйелер мен ерітінділер туралы түсініктер, олардың құрамы және жіктелуі
Буферлік жүйелер мен ерітінділер туралы түсініктер, олардың құрамы және жіктелуі Скорость химической реакции
Скорость химической реакции Составитель: Денисова В.Г.
Составитель: Денисова В.Г. Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Метилэтилкетон. Его применение и процесс получения
Метилэтилкетон. Его применение и процесс получения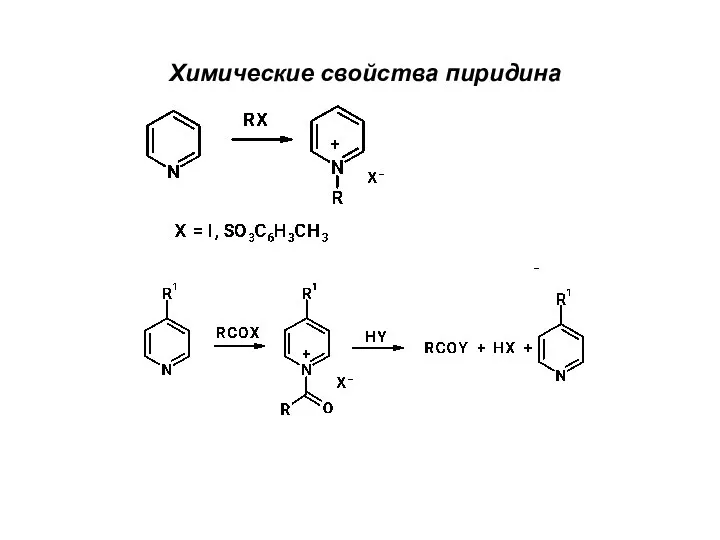 Химические свойства пиридина
Химические свойства пиридина Основные классы неорганических соединений. Общие формулы оксидов, оснований, кислот, солей
Основные классы неорганических соединений. Общие формулы оксидов, оснований, кислот, солей Карбоновые кислоты
Карбоновые кислоты Химический состав клетки
Химический состав клетки Правила ТБ при работе в кабинете химии. Приёмы обращения с лабораторным оборудованием
Правила ТБ при работе в кабинете химии. Приёмы обращения с лабораторным оборудованием Электролитическая диссоциация
Электролитическая диссоциация Характеристика химических элементов IV А группа. Углерод
Характеристика химических элементов IV А группа. Углерод Химическое равновесие и способы его смещения. Принцип Ле Шателье. 9 класс
Химическое равновесие и способы его смещения. Принцип Ле Шателье. 9 класс Активизация познавательной деятельности на уроках химии при работе с МГП (малыми графическими пособиями)
Активизация познавательной деятельности на уроках химии при работе с МГП (малыми графическими пособиями) Тренажер. Типы химических реакций
Тренажер. Типы химических реакций Галогены
Галогены Химическая связь
Химическая связь Неметаллы. Обобщение и систематизация знаний
Неметаллы. Обобщение и систематизация знаний Графит. 9 класс
Графит. 9 класс