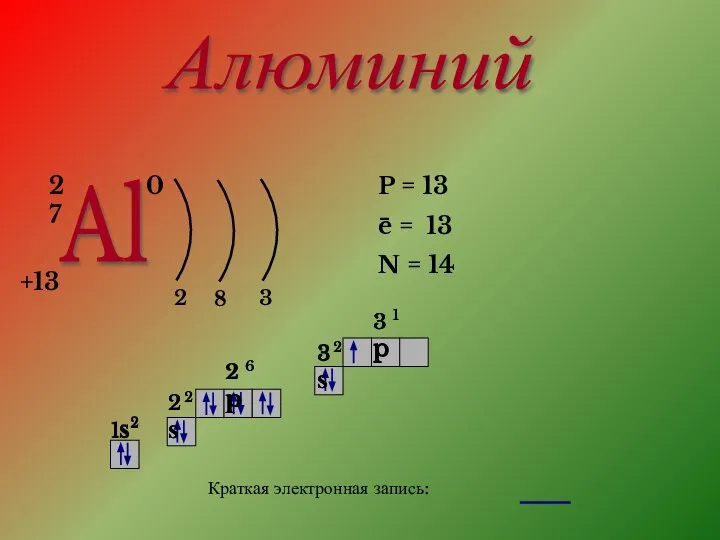
Слайд 2Алюминий
Al
27
+13
0
2
8
3
P = 13
e = 13
N = 14
−
Краткая электронная запись:
Слайд 3Физические свойства
плавления 660°С. Пластичен, легко Чистый алюминий — серебристо-белый легкий металл,вытягивается в

проволоку и раскатывается в листы и фольгу. Является хорошим проводником электричества и тепла (после серебра и меди).
Сплавы алюминия с различными металлами обладают высокой прочностью и легкостью.
Слайд 4Химические свойства
2Al
+3O2
Al2O3
+3Cl2
2AlCl3
+3S
Al2S3
+6HCl
2AlCl3 + 3H2
+3CuSO4
Al2(SO4)3 + 3Cu

Слайд 5Химические свойства
Является амфотерным элементом: взаимодействует с кислотами и со щелочами.
2Al +

6HCl = 2AlCl3 + 3H2
2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2
Оксид и гидроксид алюминия также обладают амфотерными свойствами:
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Al2O3 + 2NaOH = 2NaAlO2 + H2O
2Al(OH)3 + 6HCl = 2AlCl3 + 6H2O
Al(OH)3 + NaOH = NaAlO2 + 2H2O
Слайд 6ПОЛУЧЕНИЕ
Впервые алюминий был получен в 1821 г. в Германии химиком, которого звали Ф. Веллер.

Он предложил получать алюминий путем его восстановления из хлорида алюминия. Спустя несколько десятилетий в 1854 г. Сент-Клер Девиль, французский ученый, изобрел электрохимический способ получения алюминия, который был востребован вплоть до конца XIX в. Сменил электрохимический способ метод электролиза, предложенный химиком Холлом в 1886 г. и применяемый по сей день.
Слайд 7ПРИМЕНЕНИЕ
Основным преимуществом использования алюминиевых сплавов является их малая плотность. Масса кузова из

алюминиевого сплава может быть приблизительно в два раза легче эквивалентного стального кузова с такими же характеристиками по жесткости и пассивной безопасности. Алюминий меньше коррозирует, так как защищен поверхностной окисной пленкой.






 Презентация на тему Воздух. Кислород. Горение
Презентация на тему Воздух. Кислород. Горение  Альдегиды. Строение молекул
Альдегиды. Строение молекул 8_ANIONY_2_3_angr
8_ANIONY_2_3_angr Кислоты основания и соли как электролиты
Кислоты основания и соли как электролиты Реакции по направлению процесса
Реакции по направлению процесса Характеристика щелочных металлов (9 класс)
Характеристика щелочных металлов (9 класс) Калий. Общая информация
Калий. Общая информация Алгебраический метод решения задач В-9 – элемент решения задач С4
Алгебраический метод решения задач В-9 – элемент решения задач С4 Применение серы, хлора, углерода
Применение серы, хлора, углерода Ocena zawartości mikotoksyn w wybranych produktach spożywczych
Ocena zawartości mikotoksyn w wybranych produktach spożywczych Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19 Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса
Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса Квест Секретная лаборатория. Первоначальные химические понятия. 8 класс
Квест Секретная лаборатория. Первоначальные химические понятия. 8 класс Растворы электролитов
Растворы электролитов Аналитический обзор по теме Процесс разложения аммиака
Аналитический обзор по теме Процесс разложения аммиака О некоторых удивительных удивительных свойствах свойствах веществ
О некоторых удивительных удивительных свойствах свойствах веществ Интерактивный плакат Алканы
Интерактивный плакат Алканы Новейшие достижения в области высокомолекулярных соединений
Новейшие достижения в области высокомолекулярных соединений Ð¥ÐÐÐЧÐСÐÐÐ Ð ÐÐÐÐÐÐСÐÐ1
Ð¥ÐÐÐЧÐСÐÐÐ Ð ÐÐÐÐÐÐСÐÐ1 prezentatsia_lektsia_1_LF_Rastvory_Kolligativnye_svoi_774_stva_rastvorov_Osmos
prezentatsia_lektsia_1_LF_Rastvory_Kolligativnye_svoi_774_stva_rastvorov_Osmos Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Протолитические буферные системы. Буферные системы организма, их взаимодействие
Протолитические буферные системы. Буферные системы организма, их взаимодействие Использование информационных технологий на уроках химии Радченко Н.В. учитель химии МОУ ПСОШ №3
Использование информационных технологий на уроках химии Радченко Н.В. учитель химии МОУ ПСОШ №3 Методика измерений массовой концентрации ионов аммония в природных и сточных водах фотометрическим методом с реактивом Несслера
Методика измерений массовой концентрации ионов аммония в природных и сточных водах фотометрическим методом с реактивом Несслера Красители для волос. Первая группа
Красители для волос. Первая группа Ионные уравнения
Ионные уравнения Презентация на тему Основные классы неорганических соединений
Презентация на тему Основные классы неорганических соединений  Фосфорні добрива. Технології збагачення фосфоровмісної сировини
Фосфорні добрива. Технології збагачення фосфоровмісної сировини