Содержание
- 2. План Методы качественного анализа Понятие систематического и дробного хода анализа
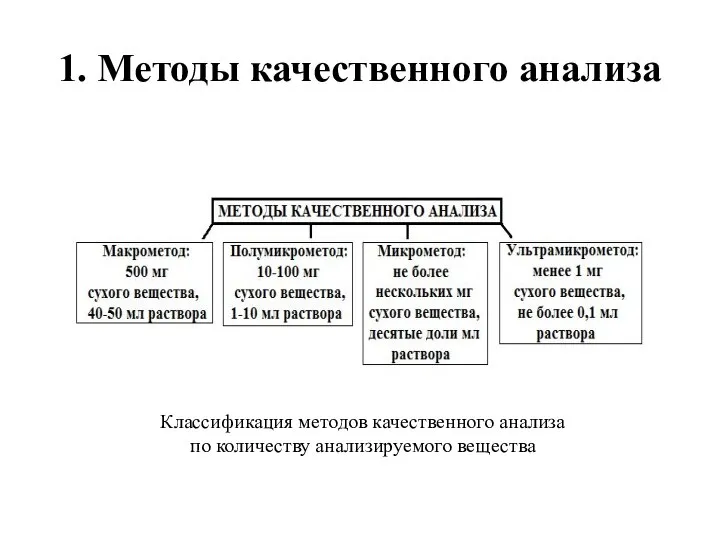
- 3. 1. Методы качественного анализа Классификация методов качественного анализа по количеству анализируемого вещества
- 4. 1. Методы качественного анализа В качественном химическом анализе можно проводить аналитические реакции «сухим» и «мокрым» способами
- 5. 1. Методы качественного анализа «сухой» способ 1) окрашивание пламени Тест на окраску пламени
- 6. 1. Методы качественного анализа «сухой» способ 2) образование окрашенных перлов К реакциям, проводимым «сухим» способом, относится
- 7. Получение перла Изогнуть платиновую проволоку в петельку диаметром 0,5…1 мм (в случае фосфорной соли – продолговатую)
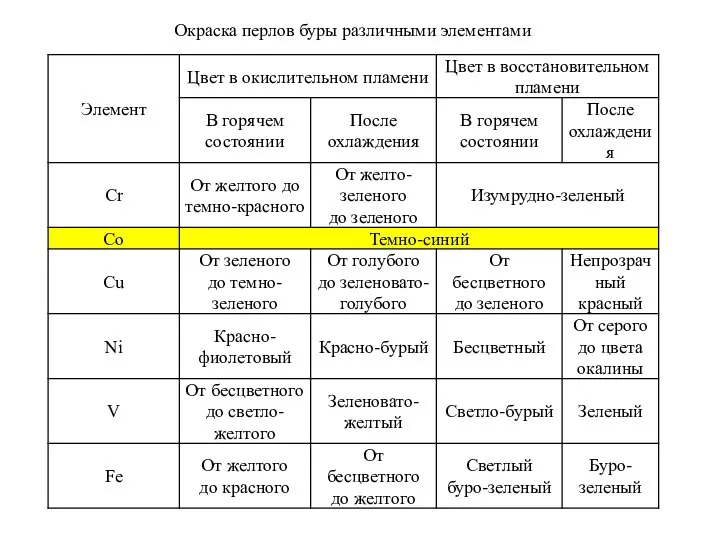
- 8. Окраска перлов буры различными элементами
- 9. Окраска перлов буры Na2B4O7 · 10 H2O = 2 NaBO2 + B2O3 + 10 H2O B2O3
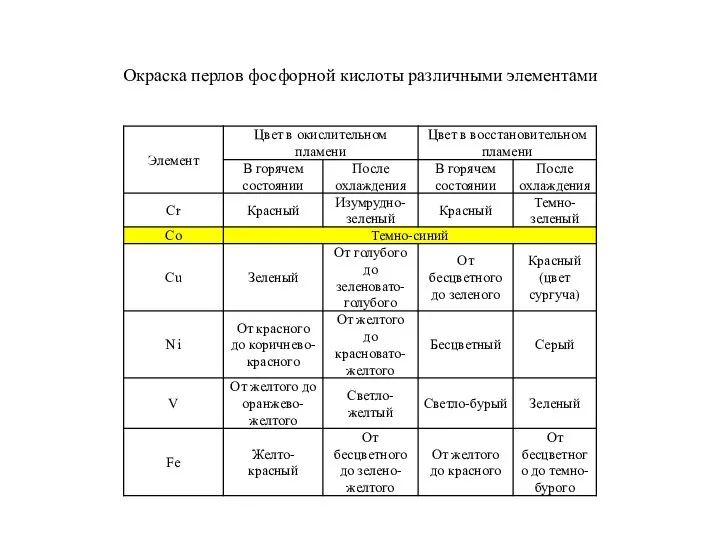
- 10. Окраска перлов фосфорной кислоты различными элементами
- 11. 1. Методы качественного анализа «сухой» способ 3) растирание (В. М. Флавицкий, 1898 г) FeCl3 NH4CNS Fe(SCN)3
- 12. 1. Методы качественного анализа «мокрый» способ капельный анализ (Н. А. Тананаев, 1933) Капельный анализ – метод
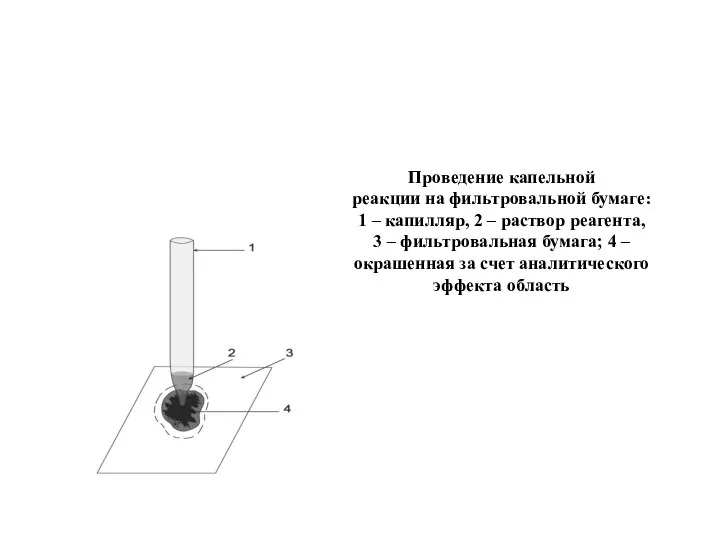
- 13. Проведение капельной реакции на фильтровальной бумаге: 1 – капилляр, 2 – раствор реагента, 3 – фильтровальная
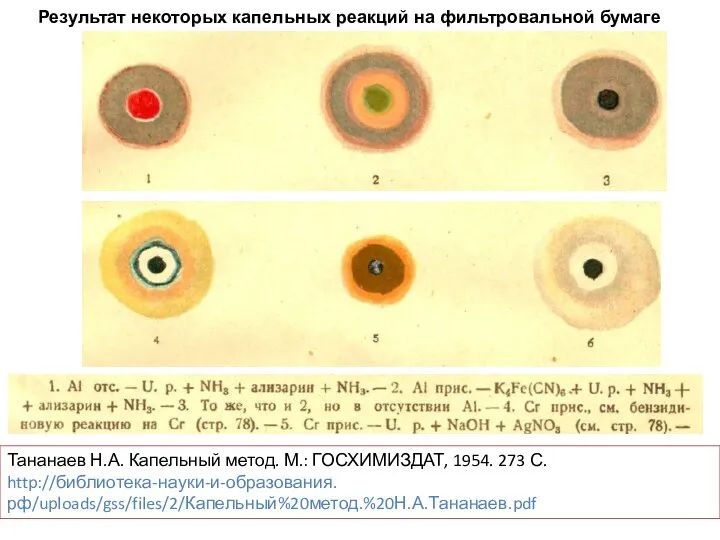
- 14. Тананаев Н.А. Капельный метод. М.: ГОСХИМИЗДАТ, 1954. 273 С. http://библиотека-науки-и-образования.рф/uploads/gss/files/2/Капельный%20метод.%20Н.А.Тананаев.pdf Результат некоторых капельных реакций на фильтровальной
- 15. 2. Понятие систематического и дробного хода анализа Дробный ход анализа – обнаружение ионов с помощью специфических
- 16. Систематический ход анализа – определенный порядок (последовательность) ведения аналитических реакций, при котором каждый последующий ион открывают
- 17. В аналитической химии для удобства проведения качественного анализа катионы и анионы делят на аналитические группы. В
- 18. Сероводородная классификация Сульфидная классификация разработана наиболее подробно, но применяется всё реже из-за токсичности H2S и длительности
- 19. Аммиачно-фосфатная классификация катионов Основана на растворимости фосфатов в воде, NH3, уксусной кислоте
- 20. Кислотно-основная классификация Основана на различии в свойствах их гидроксидов (основные или амфотерные, растворимые или не растворимые
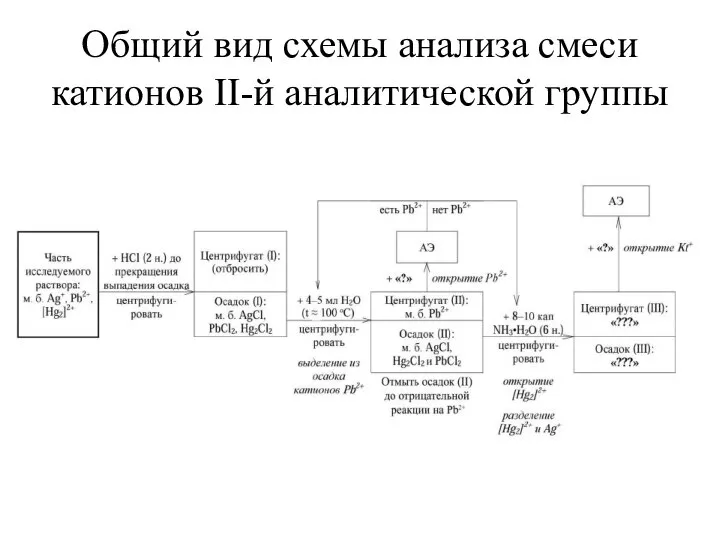
- 21. Общий вид схемы анализа смеси катионов II-й аналитической группы
- 23. Скачать презентацию














 Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1)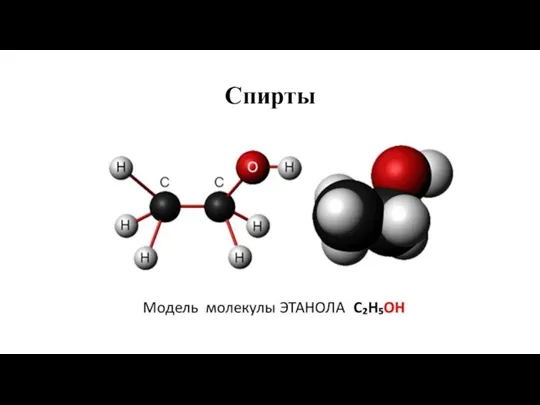 Спирты
Спирты Лабораторное оборудование. Тесты
Лабораторное оборудование. Тесты Вода - растворитель
Вода - растворитель Алмазы
Алмазы Циклоалканы. Номенклатура и строение
Циклоалканы. Номенклатура и строение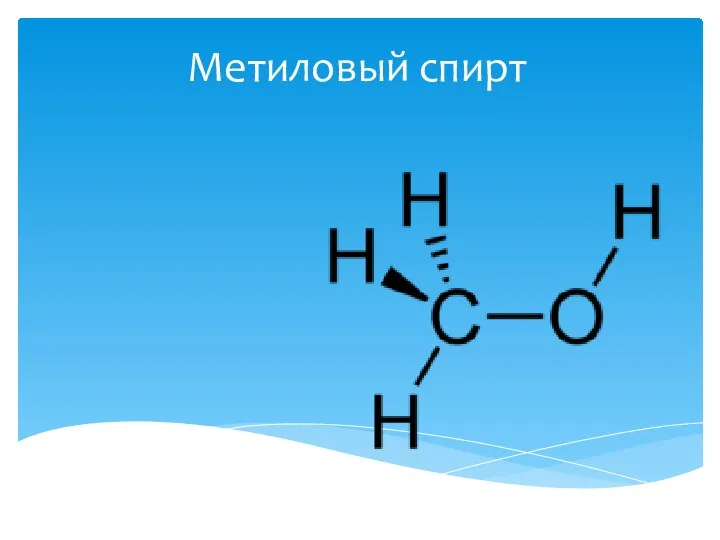 Метиловый спирт
Метиловый спирт Классы неорганических соединений
Классы неорганических соединений Квантовая химия
Квантовая химия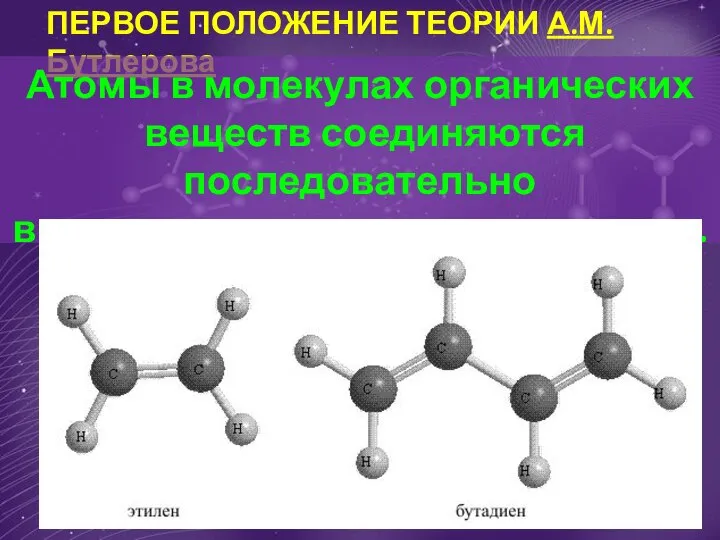 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Влияние растворителей на скорость органических реакций. (Лекция 10)
Влияние растворителей на скорость органических реакций. (Лекция 10) Лекция_Химическая_кинетика_и_катализ
Лекция_Химическая_кинетика_и_катализ Основания. Простые и сложные ионы
Основания. Простые и сложные ионы Спирты. Классификация, номенклатура, изомерия, получение и применение. 10 класс
Спирты. Классификация, номенклатура, изомерия, получение и применение. 10 класс Раздел 1
Раздел 1 Решение задач. Подготовка к контрольной работе по химии
Решение задач. Подготовка к контрольной работе по химии Классификация аминокислот в зависимости от природы радикалов
Классификация аминокислот в зависимости от природы радикалов Metals Properties and compounds
Metals Properties and compounds Получение пластмасс
Получение пластмасс Использование информационных технологий в образовательном процессе на примере химии
Использование информационных технологий в образовательном процессе на примере химии Химические реакции
Химические реакции Кислотно-основные равновесия
Кислотно-основные равновесия Budowa pasmowa ciał stałych
Budowa pasmowa ciał stałych Изготовление индикаторной бумаги
Изготовление индикаторной бумаги Кислоты. Состав кислот, их классификация и физические свойства, 8 класс
Кислоты. Состав кислот, их классификация и физические свойства, 8 класс Распространение ПВО в приземном слое атмосферы
Распространение ПВО в приземном слое атмосферы Простые вещества – неметаллы. Получение и химические свойства неметаллов
Простые вещества – неметаллы. Получение и химические свойства неметаллов Электролитическая диссоциация
Электролитическая диссоциация