Содержание
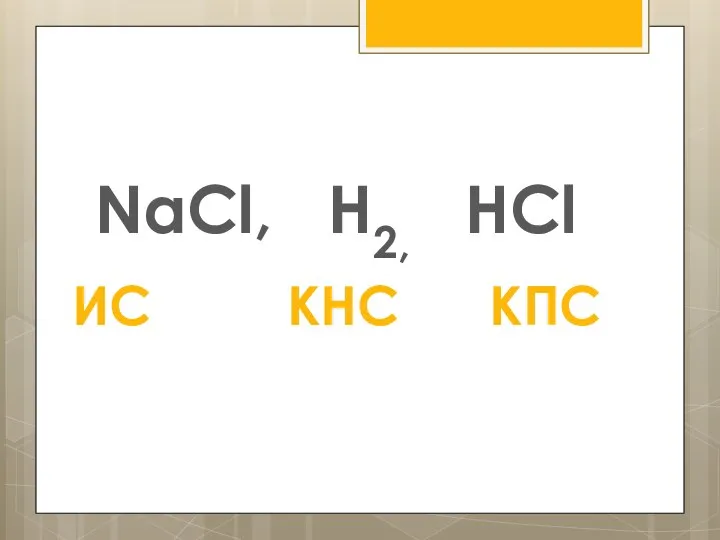
- 2. NaCl, Н2, HCl ИС КНС КПС
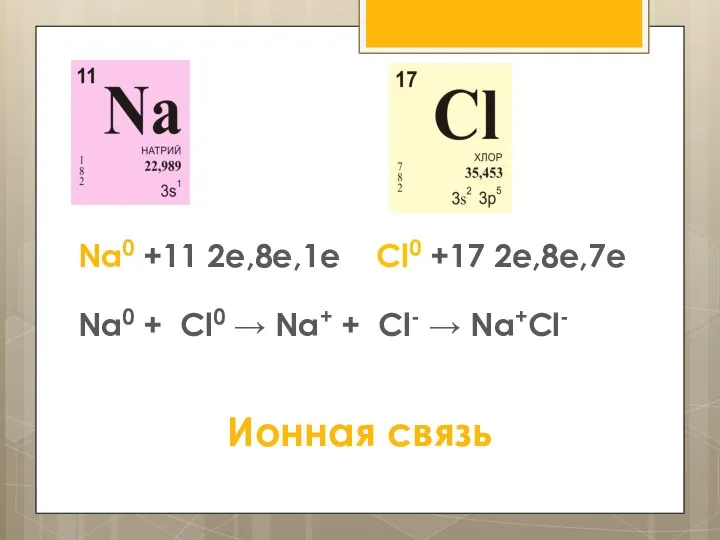
- 3. Na0 +11 2е,8е,1е Cl0 +17 2e,8e,7e Na0 + Cl0 → Na+ + Cl- → Na+Cl- Ионная
- 4. Н + Н → Н Н Может ли быть смещена общая пара к какому-либо из атомов
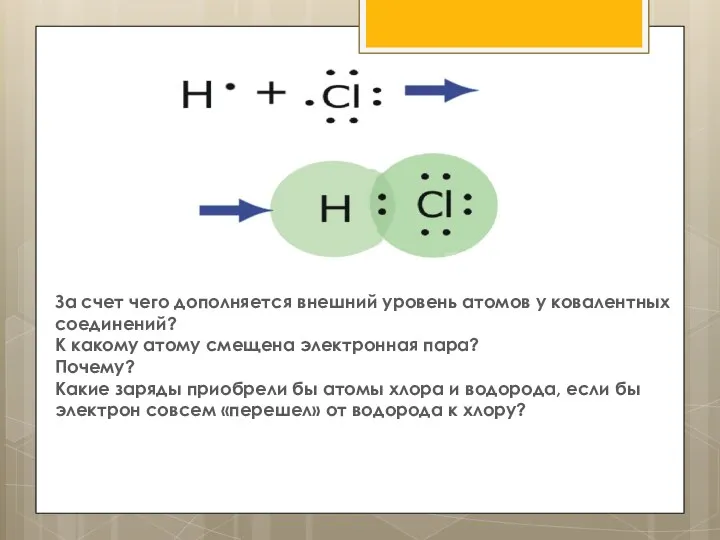
- 5. За счет чего дополняется внешний уровень атомов у ковалентных соединений? К какому атому смещена электронная пара?
- 6. Сравним соединения NaCl, Н2, HCl У каких соединений будут наблюдаться заряды?
- 7. Степени окисления химических элементов Учитель химии ГБОУ СОШ№546 Светлана Васильевна Носик
- 8. Цель урока на основе знаний об электронном строении атомов химических элементов и химической связи сформировать знания
- 9. С.О. - условный заряд атома в химическом соединении, вычисленный из предположения, что все связи ионные Степень
- 10. Определить с.о. в соединениях: CaH2; N2O5; O2F2 ??????????
- 11. Задание 1. Используя ПС или ряд ЭО на последнем форзаце учебника, обозначьте на валентном штрихе направление
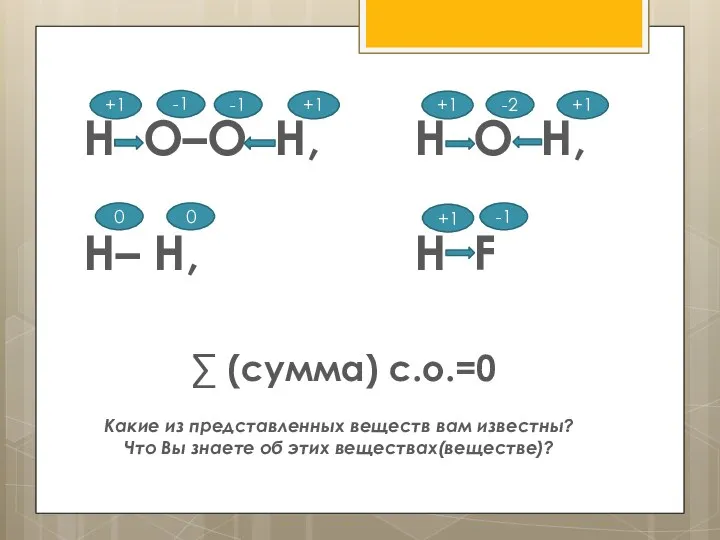
- 12. Н О–О Н, Н О Н, Н– Н, Н F +1 -1 ∑ (сумма) с.о.=0 Какие
- 13. ВОДА
- 14. Перекись водорода
- 15. Правила определения степеней окисления 1.В простом веществе степень окисления атомов равна - 0. 2. Сумма степеней
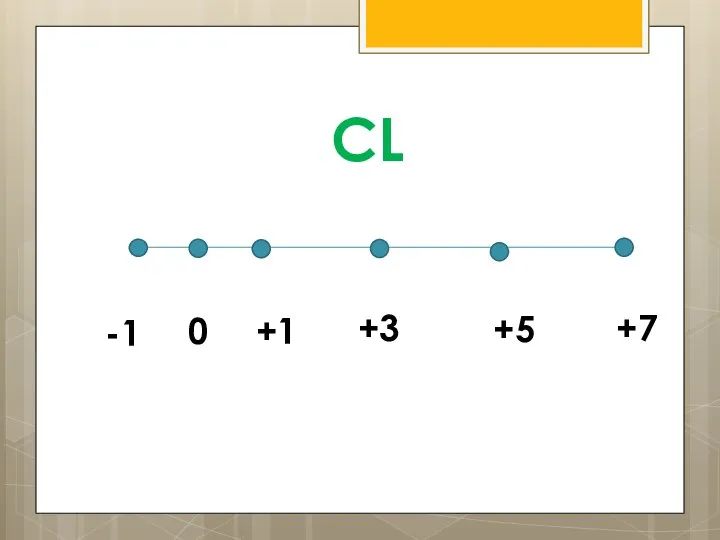
- 16. Задание 2 Определите возможные С.О. хлора
- 17. -1 0 +3 +5 +7 CL +1
- 18. Вернемся к нашему заданию Используя алгоритм определения СО и математические знания определите СО химических элементов в
- 19. Проверяем!
- 20. Задание№4. Определи степени окисления атомов элементов, входящих в состав первых трех веществ: AlCl3, H2Se, SiF4, AlN,
- 22. Скачать презентацию














 Производство серной кислоты
Производство серной кислоты Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Вода. Растворы
Вода. Растворы Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Соли
Соли Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Металлы побочных подгрупп
Металлы побочных подгрупп Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Химический элемент кислород
Химический элемент кислород Химическая география чудес природы
Химическая география чудес природы Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1) Презентация по Химии "Схема получения моноизотопного кремния"
Презентация по Химии "Схема получения моноизотопного кремния"  Посвящение в химики
Посвящение в химики Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты)
Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты) Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Общая характеристика оксидов
Общая характеристика оксидов Серная кислота
Серная кислота Основные понятия химии
Основные понятия химии Диссоциация веществ
Диссоциация веществ Химическая связь и ее типы
Химическая связь и ее типы Соли. Химические свойства
Соли. Химические свойства Соль. Добыча соли
Соль. Добыча соли Металлы. Атомы металлов
Металлы. Атомы металлов Природные источники углеводорода
Природные источники углеводорода Кислоты. Кислоты, вокруг нас
Кислоты. Кислоты, вокруг нас