Содержание
- 2. Белки сложные полимерные вещества, построенные из остатков аминокислот Аминокислоты -полифункциональные соединения, содержащие одновременно амино- и карбоксильную
- 3. NH2-CH2-COOH 2-аминоэтановая кислота α-аминоуксусная кислота глицин СН3-СН-СООН NH2 2-аминопропановая кислота α-аминопропионовая кислота аланин NH2-CH2CH2-COOH 3-аминопропановая кислота
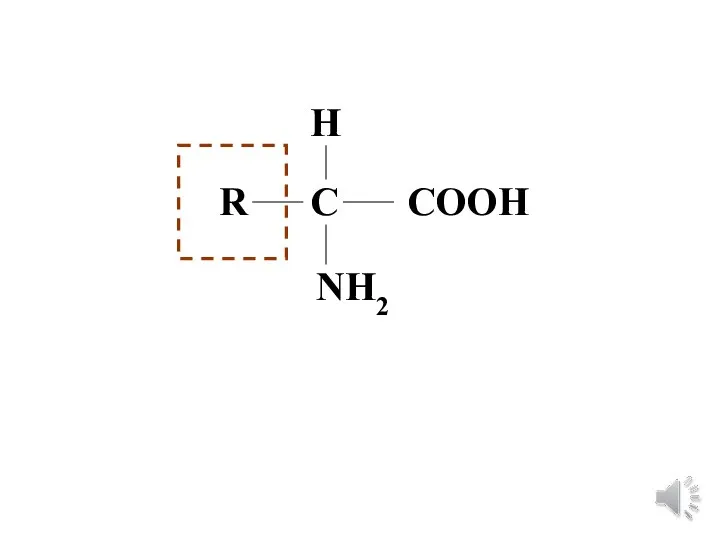
- 4. R C H NH2 COOH
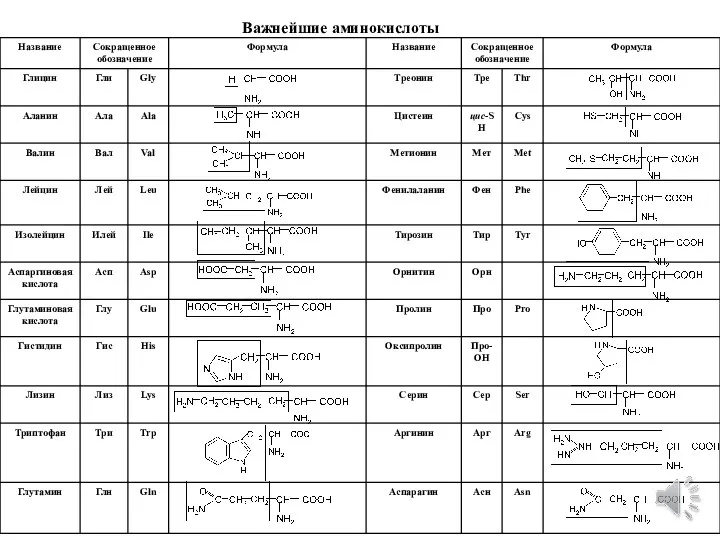
- 5. Важнейшие аминокислоты
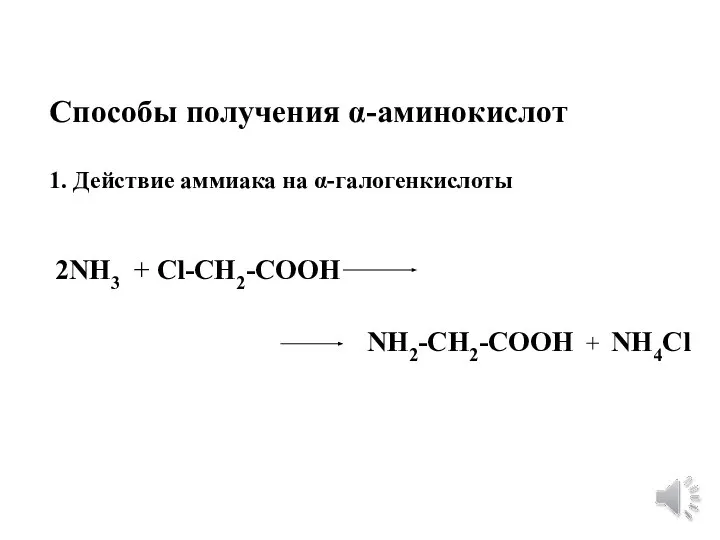
- 6. Способы получения α-аминокислот 1. Действие аммиака на α-галогенкислоты 2NH3 + Cl-CH2-COOH NH2-CH2-COOH + NH4Cl
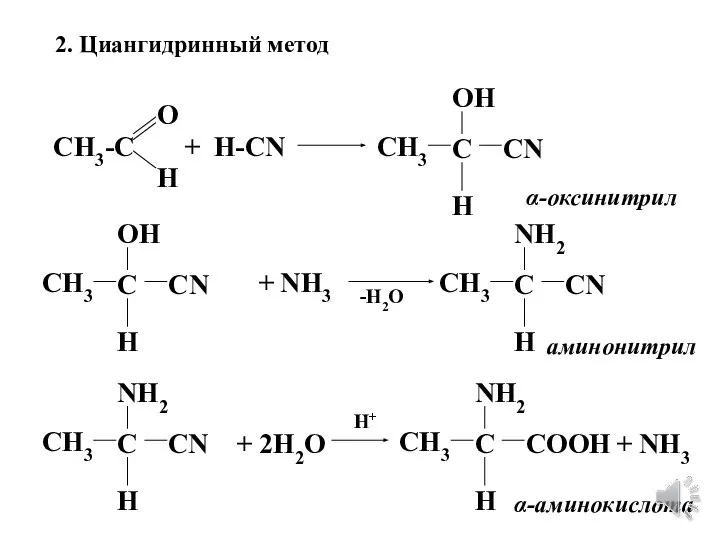
- 7. 2. Циангидринный метод CH3-C O H + H-CN CH3 OH H C CN α-оксинитрил CH3 OH
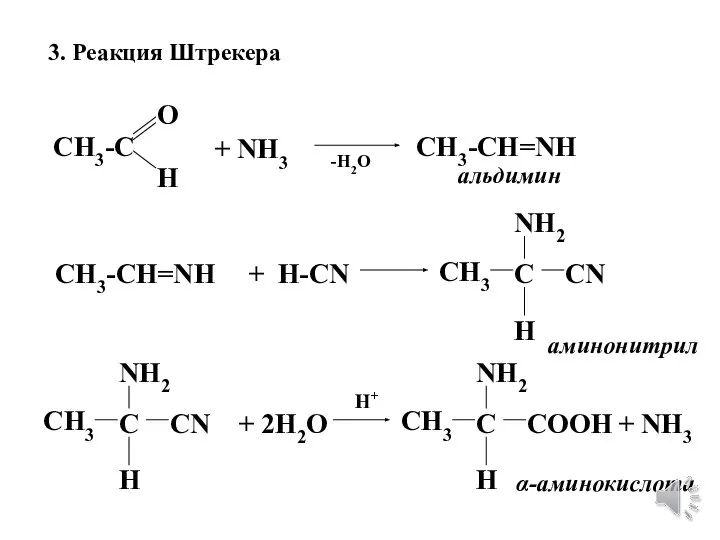
- 8. 3. Реакция Штрекера CH3-C O H + NH3 СH3-CH=NH СH3-CH=NH + H-CN CH3 NH2 H C
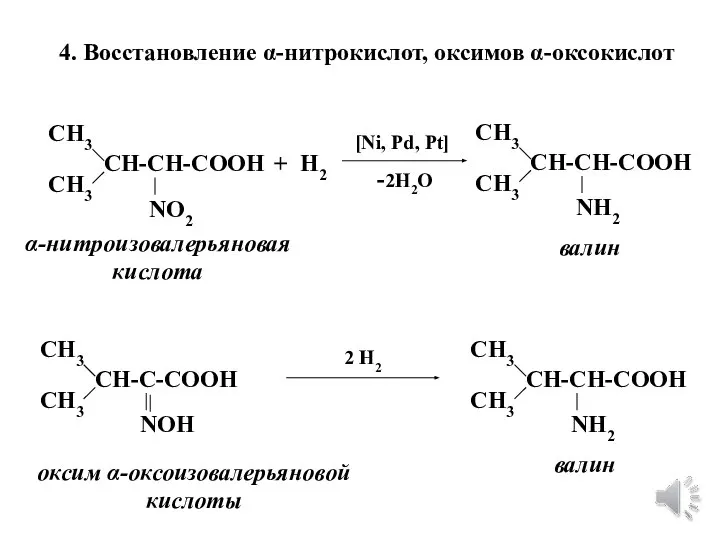
- 9. 4. Восстановление α-нитрокислот, оксимов α-оксокислот СН3 СН3 СН-СН-СООН + Н2 [Ni, Pd, Pt] -2H2O NO2 СН3
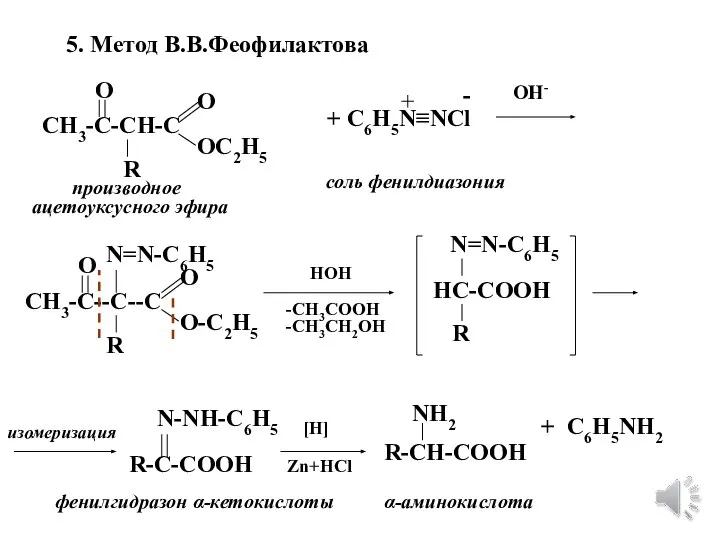
- 10. 5. Метод В.В.Феофилактова СН3-С-СН-С R O O OC2H5 + C6H5N≡NCl производное соль фенилдиазония + - ОН-
- 11. 6. Микробиологический синтез основан на гидролизе белков и последующем разделением смеси.
- 12. Физические свойства α-аминокислот - бесцветные кристаллические вещества; - легко растворимы в воде; - многие обладают сладким
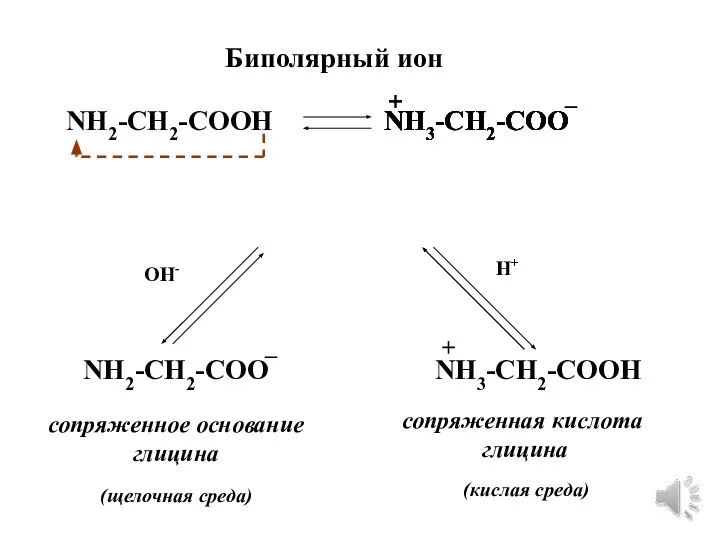
- 13. Биполярный ион NH2-CH2-COOH NH3-CH2-COO + _ NH3-CH2-COO + NH2-CH2-COO NH3-CH2-COOH + _ сопряженное основание глицина (щелочная
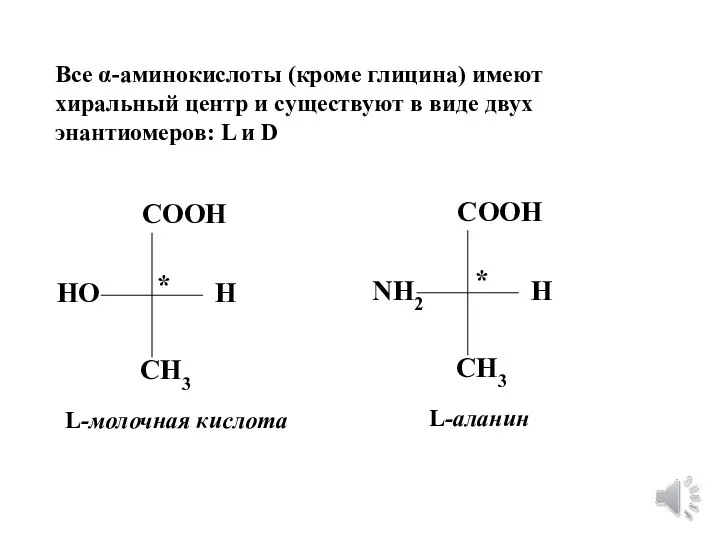
- 14. Все α-аминокислоты (кроме глицина) имеют хиральный центр и существуют в виде двух энантиомеров: L и D
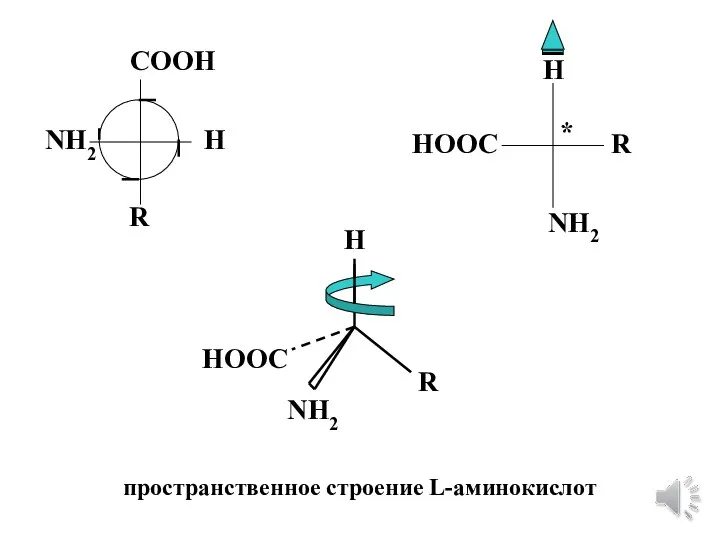
- 15. COOH H R NH2 НООC H R NH2 * H R NH2 НООC пространственное строение L-аминокислот
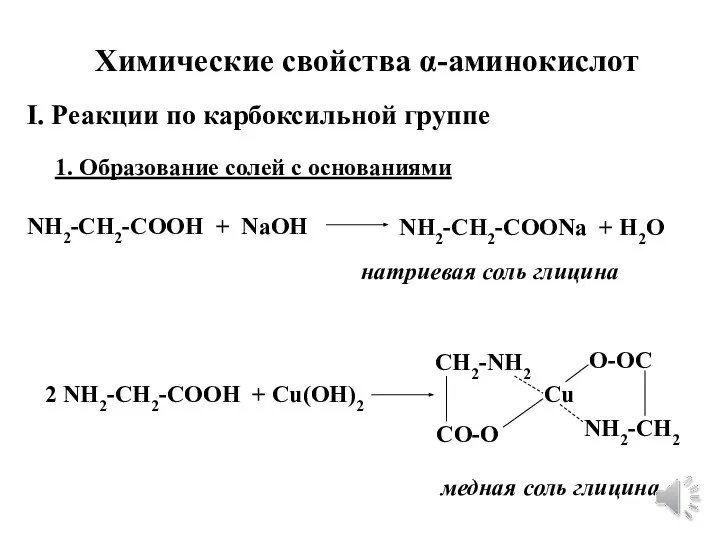
- 16. Химические свойства α-аминокислот I. Реакции по карбоксильной группе 1. Образование солей с основаниями NH2-CH2-COOH + NaOH
- 17. 2. Образование эфиров (защита карбоксильной группы) NH2-CH2-COOH + CH3-CH2-OH HCl -H2O Cl-[NH3-CH2-COOCH2CH3] NaOH -NaCl -H2O NH2-CH2-COOCH2CH3
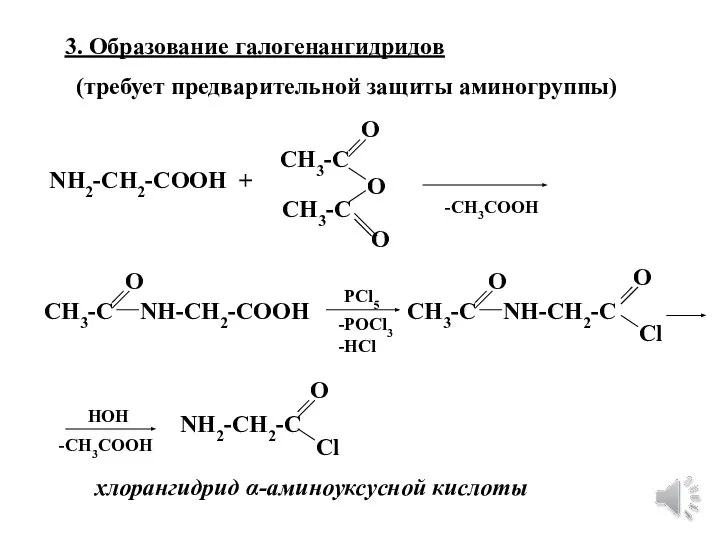
- 18. 3. Образование галогенангидридов (требует предварительной защиты аминогруппы) NH2-CH2-COOH + CH3-C CH3-C О О О -СН3СООН CH3-C
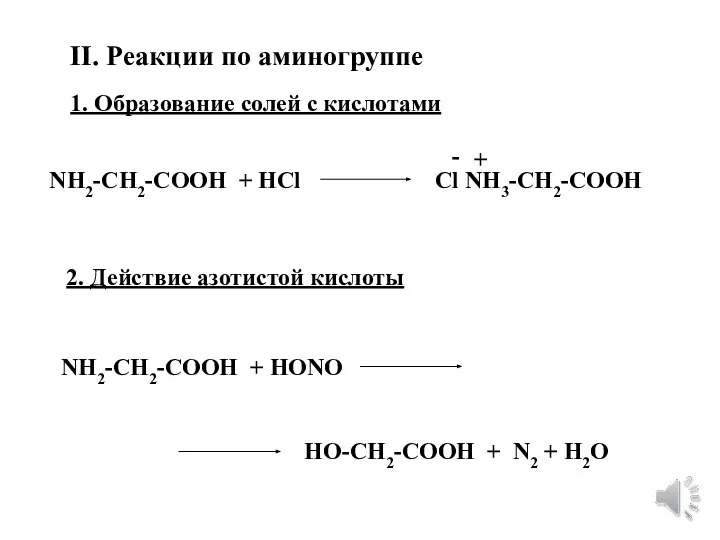
- 19. II. Реакции по аминогруппе 1. Образование солей с кислотами NH2-CH2-COOH + HCl Cl NH3-CH2-COOH + -
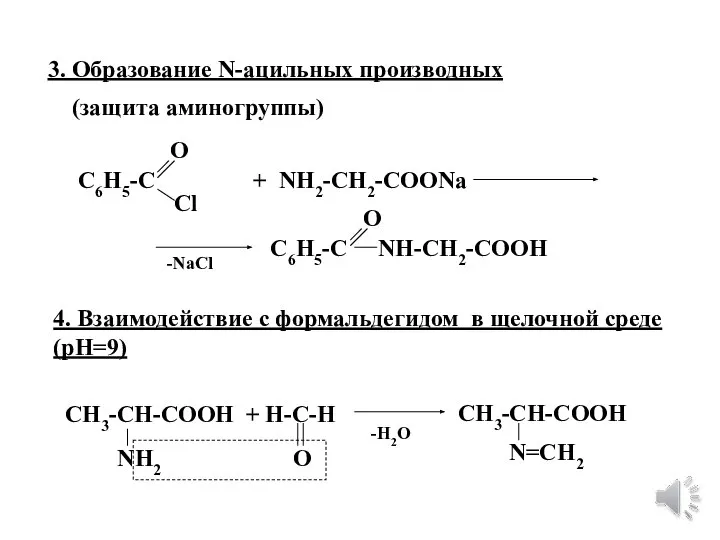
- 20. 3. Образование N-ацильных производных (защита аминогруппы) + NH2-CH2-COONa C6H5-C О Cl C6H5-C О NH-CH2-COOH -NaCl 4.
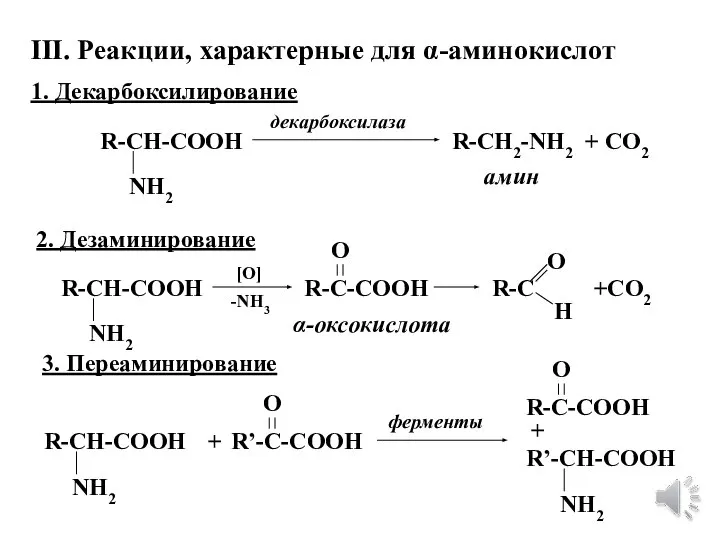
- 21. III. Реакции, характерные для α-аминокислот 1. Декарбоксилирование R-CH-COOH NH2 R-CH2-NH2 + CO2 декарбоксилаза амин 2. Дезаминирование
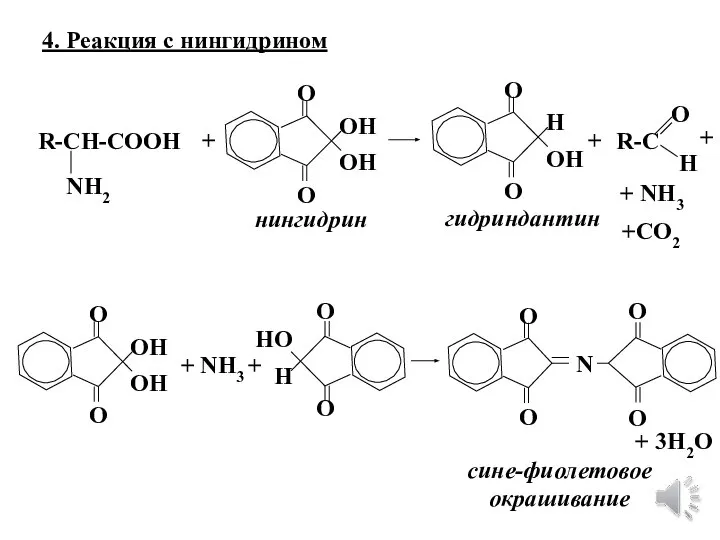
- 22. 4. Реакция с нингидрином R-CH-COOH NH2 R-C O H + ОН ОН О О нингидрин +
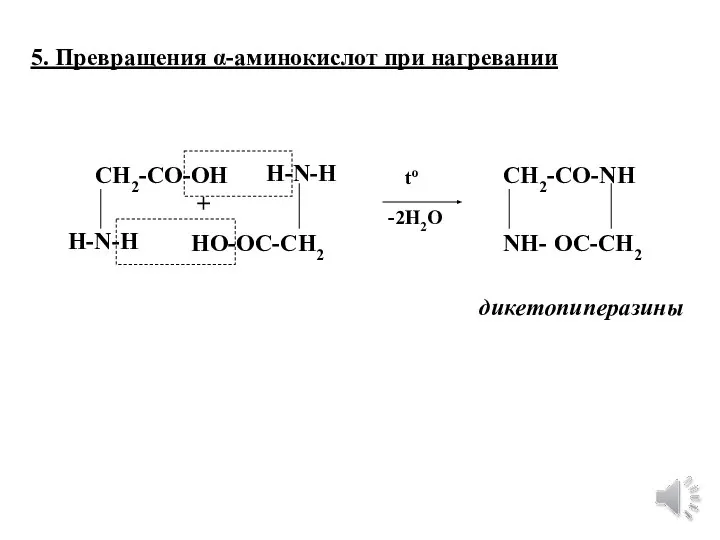
- 23. 5. Превращения α-аминокислот при нагревании CH2-CO-OH H-N-H HO-OC-CH2 H-N-H + CH2-CO- NH- OC-CH2 NH -2H2O дикетопиперазины
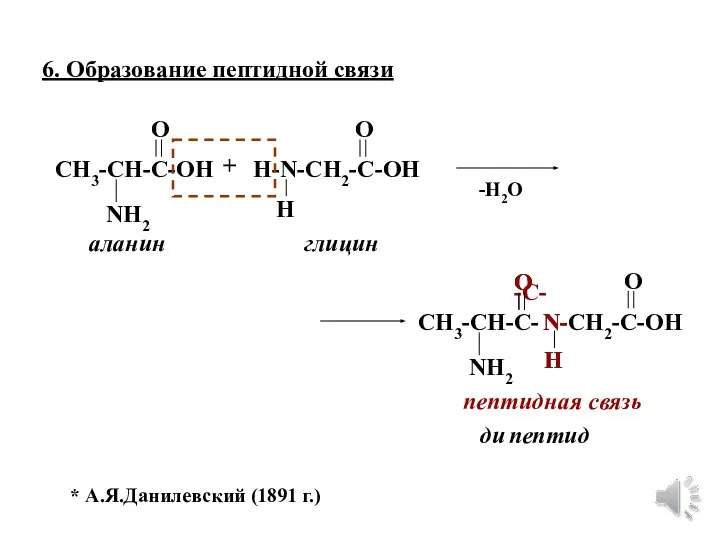
- 24. 6. Образование пептидной связи CH3-CH-C-OH NH2 O H-N-CH2-C-OH O H аланин глицин + -Н2О CH3-CH-C- NH2
- 25. Полипептид – пептид, содержащий более 10 аминокислотных звеньев Белок – пептид, содержащий более 50 аминокислотных остатков
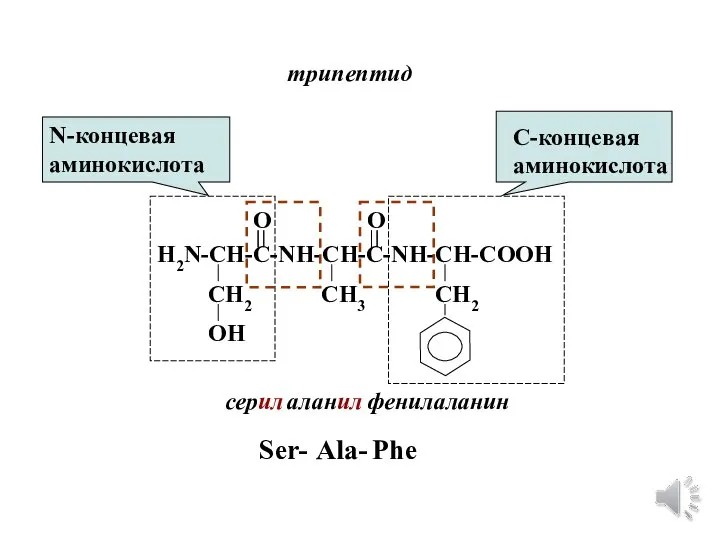
- 26. трипептид H2N-CH-C-NH-CH-C-NH-CH-COOH CH2 OH CH3 CH2 O O серил аланил фенилаланин Ser- Ala- Phe N-концевая аминокислота
- 28. Скачать презентацию




![2. Образование эфиров (защита карбоксильной группы) NH2-CH2-COOH + CH3-CH2-OH HCl -H2O Cl-[NH3-CH2-COOCH2CH3]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1175666/slide-16.jpg)

 Химия и нанотехнологии
Химия и нанотехнологии Диссоциация кислот
Диссоциация кислот Гальванические элементы
Гальванические элементы Химические методы анализа. Гравиметрический метод анализа
Химические методы анализа. Гравиметрический метод анализа Анодное растворение mn5si3-электрода в сернокислом фторидсодержащем электролите
Анодное растворение mn5si3-электрода в сернокислом фторидсодержащем электролите Моносахариды
Моносахариды Химическая промышленность. Аварии на химических предприятиях
Химическая промышленность. Аварии на химических предприятиях Гетерогенные дисперсные системы
Гетерогенные дисперсные системы Каталітичні процеси нафтопереробки
Каталітичні процеси нафтопереробки Презентация на тему Химия и проблемы экологии. Кислотные дожди
Презентация на тему Химия и проблемы экологии. Кислотные дожди  Углеродистые стали
Углеродистые стали Неметаллические материалы
Неметаллические материалы Бикомпонентные покрытия
Бикомпонентные покрытия Карбонильные производные (кислоты, альдегиды, кетоны, сложные эфиры)
Карбонильные производные (кислоты, альдегиды, кетоны, сложные эфиры) Составление ионных уравнений
Составление ионных уравнений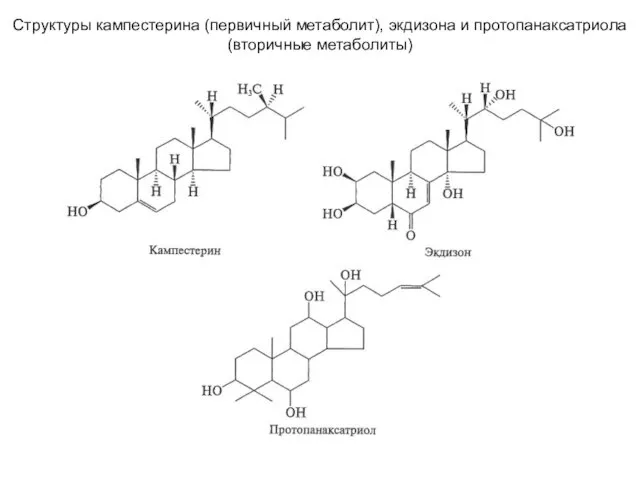 Структуры кампестерина (первичный метаболит), экдизона и протопанаксатриола (вторичные метаболиты)
Структуры кампестерина (первичный метаболит), экдизона и протопанаксатриола (вторичные метаболиты) Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Присадки для базовых масел. Присадки и наполнители пластичных смазок
Присадки для базовых масел. Присадки и наполнители пластичных смазок Стерилизация технологических потоков и оборудования
Стерилизация технологических потоков и оборудования Скорость химической реакции
Скорость химической реакции Физико-химические процессы в гидросфере
Физико-химические процессы в гидросфере Алканы. Химические свойства. Применение
Алканы. Химические свойства. Применение Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность Изучение зависимости скорости химической реакции от различных факторов. Практическая работа № 6
Изучение зависимости скорости химической реакции от различных факторов. Практическая работа № 6 Периодическая система химических элементов Д. И. Менделеева
Периодическая система химических элементов Д. И. Менделеева Презентация на тему Закон постоянства состава
Презентация на тему Закон постоянства состава  Классификация химических реакций
Классификация химических реакций Раздел 1
Раздел 1