Содержание
- 2. Образование двойного электрического слоя Причины возникновения двойного электрического слоя (ДЭС): Поверхностная диссоциация ионов; Адсорбция ионов из
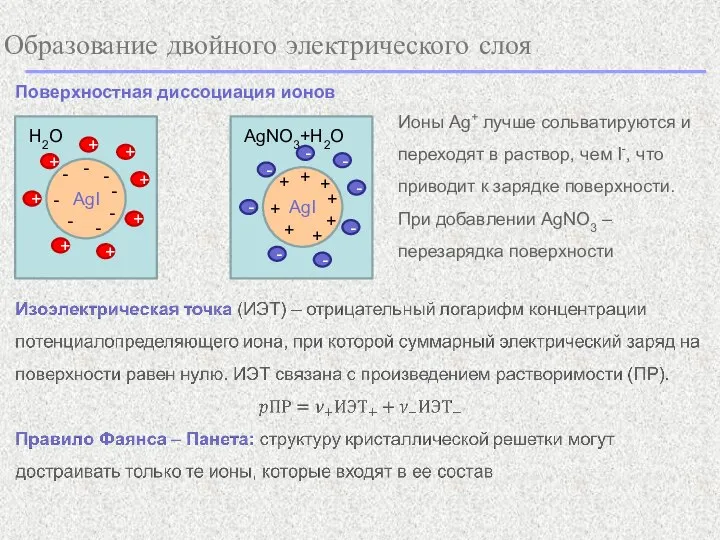
- 3. Образование двойного электрического слоя Поверхностная диссоциация ионов Ионы Ag+ лучше сольватируются и переходят в раствор, чем
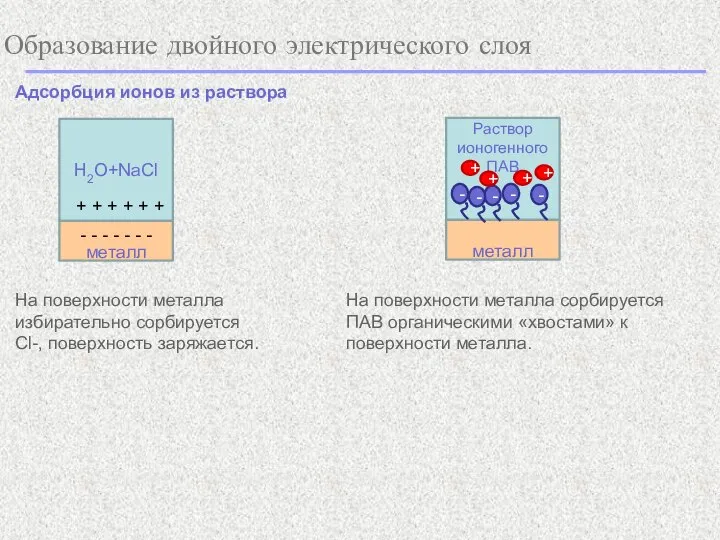
- 4. Образование двойного электрического слоя Адсорбция ионов из раствора На поверхности металла избирательно сорбируется Cl-, поверхность заряжается.
- 5. Образование двойного электрического слоя Адсорбция диполей. Контакт с неполярными жидкостями ДЭС могут образовывать и неполярные (малополярные)
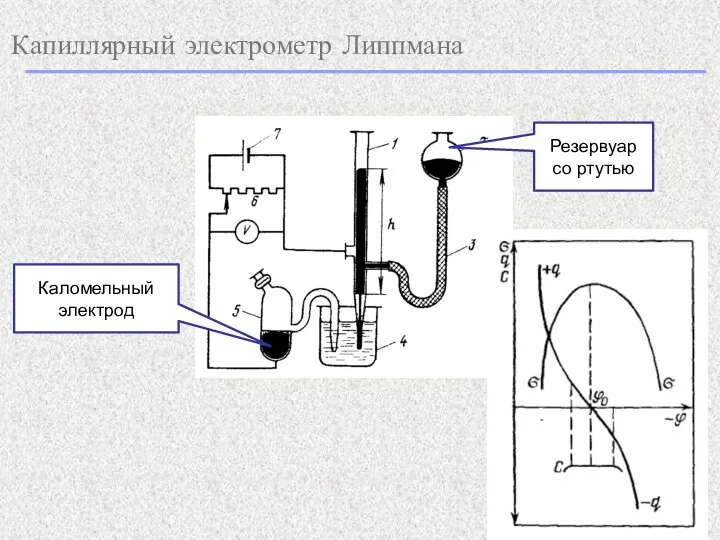
- 6. Капиллярный электрометр Липпмана Резервуар со ртутью Каломельный электрод
- 7. Первое уравнение Липпмана - первое уравнение Липпмана
- 8. Второе уравнение Липпмана. Емкость ДЭС - первое уравнение Липпмана - второе уравнение Липпмана
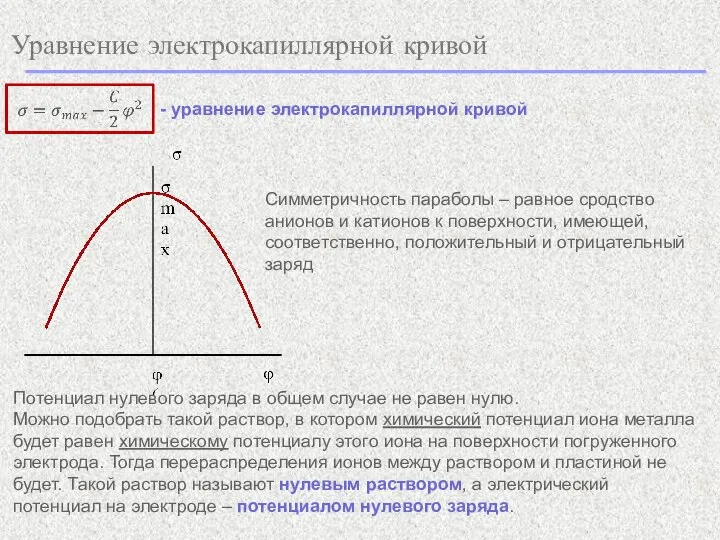
- 9. Уравнение электрокапиллярной кривой - первое уравнение Липпмана - второе уравнение Липпмана Потенциал нулевого заряда - уравнение
- 10. Уравнение электрокапиллярной кривой - уравнение электрокапиллярной кривой Симметричность параболы – равное сродство анионов и катионов к
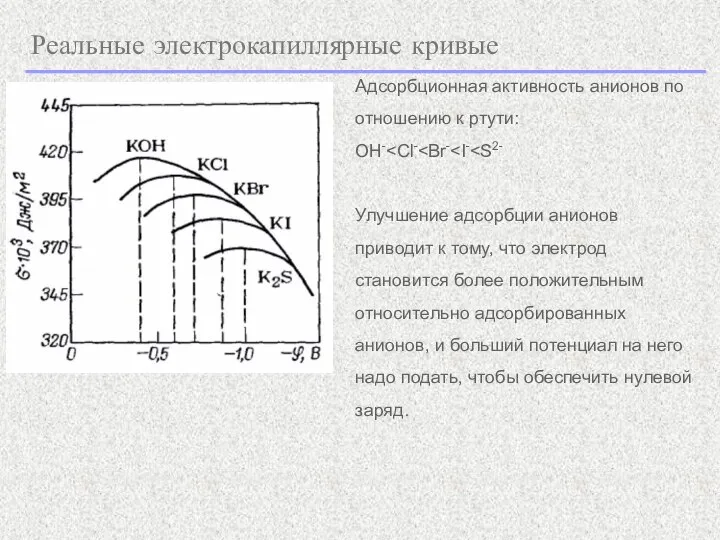
- 11. Реальные электрокапиллярные кривые Адсорбционная активность анионов по отношению к ртути: OH- Улучшение адсорбции анионов приводит к
- 12. Строение ДЭС Эволюция представлений о строении ДЭС Взгляды Гельмгольца (плоский конденсатор) Теория Гуи – Чепмена (учет
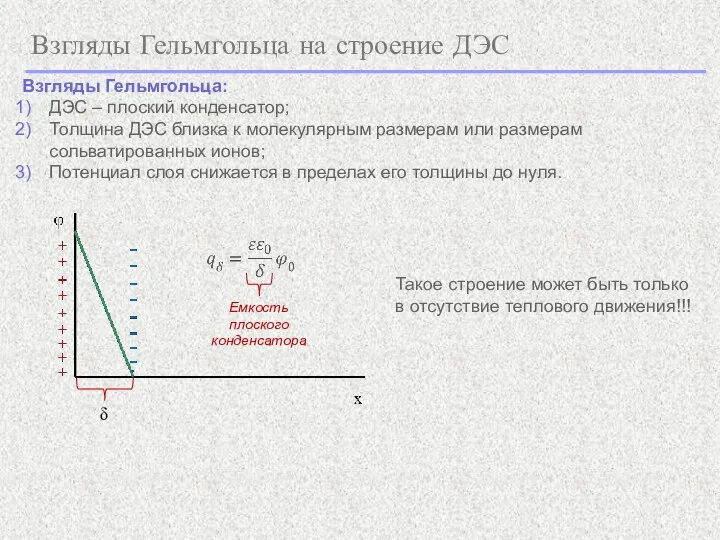
- 13. Взгляды Гельмгольца на строение ДЭС Взгляды Гельмгольца: ДЭС – плоский конденсатор; Толщина ДЭС близка к молекулярным
- 14. Теория Гуи - Чеппмена Концентрация в объеме Заряд иона Число Фарадея
- 15. Теория Гуи - Чеппмена Эл. потенциал на расстоянии x от поверхности - уравнение Пуассона - Больцмана
- 16. Теория Гуи - Чеппмена пренебрегаем Равно 0 из соображений электро-нейтральности Слабозаряж. поверхность Удвоенная ионная сила I
- 17. Теория Гуи - Чеппмена
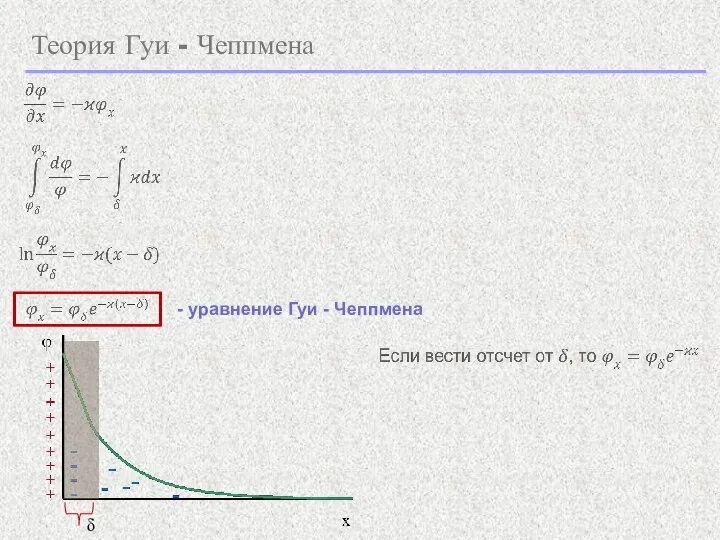
- 18. Теория Гуи - Чеппмена - уравнение Гуи - Чеппмена δ
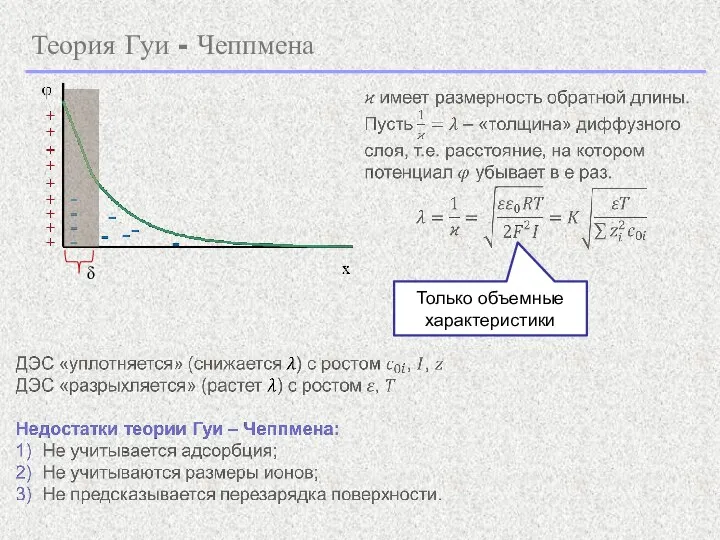
- 19. Теория Гуи - Чеппмена δ Только объемные характеристики
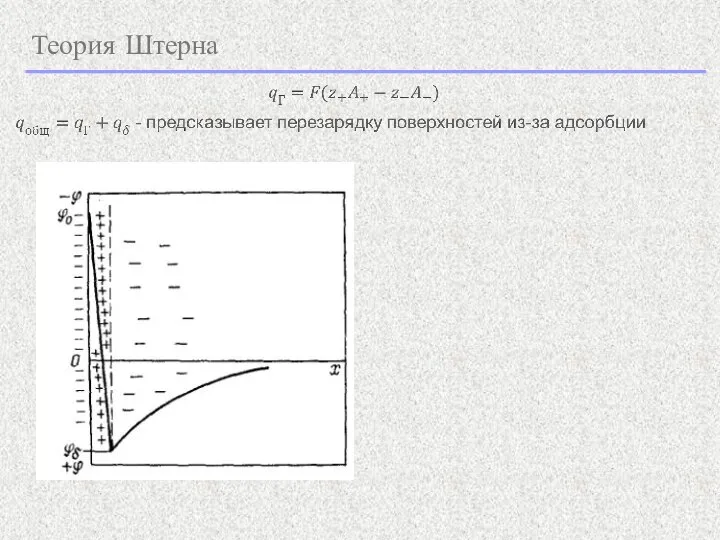
- 20. Теория Штерна δ Слой Гельмгольца Диффузный слой
- 21. Теория Штерна
- 22. Теория Штерна Учет знака заряда иона
- 23. Теория Штерна
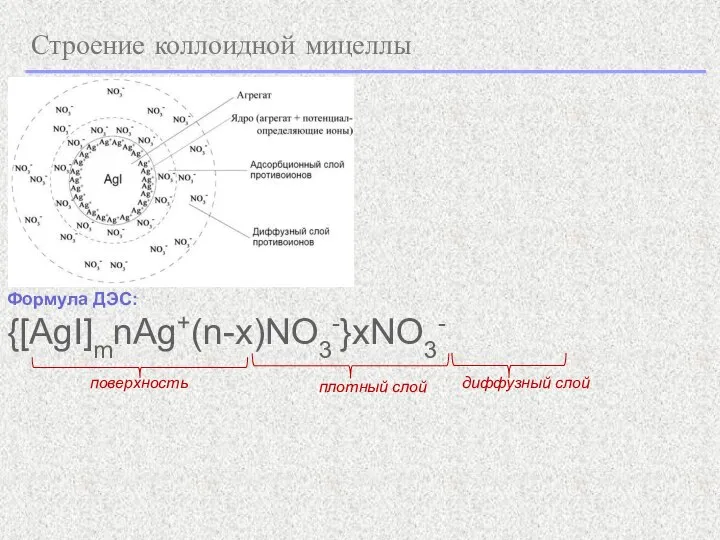
- 24. Строение коллоидной мицеллы
- 25. Строение коллоидной мицеллы Формула мицеллы {[AgI]mnAg+(n-x)NO3-}xNO3- агрегат ядро частица мицелла Мицелла в целом - электронейтральна
- 26. Запись формулы мицеллы Мицелла в целом – электронейтральна Правило Фаянса – Панета: структуру кристаллической решетки могут
- 27. Запись формулы мицеллы Мицелла в целом – электронейтральна Правило Фаянса – Панета: структуру кристаллической решетки могут
- 28. Запись формулы мицеллы Мицелла в целом – электронейтральна Правило Фаянса – Панета: структуру кристаллической решетки могут
- 30. Скачать презентацию













![Строение коллоидной мицеллы Формула мицеллы {[AgI]mnAg+(n-x)NO3-}xNO3- агрегат ядро частица мицелла Мицелла в целом - электронейтральна](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/998075/slide-24.jpg)



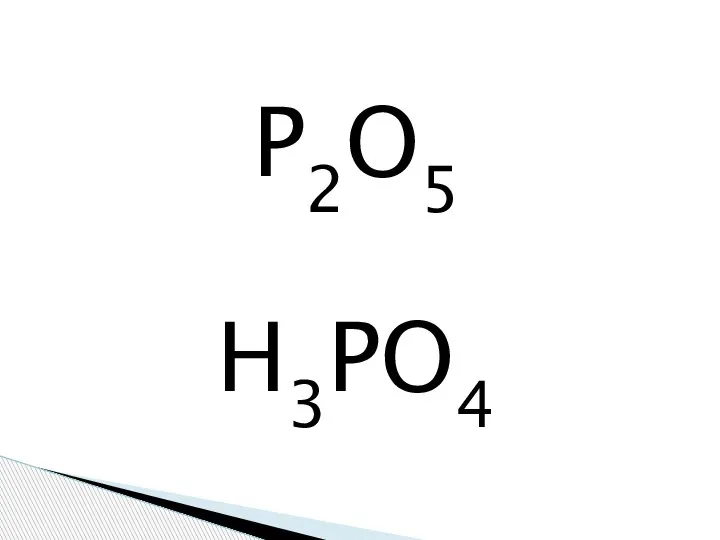 Фосфорная кислота
Фосфорная кислота Ароматические углеводороды. Бензол
Ароматические углеводороды. Бензол Презентация на тему Переработка нефти
Презентация на тему Переработка нефти  ОГЭ ХИМИЯ 1
ОГЭ ХИМИЯ 1 Презентация на тему Металлы
Презентация на тему Металлы  Графический диктант. Азот и Аммиак
Графический диктант. Азот и Аммиак Значение и применение спиртов
Значение и применение спиртов Новогодний Пробник №190415
Новогодний Пробник №190415 Реакции ионного обмена. Задания. 9 класс
Реакции ионного обмена. Задания. 9 класс Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Научный эксперимент в химической технологии
Научный эксперимент в химической технологии Основания. Щелочи – растворимые основания
Основания. Щелочи – растворимые основания Свойства растворов и их взаимодействие с газовой фазой
Свойства растворов и их взаимодействие с газовой фазой Презентация на тему Нанохимия
Презентация на тему Нанохимия  Свойства солёной воды. Море у меня в стакане
Свойства солёной воды. Море у меня в стакане Алкины. Химия с элементами биологии
Алкины. Химия с элементами биологии Применение эфиров в производстве автомобильных бензинов
Применение эфиров в производстве автомобильных бензинов Презентация на тему Электрохимический ряд напряжений металлов
Презентация на тему Электрохимический ряд напряжений металлов  Типичные реакции кислот
Типичные реакции кислот Среды для культивирования эмбрионов-история разработки и составы
Среды для культивирования эмбрионов-история разработки и составы Лабораторное оборудование. Тесты
Лабораторное оборудование. Тесты Кислоты
Кислоты Химический состав продуктов питания
Химический состав продуктов питания Судьба углеродного скелета аминокислот
Судьба углеродного скелета аминокислот Пищевые добавки: вред и польза
Пищевые добавки: вред и польза Электролитическая диссоциация
Электролитическая диссоциация Презентация на тему В мире полимеров
Презентация на тему В мире полимеров  Игра по химии Классики
Игра по химии Классики