Содержание
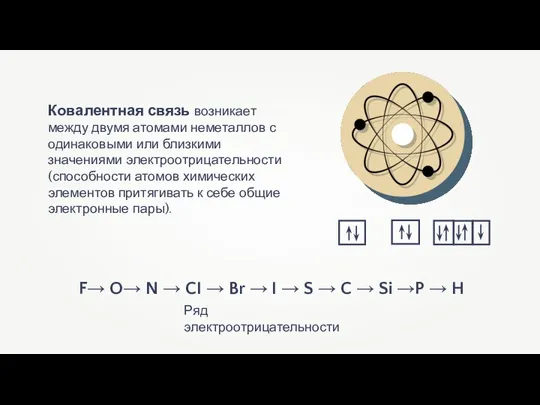
- 2. Ковалентная связь возникает между двумя атомами неметаллов с одинаковыми или близкими значениями электроотрицательности (способности атомов химических
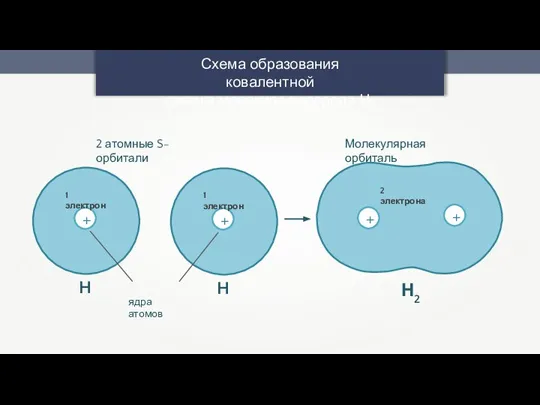
- 3. Схема образования ковалентной связи в молекуле водорода Н2 + 1 электрон H ядра атомов + 1
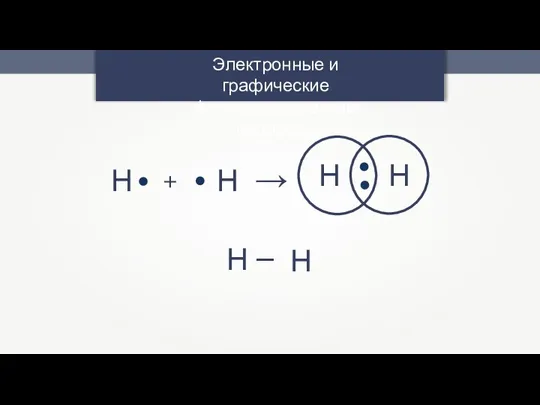
- 4. Электронные и графические формулы молекулы водорода Н + Н → Н Н Н — Н
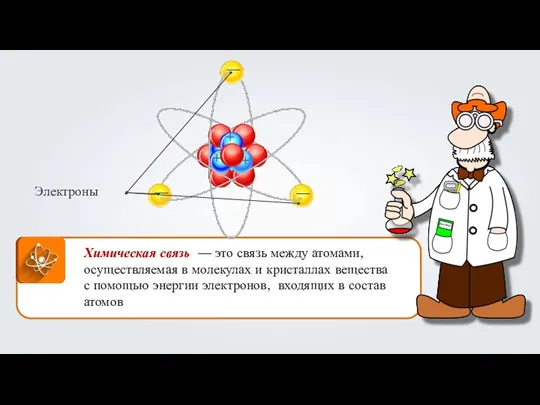
- 5. Ковалентная химическая связь – химическая связь между атомами, которая осуществляется за счёт образования общих электронных пар.
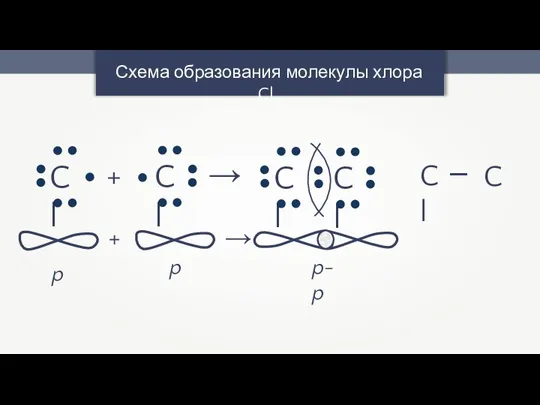
- 6. Схема образования молекулы хлора Cl2 + → Cl — C p p p-p + →
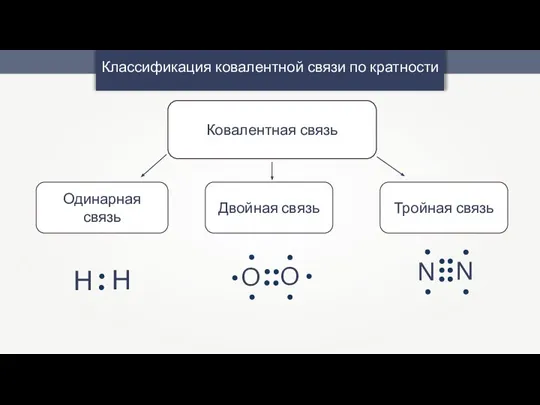
- 7. Классификация ковалентной связи по кратности Ковалентная связь
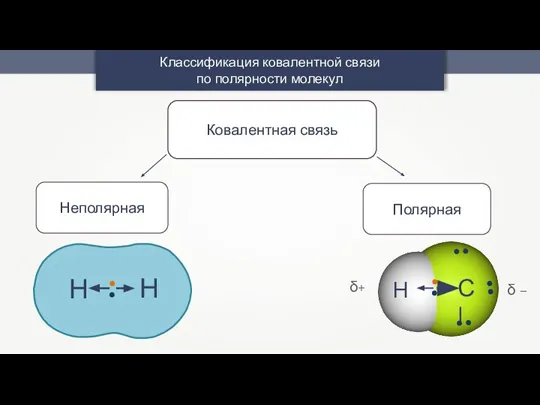
- 8. Классификация ковалентной связи по полярности молекул Ковалентная связь Сl H δ+ δ –
- 9. Диполь — молекула с двумя противоположно заряженными полюсами. – +
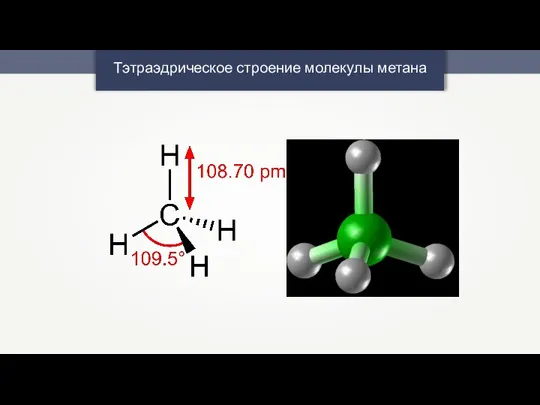
- 10. Тэтраэдрическое строение молекулы метана
- 11. Полярность молекулы зависит не только от полярности связей, но и от её геометрического строения.
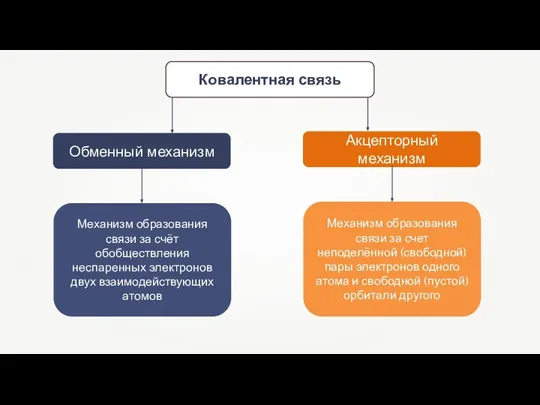
- 12. Обменный механизм Акцепторный механизм Механизм образования связи за счёт обобществления неспаренных электронов двух взаимодействующих атомов Механизм
- 13. Донорно-акцепторный механизм на примере образования иона аммония Полное молекулярное уравнение NH3 + HCl = NH4Cl Сокращённое
- 14. Донорно-акцепторный механизм на примере образования иона аммония Электронная схема взаимодействия Н Н Н N X X
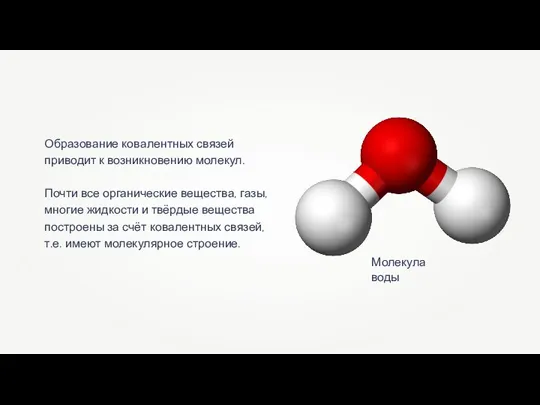
- 15. Образование ковалентных связей приводит к возникновению молекул. Почти все органические вещества, газы, многие жидкости и твёрдые
- 16. Молекулярная кристаллическая решетка Углекислый газ Йод
- 18. Скачать презентацию






 Ковалентная неполярная химическая связь
Ковалентная неполярная химическая связь Кислород. 8 класс
Кислород. 8 класс Альдегиды, их химические и физические свойства. Получение и применение альдегидов
Альдегиды, их химические и физические свойства. Получение и применение альдегидов Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Метаболизм липидов
Метаболизм липидов Жиры. Определение и общая формула
Жиры. Определение и общая формула Алюминий и его соединения
Алюминий и его соединения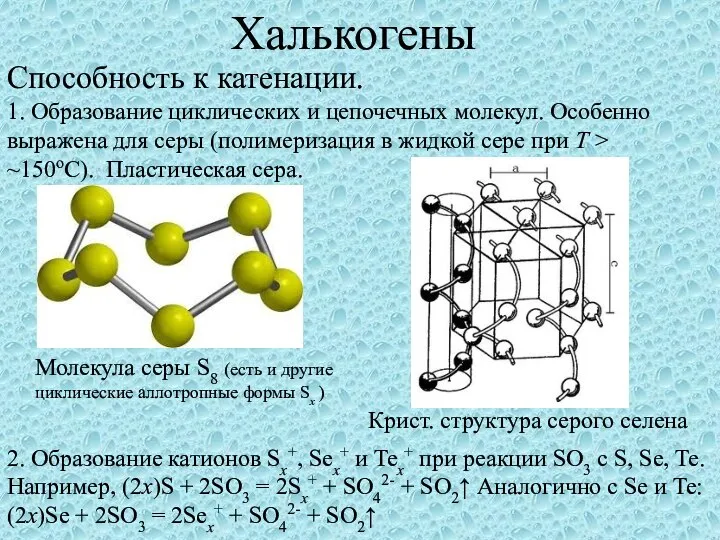 Халькогены. Способность к катенации
Халькогены. Способность к катенации Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Арбузный снег. Предположения
Арбузный снег. Предположения Презентация на тему ОВР в органической химии
Презентация на тему ОВР в органической химии  Её величество – вода Интегрированный урок химии в 8 классе
Её величество – вода Интегрированный урок химии в 8 классе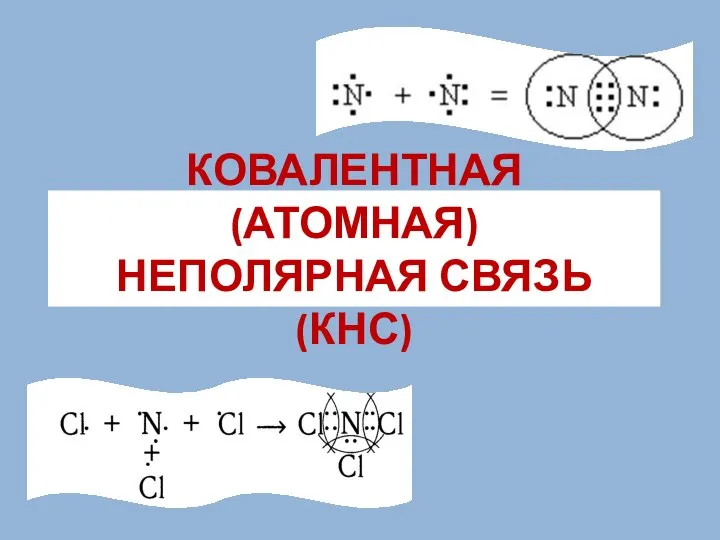 676a1c5e85f2455c9a6d495b8a94b9f9
676a1c5e85f2455c9a6d495b8a94b9f9 Периодическая система
Периодическая система Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность Презентация на тему Лекарства дома
Презентация на тему Лекарства дома  Радиоактивность. Тест
Радиоактивность. Тест Презентация на тему Лабораторное оборудование. Посуда и средства защиты
Презентация на тему Лабораторное оборудование. Посуда и средства защиты 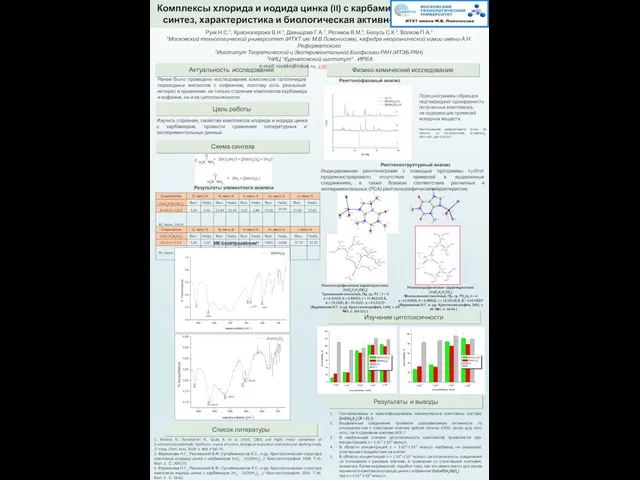 Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность
Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность Закон сохранения массы веществ
Закон сохранения массы веществ Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Основные понятия химической термодинамики
Основные понятия химической термодинамики Основы химической термодинамики. Основные понятия химической термодинамики. Лекция 1
Основы химической термодинамики. Основные понятия химической термодинамики. Лекция 1 Сокровища соляных дворцов
Сокровища соляных дворцов Презентация на тему Занимательная химия
Презентация на тему Занимательная химия  Подготовка к административной контрольной работе по химии
Подготовка к административной контрольной работе по химии Гидроксид кальция – гашеная известь
Гидроксид кальция – гашеная известь Анализ свойств карбамидоформальдегидных смол
Анализ свойств карбамидоформальдегидных смол