Содержание
- 2. Электролиз растворов и расплавов солей
- 3. Учебная цель: 10.2.3.8 описывать сущность процесса электролиза; 10.2.3.9 применять эмпирические правила для прогнозирования продуктов электролиза на
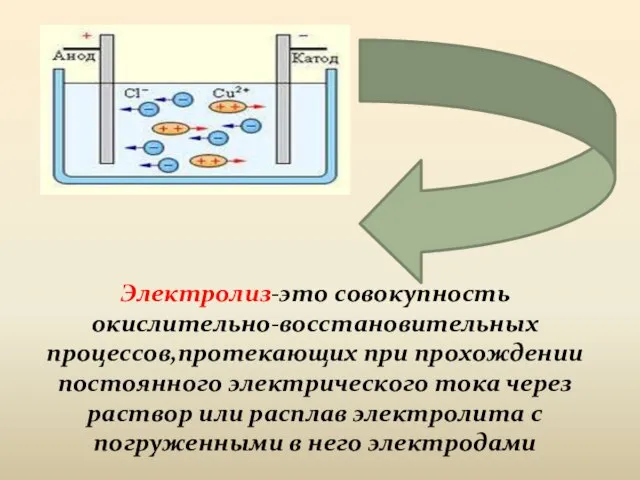
- 4. Электролиз-это совокупность окислительно-восстановительных процессов,протекающих при прохождении постоянного электрического тока через раствор или расплав электролита с погруженными
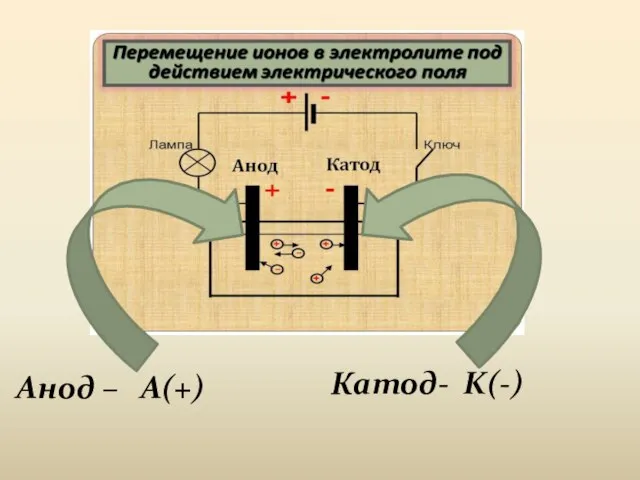
- 5. Катод- K(-) Анод – A(+)
- 6. Электролиз расплава NaBr I. В расплаве электролита присутствуют только ионы, образовавшиеся при его диссоциации, они и
- 7. II. Электролиз водного раствора электролита В отличии от расплава в растворе электролита кроме ионов, получившихся при
- 8. MnZnCrFeCoNiSnPb Если у катода накапливаются катионы металла (стоящего в ряду напряжений после H2), то восстанавливаются ионы
- 9. 3) Если у катода накапливаются катионы металла,который расположен в ряду напряжений (после AL и до H2),то
- 10. 5) При электролизе растворов солей бескислородных кислот( кроме фторидов) окисляются анионы кислотных остатков 2CL- - 2e-=CL2
- 11. 6) При электролизе растворов солей кислородосодержащих кислот и фторидов идет процесс окисления гидроксид-ионов из молекул воды
- 12. Алгоритм составления уравнения электролиза на примере р-ра CuSO4 Записать уравнение диссоциации соли. Записать полуреакцию процесса, который
- 13. 5. Сложить левые и правые части полуреакций, умножив их на коэффициенты, получив сокращенное ионное уравнение. 6.
- 14. Пример составления уравнения электролиза раствора CuSO4
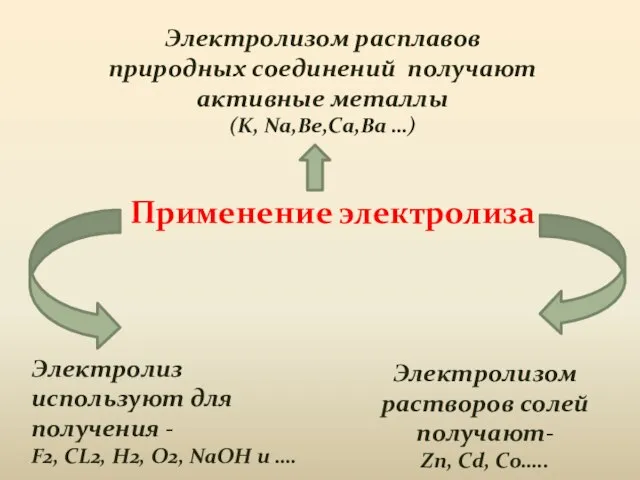
- 15. Применение электролиза Электролизом расплавов природных соединений получают активные металлы (K, Na,Be,Ca,Ba …) Электролизом растворов солей получают-
- 16. Критерий оценивания: составляет уравнение электролиза Дескриптор: Записывает уравнение диссоциации соли (1 балл); Записывает полуреакции, протекающие на
- 17. Записать уравнение электролиза водного раствора нитрата серебра AgNO3. Задание на закрепление:
- 18. Проверь себя 1. При электролизе водного раствора хлорида лития (LiCL) на аноде в результате электролиза образуется:
- 19. Проверь себя 2. При электролизе водного раствора сульфата меди (II) ( CuSO4) на катоде выделится: А)
- 20. Проверь себя 3. Установите соответствие между формулой соли и продуктом,образующимся на инертном аноде при электролизе ее
- 21. Самопроверка 1) В Установите соответствие между формулой соли и продуктом,образующимся на инертном аноде при электролизе ее
- 23. Скачать презентацию

















 Юные химики. Своя игра
Юные химики. Своя игра Оксидтер мен негіздердің реакциялары
Оксидтер мен негіздердің реакциялары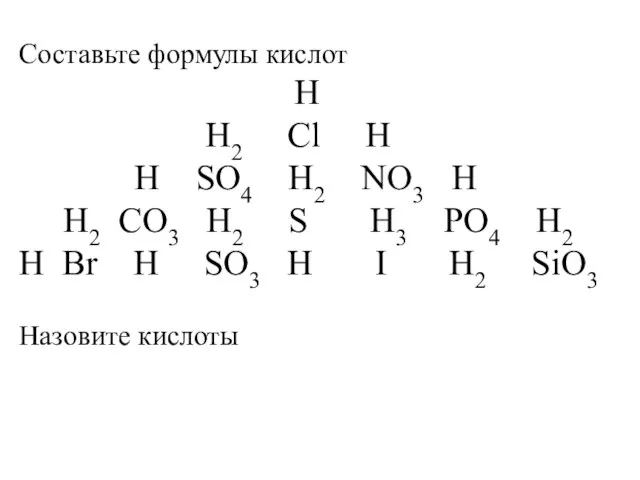 Составьте формулы кислот
Составьте формулы кислот Физико - химические основы получения лекарственных препаратов (лекция 4)
Физико - химические основы получения лекарственных препаратов (лекция 4) Гидрометаллургическое обескремнивание титанового сырья соединениями фтора
Гидрометаллургическое обескремнивание титанового сырья соединениями фтора Электролитическая диссоциация
Электролитическая диссоциация Углеводороды. Урок-игра
Углеводороды. Урок-игра Якісні реакції органічних речовин
Якісні реакції органічних речовин Липиды молока и молочных продуктов. Группы липидов
Липиды молока и молочных продуктов. Группы липидов Презентация на тему Природные источники углеводородов
Презентация на тему Природные источники углеводородов  Презентация по Химии "Белки как основа всего живого"
Презентация по Химии "Белки как основа всего живого"  Молярная масса вещества
Молярная масса вещества Буферные растворы
Буферные растворы Химия вокруг нас. 10 класс
Химия вокруг нас. 10 класс Получение и применение аренов
Получение и применение аренов Циклоалканы. Изомерия циклоалканов
Циклоалканы. Изомерия циклоалканов Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Строение атома
Строение атома Оксид серы (VI)
Оксид серы (VI) Её величество – вода Интегрированный урок химии в 8 классе
Её величество – вода Интегрированный урок химии в 8 классе Красители vs пигменты
Красители vs пигменты Турнир Знатоков Химии
Турнир Знатоков Химии Производство аммиака
Производство аммиака Химический состав молока
Химический состав молока Классификация реакций и реагентов. Кислотные и основные свойства биомолекул
Классификация реакций и реагентов. Кислотные и основные свойства биомолекул Основания. Химические свойства.получение
Основания. Химические свойства.получение Введение. Тренажер
Введение. Тренажер Конкурс О, химия – ты муза вдохновения!
Конкурс О, химия – ты муза вдохновения!