Содержание
- 2. Химический состав бурового раствора определяет и влияет на Обзор Взаимодействие его дисперсионной и дисперсной сред Взаимодействие
- 3. Задачи Основные понятия и терминология Щелочность
- 4. Основные понятия и терминология Baroid a Halliburton Company
- 5. Однородная система или вещество - полностью однородны, имеют одинаковые свойства в каждой пробной точке. Неоднородная система
- 6. Отдельные части неоднородных систем отделяются поверхностью раздела, но каждая среда сама по себе будет являться однородной.
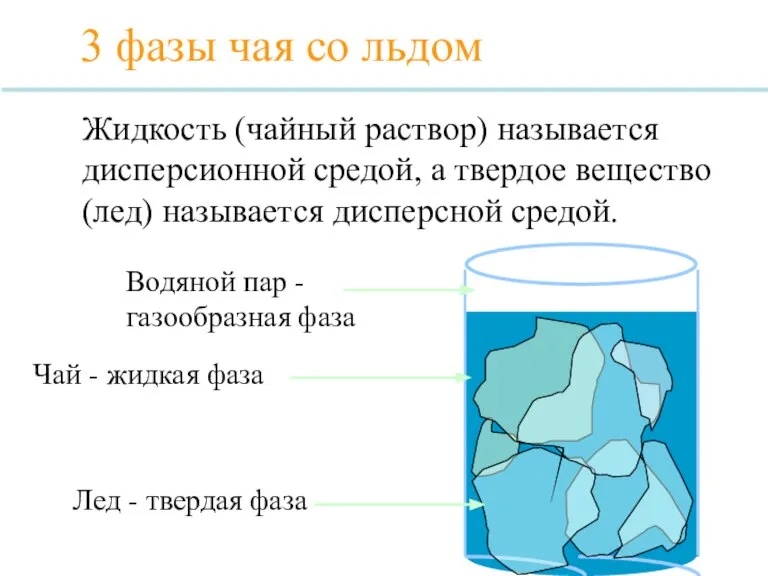
- 7. 3 фазы чая со льдом Лед - твердая фаза Водяной пар - газообразная фаза Чай -
- 8. Газов Жидкостей Твердых веществ, взвешенных в жидкости или газе. 3 фазы бурового раствора Буровой раствор -
- 9. Элементы Элемент - это химическое вещество, единственное в своем роде, которое нельзя упростить или образовать химическим
- 10. Соединение Образовано двумя или более элементарными частицами вещества при неизменном соотношении их масс Новое вещество с
- 11. Формулы представляют собой сочетание элементов, которые образуют молекулу: Молекула - наименьшая частица, которая существует самостоятельно Пример:
- 12. Атомы Атом - наименьшая частица элемента, которая участвует в образовании молекулы. Атомы состоят из более простых
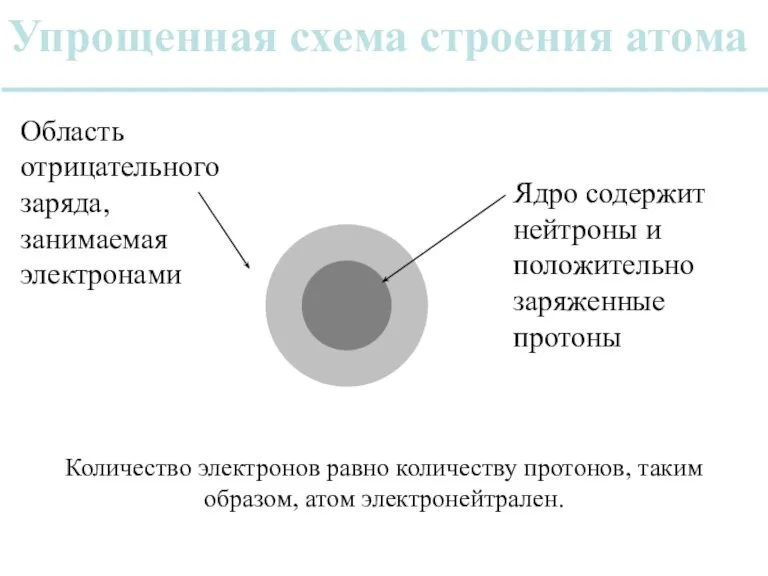
- 13. Упрощенная схема строения атома Ядро содержит нейтроны и положительно заряженные протоны Область отрицательного заряда, занимаемая электронами
- 14. Относительная атомная масса Относительные атомные массы для всех элементов приведены в Периодической таблице с точностью до
- 15. Относительная атомная масса Атомы одного элемента могут иметь различное количество нейтронов в ядре, соответственно и разные
- 16. Атомный номер Определяет атом, т.е. какой это элемент. Все 106 элементов имеют различное количество протонов в
- 17. Атомы и элементы Железо имеет плотность 7.7 г/см3 и является химическим элементом. Атомное число - 26,
- 18. Молекулярная масса Молекула - это частица, состоящая из двух или более атомов, соединенных вместе. Молекулярная масса
- 19. Постоянная Авогадро Число 6.02 x 1023 называется постоянной Авогадро для изотопа C12. Это количество атомов или
- 20. Постоянная Авогадро Один моль воды (молекулярная масса 18) весит 18 грамм, а один моль углерода (атомная
- 21. Химические реакции Химические реакции приводят к изменению энергии и перераспределению электронов, окружающих атомы, участвующие в реакции.
- 22. В результате ионной связи происходит перемещение одного или более электронов от одного атома к другому. Атомы,
- 23. Катион Положительно заряженный ион называется катионом, графически обозначается надстрочным знаком “+”, который пишется после химического знака.
- 24. Анион Атомы, которые приобрели электроны и таким образом стали отрицательно заряженными ионами, называются анионами. Так Cl-
- 25. Пример соединения Соединение натрия с хлором, хлорид натрия, - это кристаллическое вещество, которое структура которого поддерживается
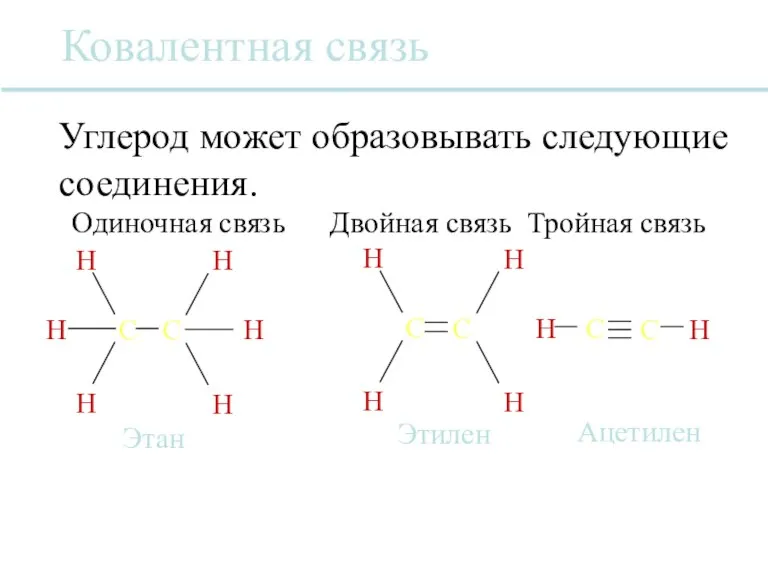
- 26. Ковалентная связь Ковалентная связь возникает, когда электроны распределяются между атомами. Два отдельных атома в одной и
- 27. Ковалентная связь H C H H H C H H H C H H C C
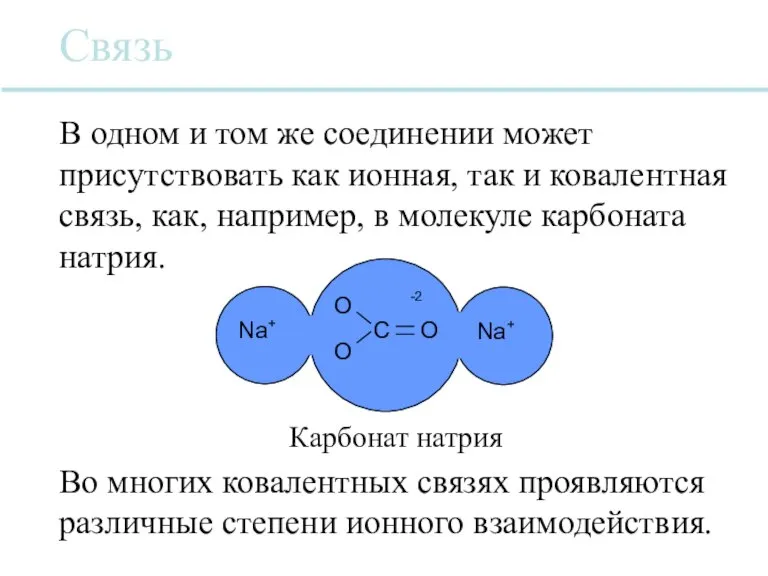
- 28. Na + O O Na + C O -2 Карбонат натрия Связь В одном и том
- 29. Различные виды атомов имеют неодинаковое электронное сродство. Когда образуется ковалентная связь, распределение электронов нарушается в сторону
- 30. Когда электроны распределяются равномерно, частичных зарядов не возникает, и молекула является неполярной. Неполярная ковалентная связь B
- 31. Растворы - это однофазные смеси различных веществ. Два вещества образуют дисперсионную жидкую фазу раствора, известную как
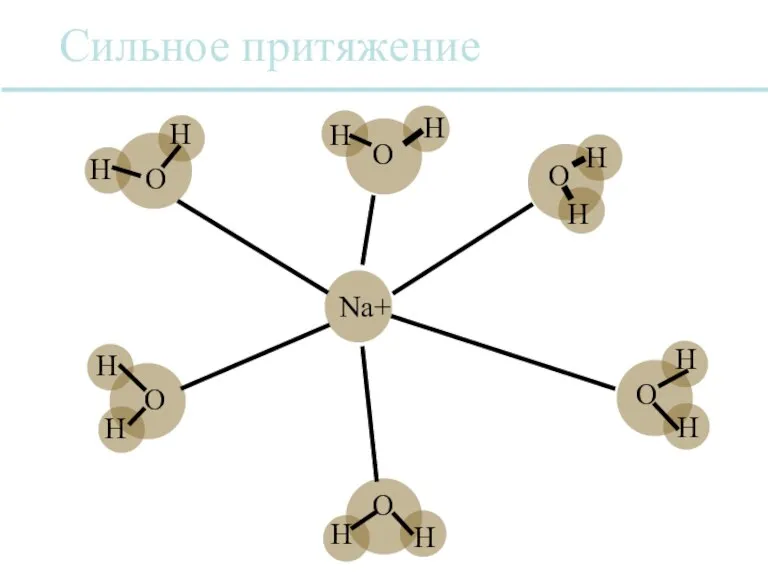
- 32. Вода является универсальным растворителем. Многие ионные соединения растворимы в воде, потому что сила притяжения между противоположно
- 33. Сильное притяжение Na+ O O O O O H H H H H H H H
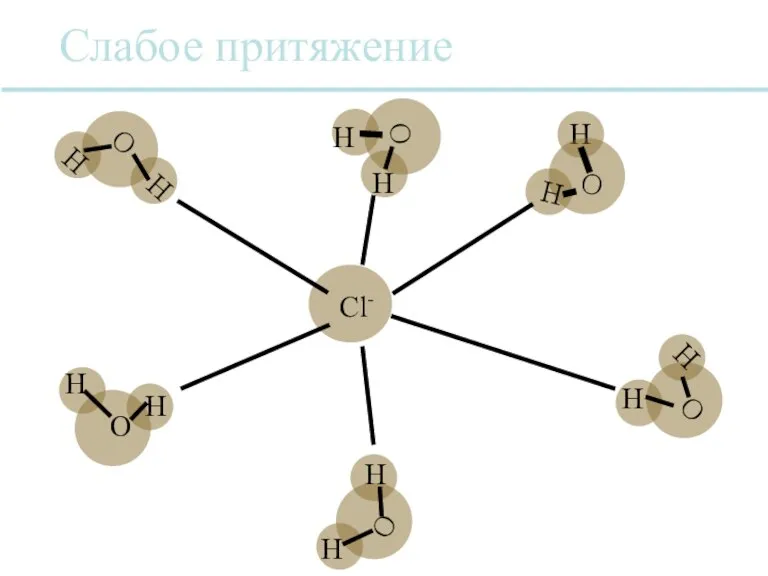
- 34. Слабое притяжение Cl- O H H H O H O O O H H H H
- 35. Неполярные растворители Дизельное топливо Не сольватирует ионы Ионные соединения не растворимы в дизельном топливе.
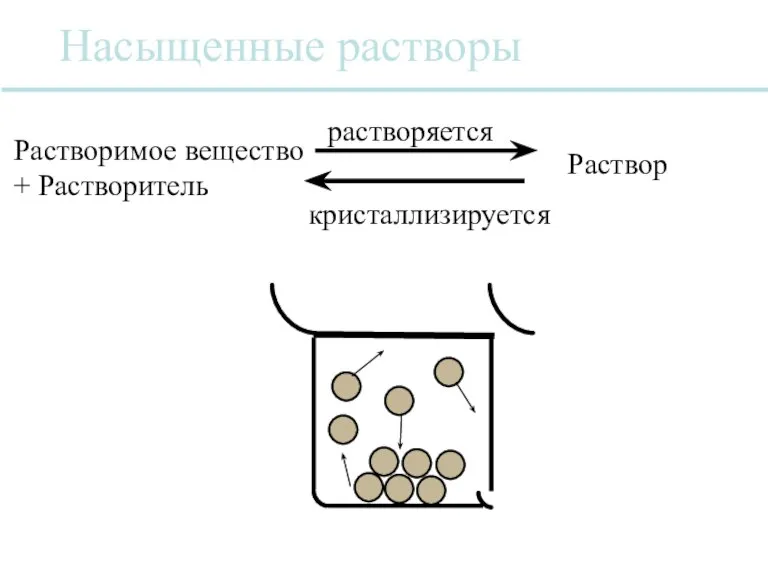
- 36. Насыщенные растворы Растворимое вещество + Растворитель Раствор растворяется кристаллизируется
- 37. Растворимость Растворимость NaCl в воде при температуре 0°F - 35.7 г на 100см3 Насыщенный раствор Ненасыщеннный
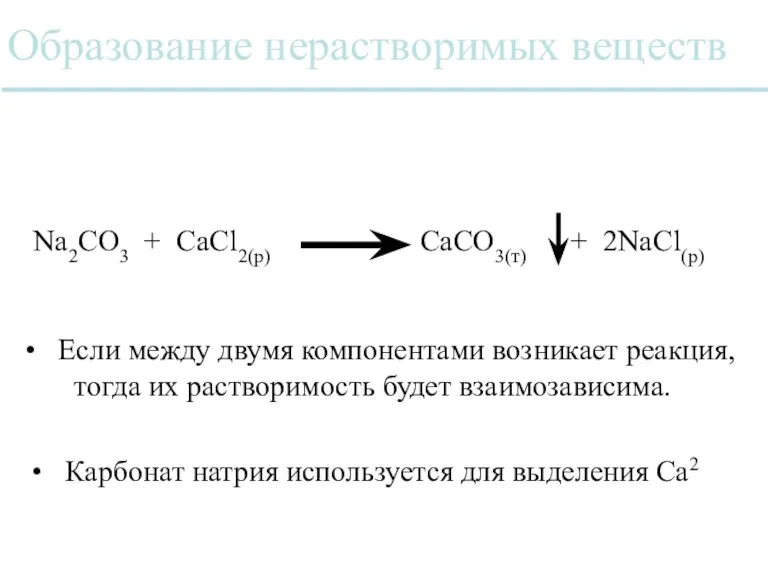
- 38. Образование нерастворимых веществ Na2CO3 + CaCl2(р) CaCO3(т) + 2NaCl(р) Карбонат натрия используется для выделения Ca2 Если
- 39. Кислоты и основания КИСЛОТА вещество, в состав которых входит водород, который может заменяться металлами с образованием
- 40. Щелочность Baroid a Halliburton Company
- 41. Щелочность Определяется растворимыми в воде ионами, которые нейтрализуют кислоту ионы, которые отдают протон (H+) H2SO4 2H+
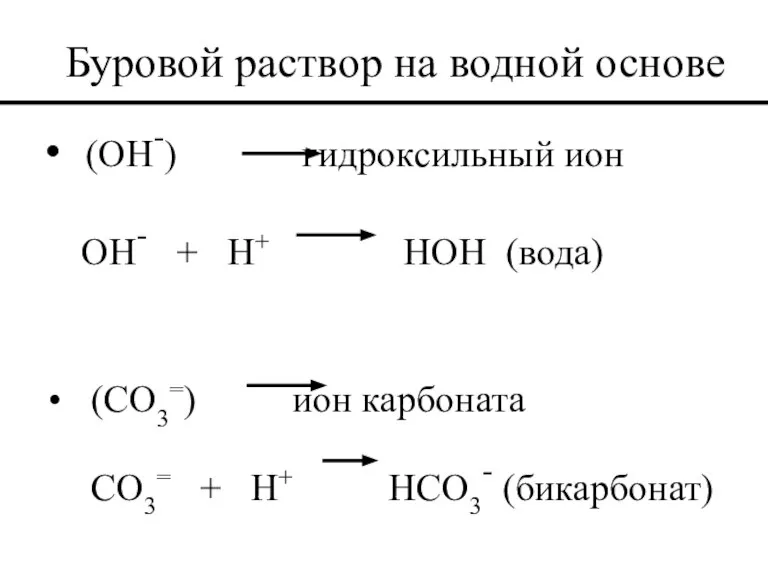
- 42. Буровой раствор на водной основе (OH-) гидроксильный ион OH- + H+ HOH (вода) (CO3=) ион карбоната
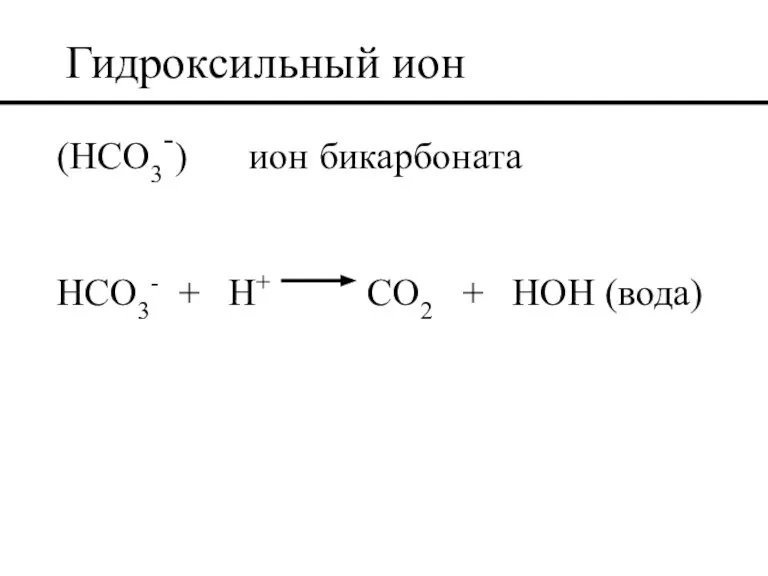
- 43. Гидроксильный ион (HCO3-) ион бикарбоната HCO3- + H+ CO2 + HOH (вода)
- 44. pH pH = - log (H+) (OH-) (H+) = 10 -14 (OH-) (H+) = Kв =
- 45. pH (H+) = 1 X 10 -4 моль/литр pH = 4 (OH-) = 1 X 10
- 46. Источники щелочности OH- (Mg(OH)2) гидроксид магния (Ca(OH)2) гидроксид кальция (известь) (NaOH) гидроксид натрия (едкий натр) (KOH)
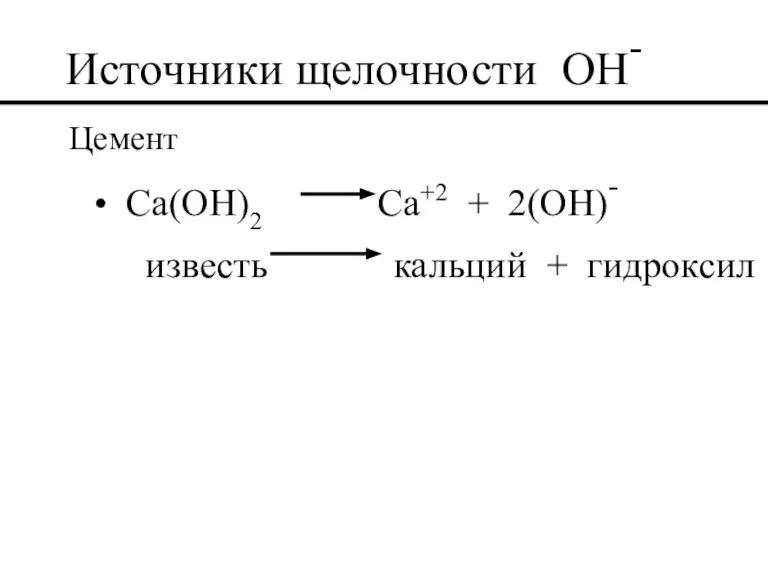
- 47. Источники щелочности OH- Цемент Ca(OH)2 Ca+2 + 2(OH)- известь кальций + гидроксил
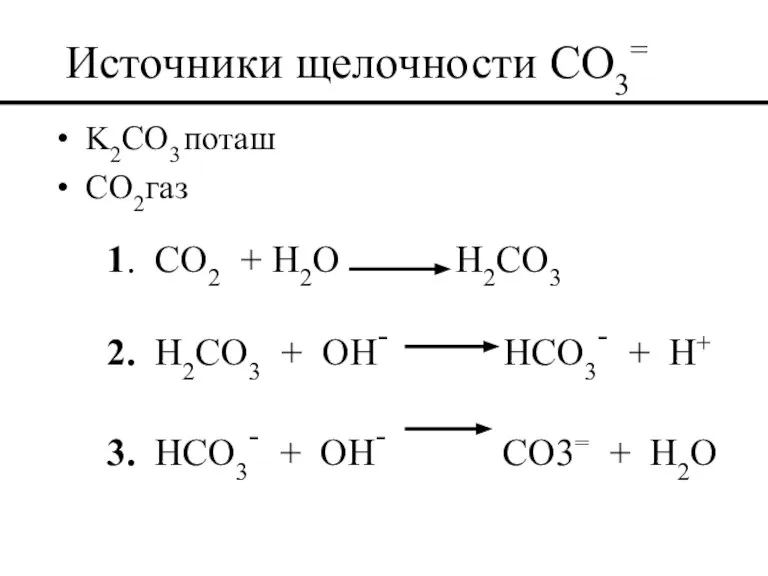
- 48. Источники щелочности CO3= K2CO3 поташ CO2 газ 1. CO2 + H2O H2CO3 2. H2CO3 + OH-
- 49. Источники CO2 Понизители водоотдачи бурового раствора, такие как KWIK SEAL и PHENO SEAL желатинизированный крахмал или
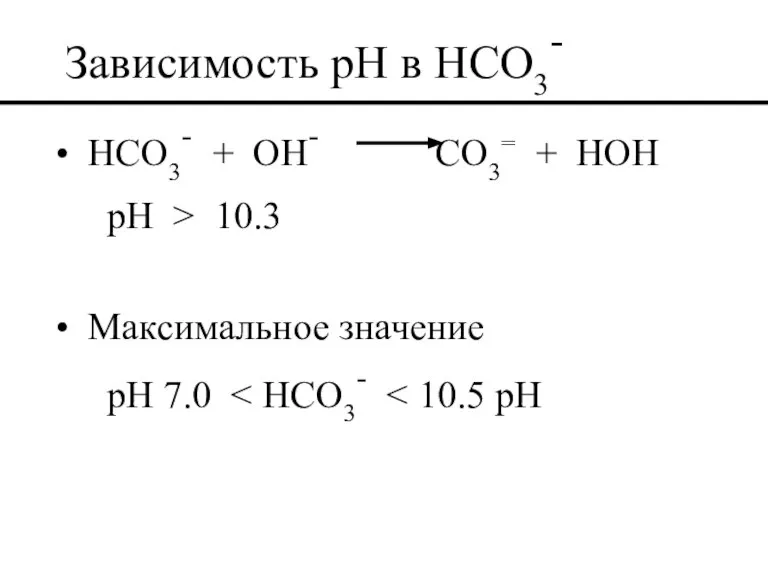
- 50. Зависимость pH в HCO3- HCO3- + OH- CO3= + HOH pH > 10.3 Максимальное значение pH
- 51. 6.3 pH > 10.3 CO3= ион карбоната 4.3 Уровень pH щелочного иона 8.5 11.5
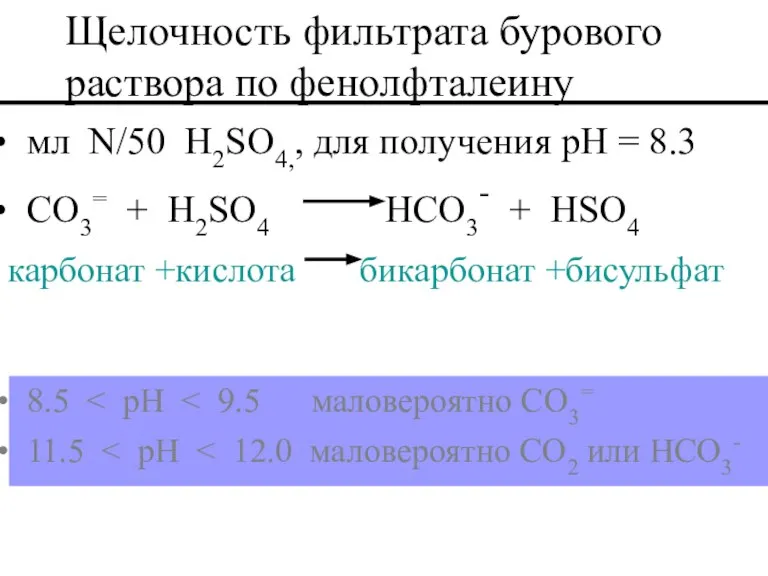
- 52. мл N/50 H2SO4,, для получения pH = 8.3 CO3= + H2SO4 HCO3- + HSO4 карбонат +кислота
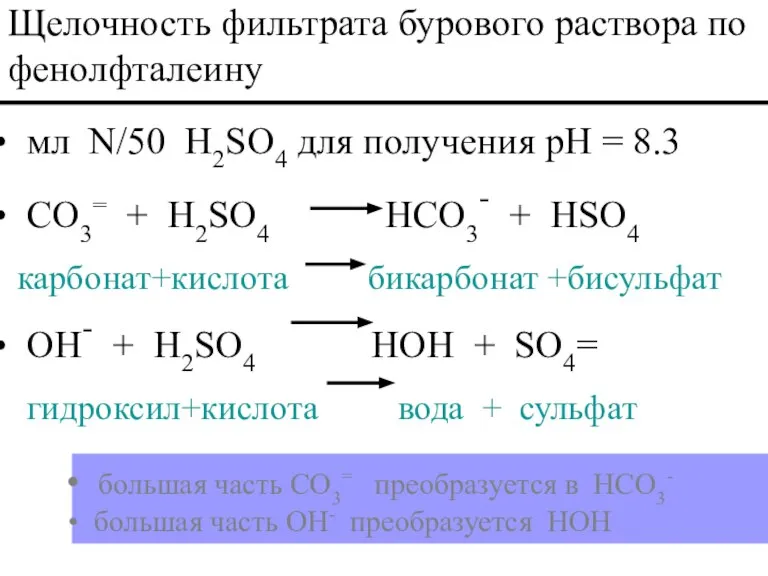
- 53. мл N/50 H2SO4 для получения pH = 8.3 CO3= + H2SO4 HCO3- + HSO4 карбонат+кислота бикарбонат
- 54. мл N/50 H2SO4,, чтобы получить уровень pH = 4.3 HCO3- + H2SO4 CO2 + H2O +
- 55. Высокая щелочность фильтрата бурового раствора по фенолфталеину и по метилоранжу CO3= Высокая щелочность фильтрата бурового раствора
- 57. Скачать презентацию

































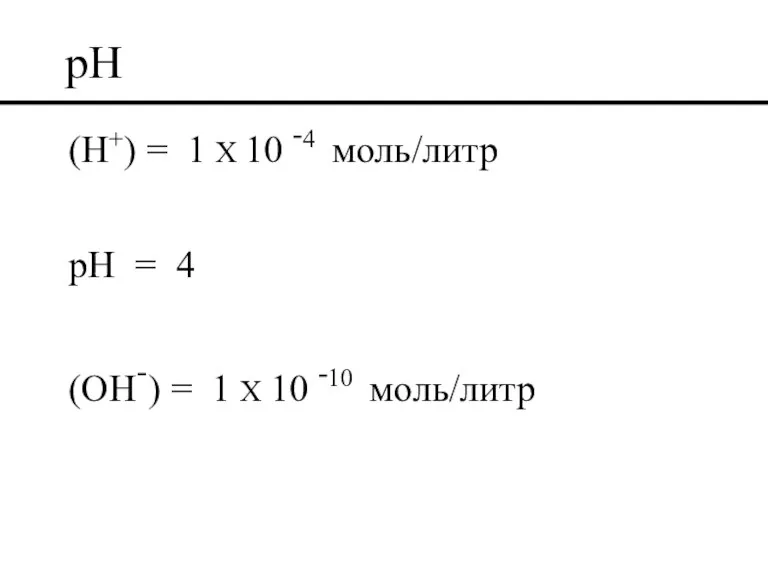





 Презентация на тему Cкорость химических реакций
Презентация на тему Cкорость химических реакций  Оксиды. Классификация оксидов
Оксиды. Классификация оксидов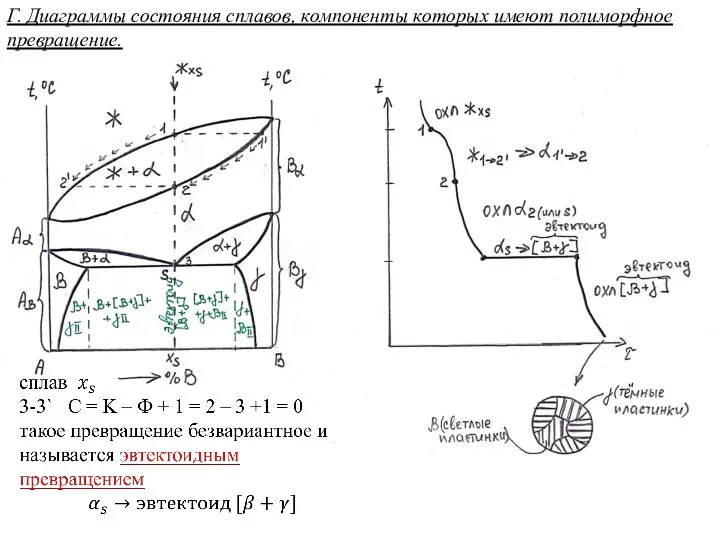 Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение
Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение Теория химического строения (ТХС). Предпосылки создания
Теория химического строения (ТХС). Предпосылки создания Посвящение в химики
Посвящение в химики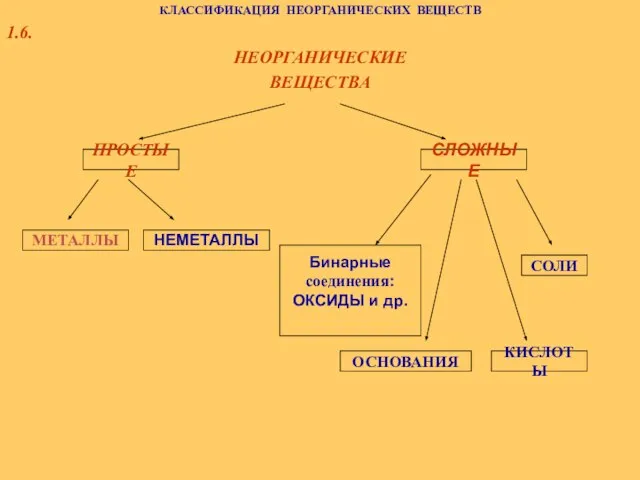 Классификация неорганических веществ
Классификация неорганических веществ Теория электролитической диссоции
Теория электролитической диссоции Применение ЦОР на уроках биологии и химии
Применение ЦОР на уроках биологии и химии Циклоалканы или цикланы – циклические насыщенные углеводороды
Циклоалканы или цикланы – циклические насыщенные углеводороды Презентация на тему Свойства простых веществ
Презентация на тему Свойства простых веществ  Электролит
Электролит Алкены. Строение
Алкены. Строение Долговечность пластмасс
Долговечность пластмасс Подготовка к контрольной работе
Подготовка к контрольной работе Кислотно-основные равновесия
Кислотно-основные равновесия Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Презентация на тему Серная кислота
Презентация на тему Серная кислота  Презентация на тему Электролиз расплавов и растворов
Презентация на тему Электролиз расплавов и растворов  Оксиды. Классификация, химические и физические свойства
Оксиды. Классификация, химические и физические свойства Элемент Фосфор
Элемент Фосфор Дифференцированный подход в преподавании химии
Дифференцированный подход в преподавании химии Классификация неорганический веществ
Классификация неорганический веществ Кислые горные породы
Кислые горные породы Vodík
Vodík Превращение веществ. История химии. Автор: Рассказова Н.Л., учитель химии и биологии МОУ «СОШ №8».
Превращение веществ. История химии. Автор: Рассказова Н.Л., учитель химии и биологии МОУ «СОШ №8». Білім алушылардың мектеп жасынан бастап экологиялық мәдениетін қалыптастыру үшін волонтерлар клубын ашу
Білім алушылардың мектеп жасынан бастап экологиялық мәдениетін қалыптастыру үшін волонтерлар клубын ашу Характеристика химического элемента по его положению в периодической системе элементов Д.И. Менделеева
Характеристика химического элемента по его положению в периодической системе элементов Д.И. Менделеева Органическая химия. Подготовка к экзамену
Органическая химия. Подготовка к экзамену