Содержание
- 2. Характеристика курса:
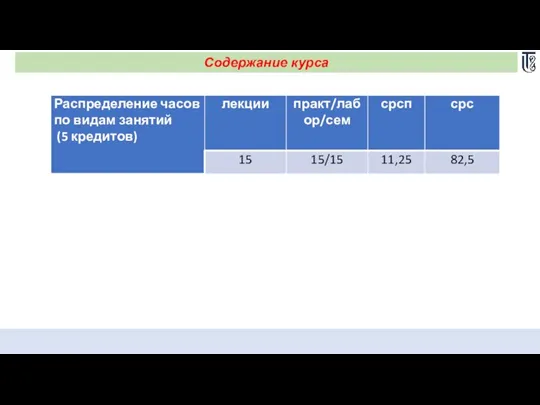
- 3. Содержание курса
- 4. Литература
- 5. Пререквизиты и постреквизиты
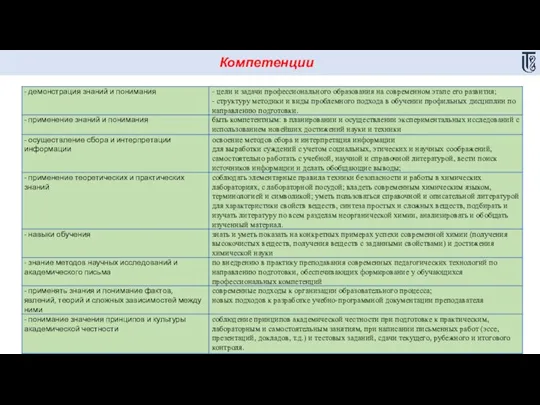
- 6. Компетенции
- 7. Академическая политика Академическая политика в НАО «Торайгыров университет» подразумевают обязательное соблюдение принципов Академической честности обучающимися, профессорско-преподавательским
- 8. Политика курса Посещение обучающимися всех очных аудиторных занятий без опозданий является обязательным. В случае пропуска занятия,
- 9. Политика курса Повторение темы и отработка пройденных материалов по каждому учебному занятию обязательны. Степень освоения учебных
- 10. Политика курса Обучающиеся должны посещать онлайн занятия, пропуски допускаются при уважительных причинах с условием обязательной отработки.
- 11. Лекция 1 Введение. Предмет изучения физической химии. Оралтаева Алмагуль Слямбековна [email protected]
- 12. План занятия Предмет физической химии. Основные разделы физической химии. Основные методы физической химии Основные агрегатные состояния
- 13. Что изучает физическая химия? Физическая химия изучает законы, управляющие химическими процессами, связь этих процессов со свойствами
- 14. Какие разделы включает Физическая химия ? 1). Строение вещества (раздел, в котором изучается взаимосвязь между строением
- 15. Основные методы физической химии 1) Квантово-механический метод (применяется к изучению структуры и свойств молекул, расчету химических
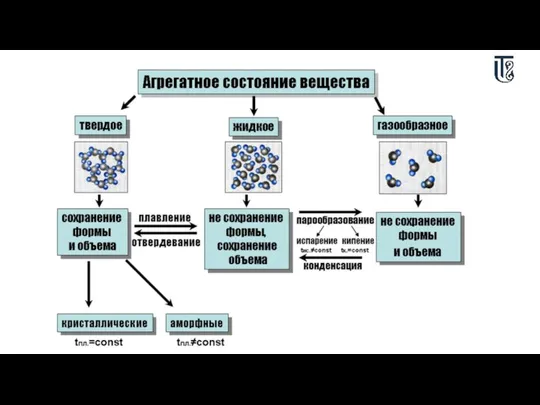
- 17. Основные агрегатные состояния веществ В зависимости от температуры и давления (условий) большинство веществ может находиться в
- 18. Строение твердых тел Молекулы твердых веществ образуют образуют твердую кристаллическую решетку. Расстояние межу молекулами очень малы
- 19. Строение жидкостей Молекулы жидкости расположены почти вплотную друг к другу , поэтому молекула жидкости ведет себя
- 20. Газообразные вещества В газах расстояние между атомами или молекулами в среднем во много раз больше размеров
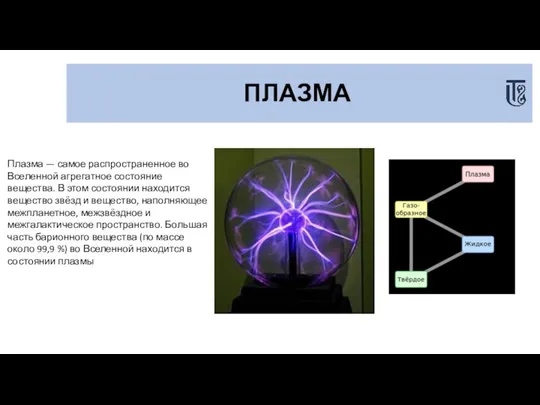
- 21. ПЛАЗМА Плазма — самое распространенное во Вселенной агрегатное состояние вещества. В этом состоянии находится вещество звёзд
- 22. Газовые законы Физическое состояние газов определяется тремя переменными (параметрами): давление (Р), температура (Т), объем (V). При
- 23. Вопросы для самоконтроля 1. Что изучает физическая химия? Разделы физической химии. 2. Основные методы физической химии.
- 25. Скачать презентацию


















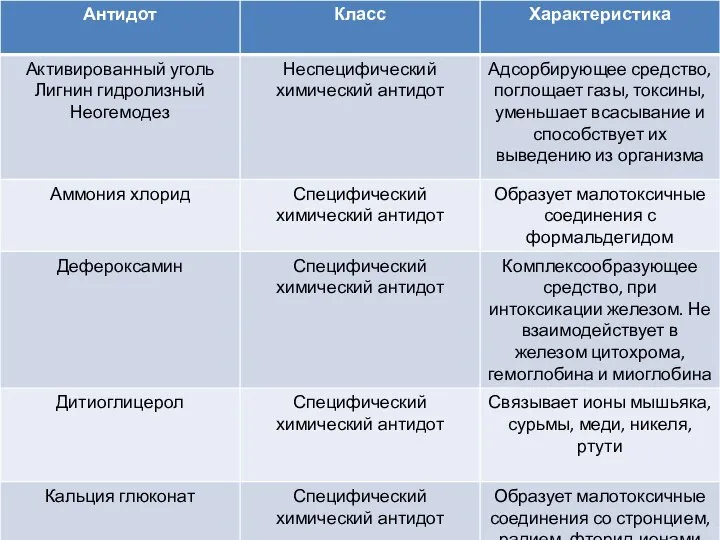 Антидоты. Класс. Характеристика
Антидоты. Класс. Характеристика valentnost
valentnost Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах
Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах Презентации 1 строение атома
Презентации 1 строение атома Наноматеріали. Тіт Лукрецій Кар
Наноматеріали. Тіт Лукрецій Кар Решение задач
Решение задач Bioenergetyka syntezy glutaminy
Bioenergetyka syntezy glutaminy Белки-1 2020
Белки-1 2020 Презентация на тему Коррозия
Презентация на тему Коррозия  Классификация и номенклатура ОС
Классификация и номенклатура ОС Электролитическая диссоциация
Электролитическая диссоциация Изменение химмотологических свойств цетанповышающей присадки в процессе хранения
Изменение химмотологических свойств цетанповышающей присадки в процессе хранения Homecredit Bank. Показатели и зоны роста
Homecredit Bank. Показатели и зоны роста Типы кристаллических решёток
Типы кристаллических решёток Алюминий
Алюминий Натрий, свойства атома, химические и физические свойства
Натрий, свойства атома, химические и физические свойства Определение Кофеина в Кофе
Определение Кофеина в Кофе Углеводороды. Алканы
Углеводороды. Алканы Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН
Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН Каучук негізіндегі материалдар
Каучук негізіндегі материалдар минералы_4_блеск
минералы_4_блеск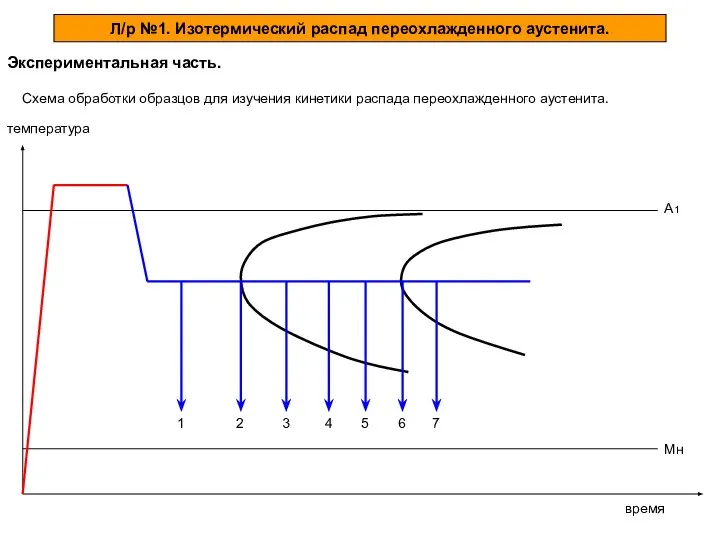 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Скорость протекания химических реакций
Скорость протекания химических реакций Составление формул по валентности. Понятие
Составление формул по валентности. Понятие Презентация на тему Гидролиз солей
Презентация на тему Гидролиз солей  Металлы
Металлы Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5
Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5 Вода-растворитель. Растворы
Вода-растворитель. Растворы