Содержание
- 2. Прав ли был Артур Конан-Дойл?
- 3. ...Да! Это была собака, огромная, черная, как смоль. Но такой собаки еще никто из нас, смертных,
- 4. Открытие фосфора Фосфор открывали несколько раз. Причем всякий раз получали его из … мочи. Есть упоминания
- 5. Строение атома фосфора
- 6. период Фосфор как химический элемент III группа VА валентных электронов 5 степени окисления -3, +3, +5
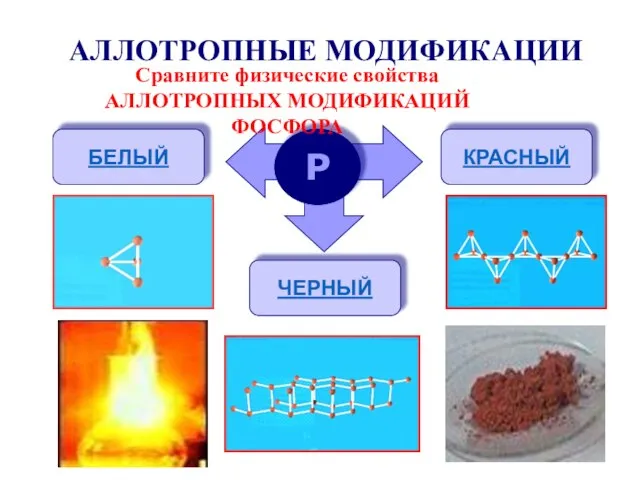
- 7. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ Р БЕЛЫЙ КРАСНЫЙ ЧЕРНЫЙ Сравните физические свойства АЛЛОТРОПНЫХ МОДИФИКАЦИЙ ФОСФОРА
- 8. Наиболее распространённые модификации: красный и белый (жёлтый)
- 9. Молекулы P4 имеют форму тетраэдра. Это легкоплавкое t(пл)=44,1оС, t(кип)=275оС, мягкое, бесцветное воскообразное вещество. Хорошо растворяется в
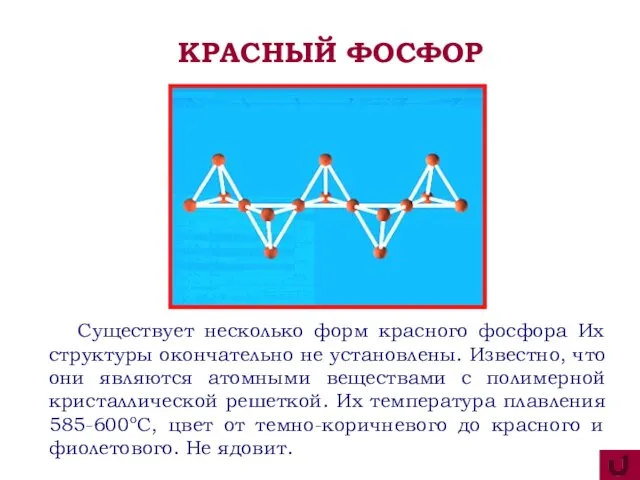
- 10. Существует несколько форм красного фосфора Их структуры окончательно не установлены. Известно, что они являются атомными веществами
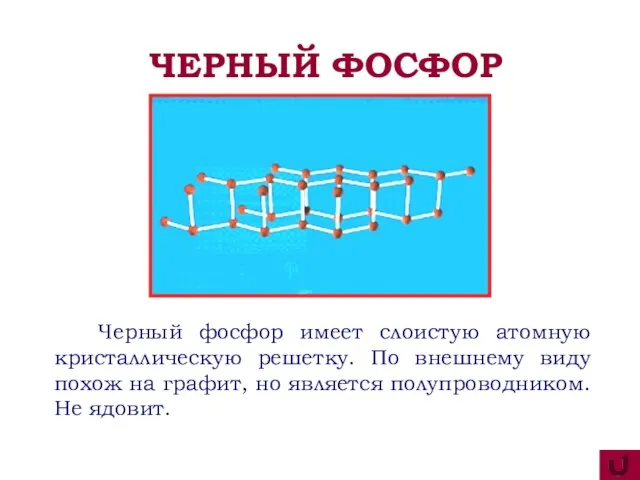
- 11. Черный фосфор имеет слоистую атомную кристаллическую решетку. По внешнему виду похож на графит, но является полупроводником.
- 13. 1.С металлами: 3Ca + 2P= Ca3 P2 фосфид кальция 2.C неметаллами: 4P + 5O2 =2P 2
- 14. 3. с бертолетовой солью при ударе взрывается, воспламеняется: KClO3 + P = P2O5 + KCl
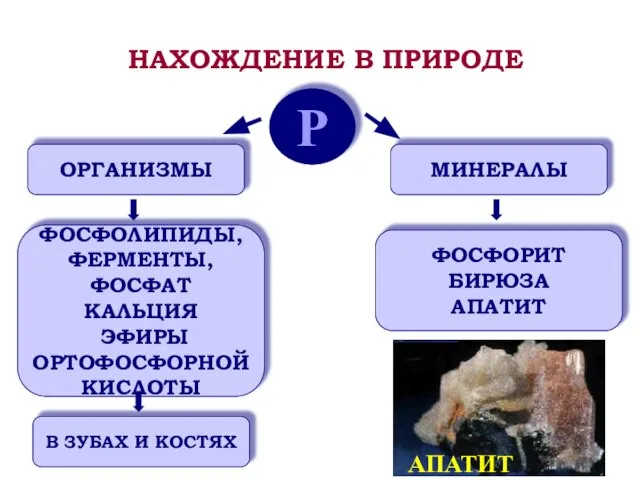
- 15. Р ОРГАНИЗМЫ МИНЕРАЛЫ ФОСФОЛИПИДЫ, ФЕРМЕНТЫ, ФОСФАТ КАЛЬЦИЯ ЭФИРЫ ОРТОФОСФОРНОЙ КИСЛОТЫ В ЗУБАХ И КОСТЯХ ФОСФОРИТ БИРЮЗА
- 16. Физиологическое действие белого фосфора Результат применения чрезмерного количества фосфора Появление лягушек с уродствами -результат применения фосфорных
- 17. Получение фосфора нагреванием смеси фосфорита, угля и песка в электропечи: Ca3(PO4)2 + C + SiO2 →
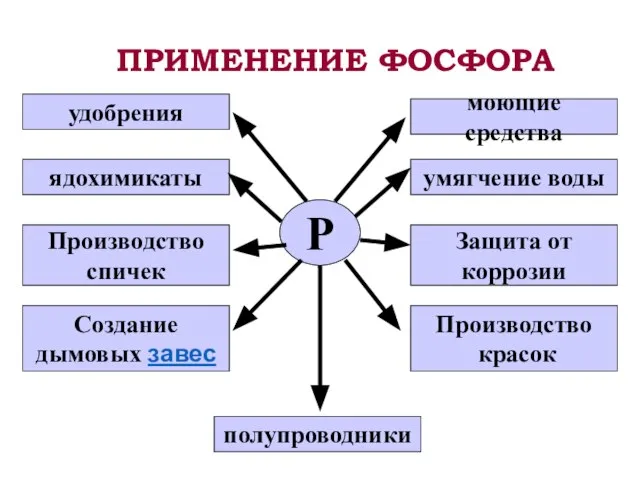
- 18. ПРИМЕНЕНИЕ ФОСФОРА Р удобрения ядохимикаты Производство спичек Создание дымовых завес полупроводники Производство красок Защита от коррозии
- 19. Биологическая роль фосфора Суточная потребность для взрослого человека 1 грамм Входит в состав скелета Входит в
- 20. Реакция организма на недостаток и избыток фосфора Недостаток Р Развивается заболевание рахит, снижается умственная и мышечная
- 25. Войска США использовали фосфорные Бомбы в Ираке, 2004 г.
- 26. ДОМАШНЕЕ ЗАДАНИЕ §21(Г.Е.Рудзитис) Индивидуальные задания. Подготовить сообщения: 1) об истории спичек; 2) о биологической роли фосфора
- 28. Скачать презентацию




















 Презентация на тему Азотная кислота и ее свойства
Презентация на тему Азотная кислота и ее свойства  Водород
Водород Получение метанола из синтез-газа
Получение метанола из синтез-газа Лекарственные средства – производные пиримидина
Лекарственные средства – производные пиримидина Chem-квест. Химический диктант
Chem-квест. Химический диктант Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини 9. Потомки светоносного элемента
9. Потомки светоносного элемента Химия - неотъемлемая часть жизни
Химия - неотъемлемая часть жизни Стратегия обучения решению задач по химии
Стратегия обучения решению задач по химии Вещество. Свойства вещества. Урок №2
Вещество. Свойства вещества. Урок №2 Ліпіди
Ліпіди Химия. 8 класс
Химия. 8 класс Презентация на тему Неорганические и органические основания
Презентация на тему Неорганические и органические основания  Товароведение и экспертиза пластических масс и изделий из них
Товароведение и экспертиза пластических масс и изделий из них Презентация на тему Свойства черных и цветных металлов
Презентация на тему Свойства черных и цветных металлов  Элемент протактиний
Элемент протактиний Виведення плям органічного походження
Виведення плям органічного походження Stereoselective total syntheses of guanacastepenes N and O
Stereoselective total syntheses of guanacastepenes N and O Растворы, растворимость
Растворы, растворимость Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды 01_Osnovnye_ponyatia_i_zakony_khimii
01_Osnovnye_ponyatia_i_zakony_khimii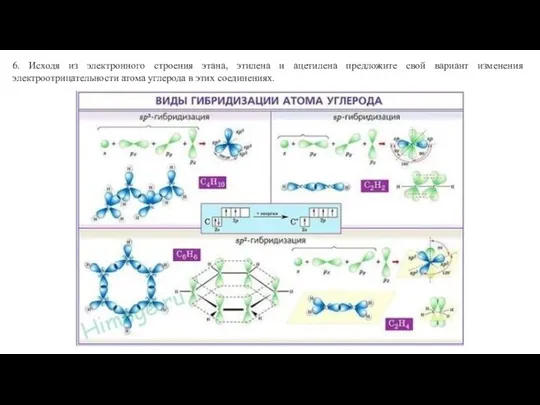 Виды гибридизации атома углерода
Виды гибридизации атома углерода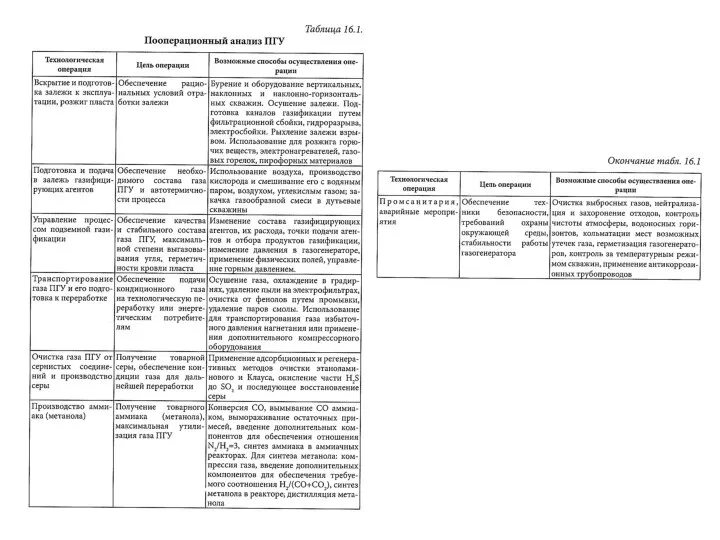 Пооперационный анализ ПГУ
Пооперационный анализ ПГУ Презентация на тему Вещества в твоей жизни
Презентация на тему Вещества в твоей жизни  Кислоты, соли
Кислоты, соли Золоторудное поле Дуэт
Золоторудное поле Дуэт Презентация по Химии "Незнайка в стране химия"
Презентация по Химии "Незнайка в стране химия"