Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды
Содержание
- 2. 1) Выпишите символы химических элементов-металлов и расположите их в порядке ослабления металлических свойств: I в: Cl;
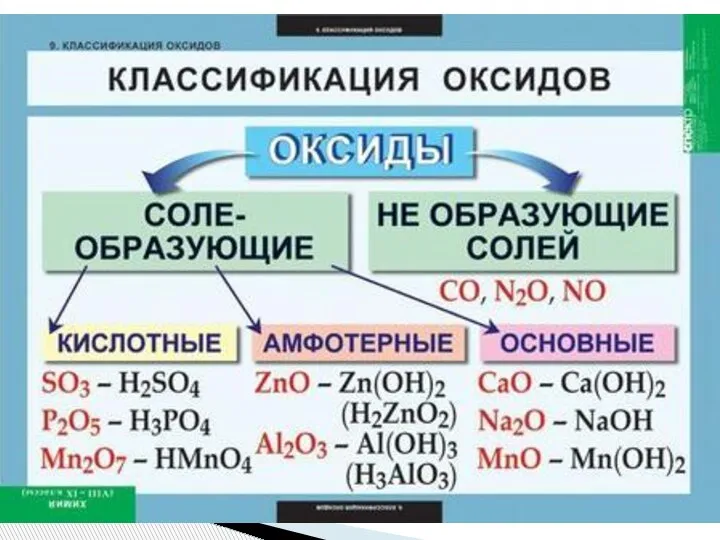
- 4. (кислородсодержащие кислоты) — гидроксиды неметаллов и металлов со степенью окисления +5, +6, +7, проявляющие кислотные свойства
- 5. гидроксиды металлов со степенью окисления +3, +4 и нескольких металлов со степенью окисления +2, которые проявляют
- 6. только гидроксиды металлов со степенью окисления +1, +2, проявляющие основные свойства (взаимодействуют с кислотами и кислотными
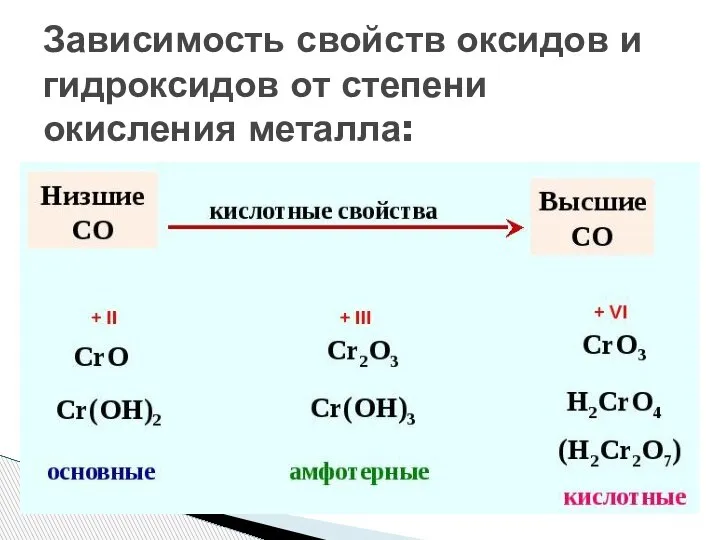
- 7. Зависимость свойств оксидов и гидроксидов от степени окисления металла:
- 9. Скачать презентацию




 Повторение классов соединений. Составление формул по названиям
Повторение классов соединений. Составление формул по названиям Презентация на тему Гигиенические аспекты загрязнения пищевых продуктов чужеродными веществами
Презентация на тему Гигиенические аспекты загрязнения пищевых продуктов чужеродными веществами  Презентация на тему Свойства черных и цветных металлов
Презентация на тему Свойства черных и цветных металлов  Кислотно-основное равновесие
Кислотно-основное равновесие Алкины. Химические свойства
Алкины. Химические свойства Презентация на тему Химический алфавит
Презентация на тему Химический алфавит  Презентация на тему Применение солей в быту
Презентация на тему Применение солей в быту  Составление ионных уравнений
Составление ионных уравнений Кислоты. Домашнее задание
Кислоты. Домашнее задание Абсорбционная осушка газа
Абсорбционная осушка газа Решение расчетных задач по химии
Решение расчетных задач по химии Ароматические вещества и их значение для человека
Ароматические вещества и их значение для человека Фенол. Понятие о фенолах
Фенол. Понятие о фенолах Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Атом. Будова атома
Атом. Будова атома физические и химические явления
физические и химические явления Воздух и его свойства
Воздух и его свойства Алкины. Понятие об алкинах
Алкины. Понятие об алкинах Строение и свойства металлов. Материаловедение. Лекция 1
Строение и свойства металлов. Материаловедение. Лекция 1 Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине Явления, происходящие с веществами
Явления, происходящие с веществами Диффузия в газах, жидкостях и твердых телах
Диффузия в газах, жидкостях и твердых телах Решение заданий ОГЭ по химии (1 - 15)
Решение заданий ОГЭ по химии (1 - 15) Хроматография
Хроматография Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Приобретённые: недостаточность митохондрий,
Приобретённые: недостаточность митохондрий, Белки
Белки Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ