Содержание
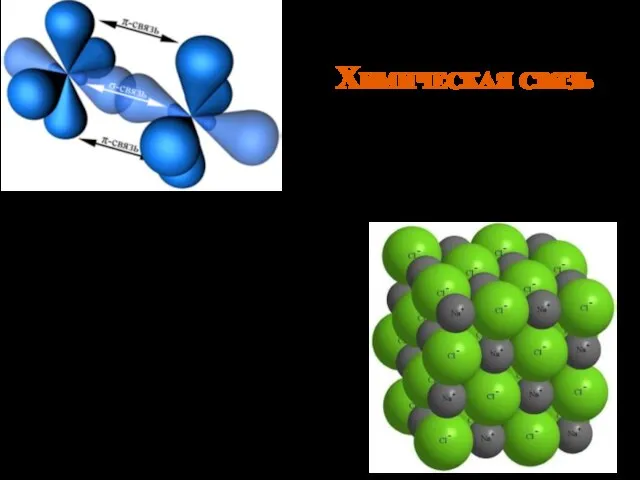
- 2. Химическая связь Под химической связью понимают такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы,
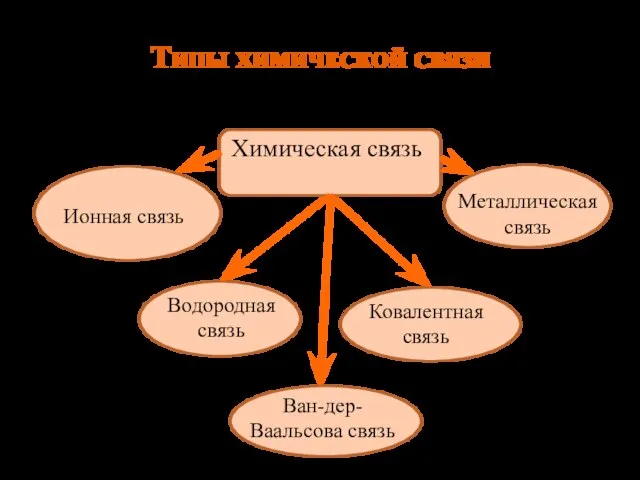
- 3. Типы химической связи Химическая связь Ионная связь Металлическая связь Водородная связь Ковалентная связь Ван-дер-Ваальсова связь
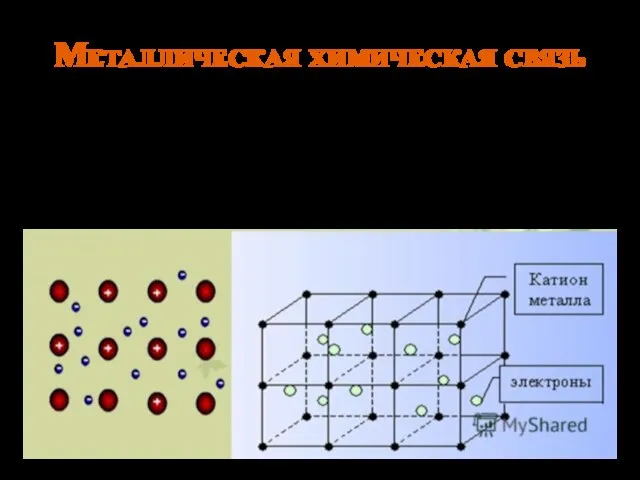
- 4. Металлическая химическая связь Связь, которую осуществляют относительно свободные электроны между ионами или атомами металлов в кристаллической
- 5. Особенности металлической связи Металлическую связь образуют элементы, атомы которых на внешнем уровне имеют мало валентных электронов
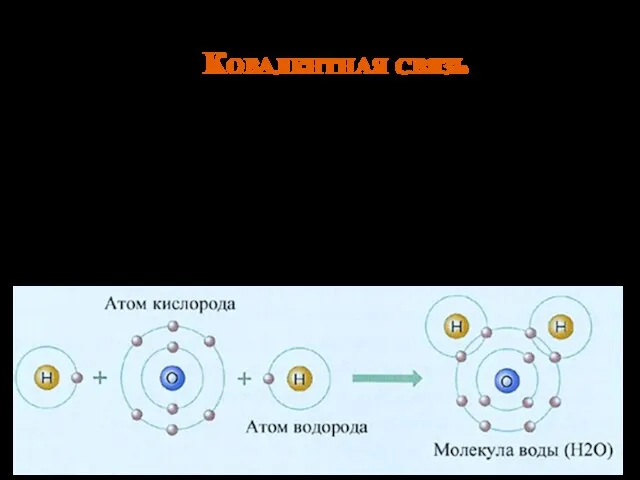
- 6. Ковалентная связь Ковалентная связь – это связь, возникающая между атомами за счет образования общих электронных пар.
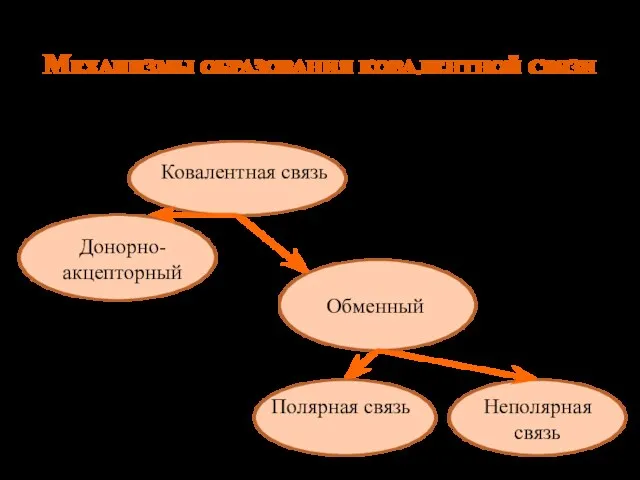
- 7. Механизмы образования ковалентной связи Ковалентная связь Донорно-акцепторный Обменный Полярная связь Неполярная связь Обменный механизм за счет
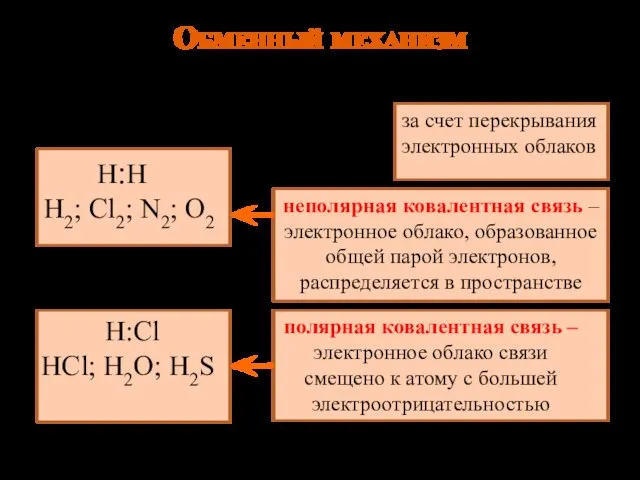
- 8. Обменный механизм за счет перекрывания электронных облаков Н:Н Н2; Cl2; N2; O2 неполярная ковалентная связь –
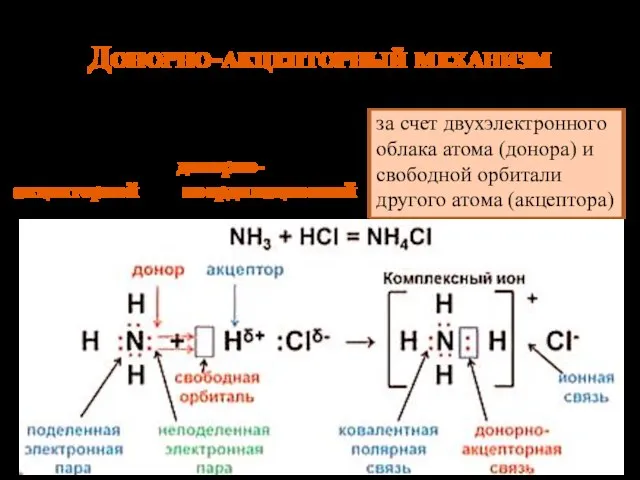
- 9. Донорно-акцепторный механизм за счет двухэлектронного облака атома (донора) и свободной орбитали другого атома (акцептора) Связь называется
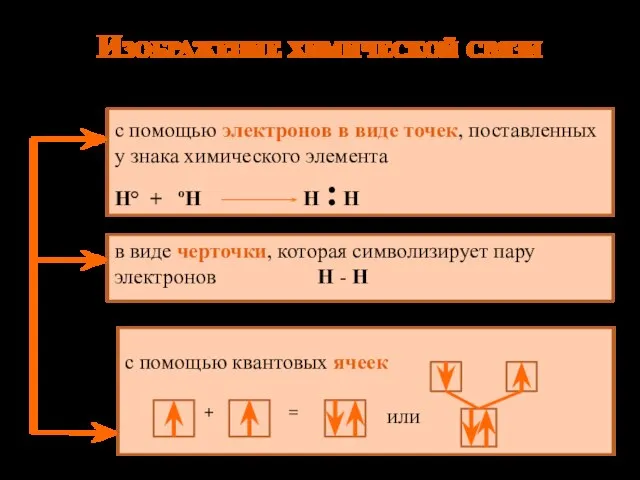
- 10. Изображение химической связи с помощью электронов в виде точек, поставленных у знака химического элемента Н° +
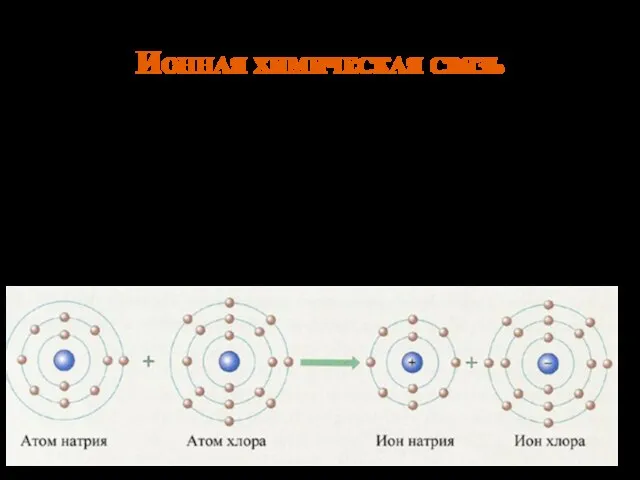
- 11. Ионная химическая связь Ионная связь – химическая связь между ионами, осуществляемая электростатическим притяжением. Образуется между атомами,
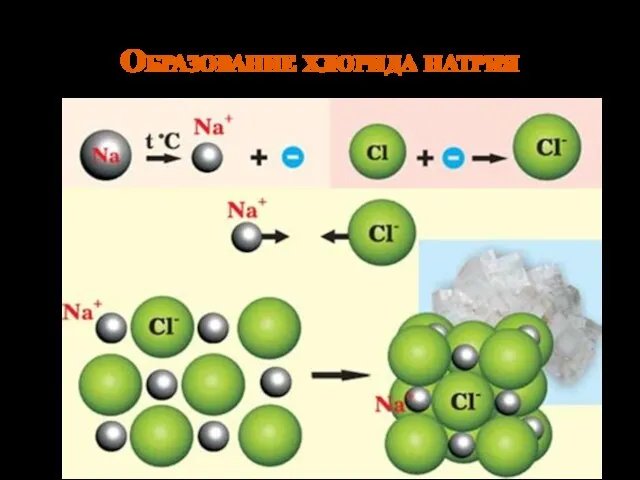
- 12. Образование хлорида натрия
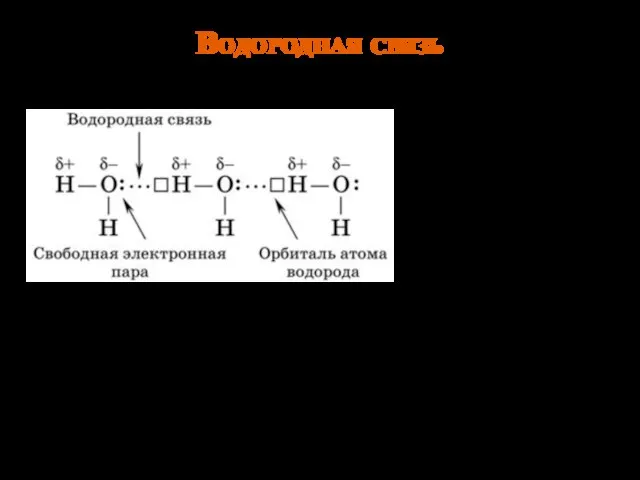
- 13. Водородная связь Связь между атомом водорода , соединенным с атомом сильно электроотрицательного элемента, одной молекулы и
- 14. Особенности водородной связи Связь относится к межмолекулярной; возможно образование внутримолекулярной водородной связи. Водородная связь слабая. Тем
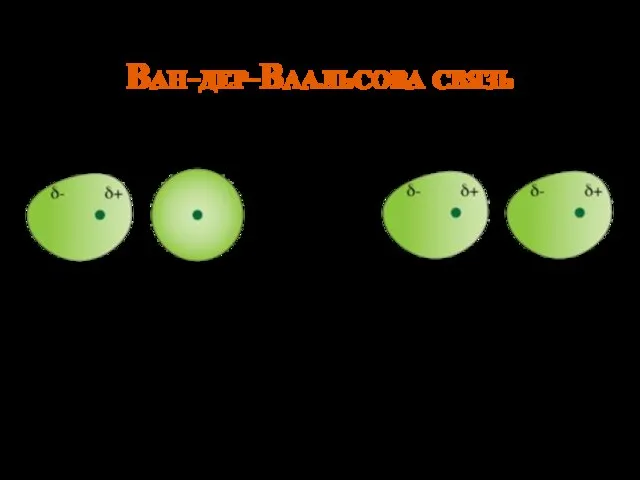
- 15. Ван-дер-Ваальсова связь
- 18. Скачать презентацию


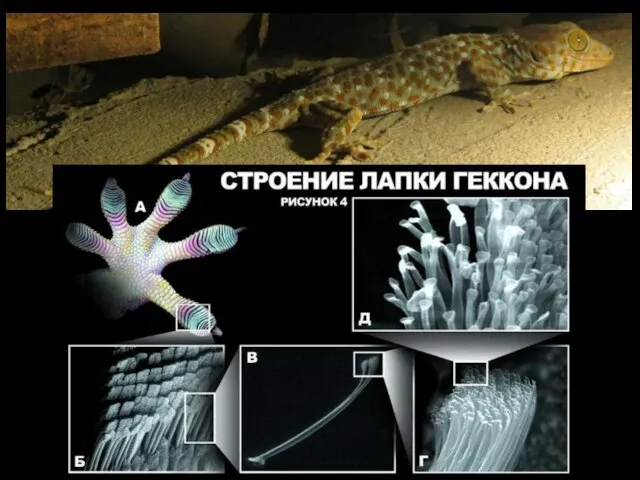
 Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом
Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом Спирты. Классификация, изомерия
Спирты. Классификация, изомерия Нуклеирующие добавки
Нуклеирующие добавки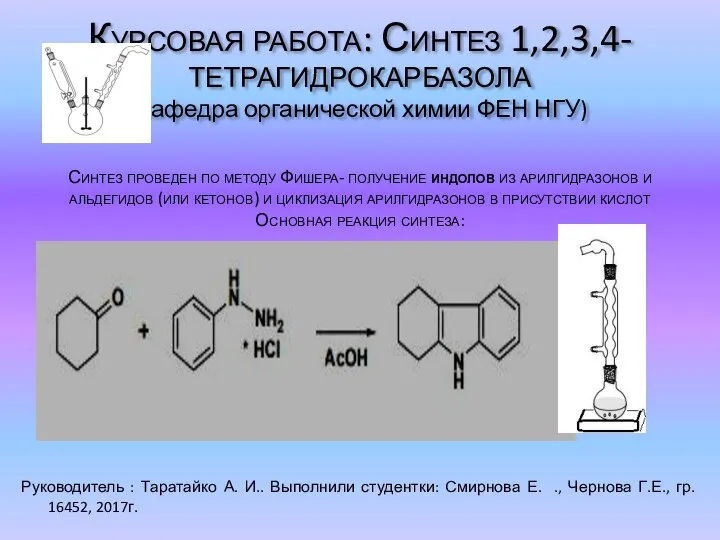 Синтез 1,2,3,4-тетрагидрокарбазола
Синтез 1,2,3,4-тетрагидрокарбазола Основные особенности процессов растворения твёрдых веществ
Основные особенности процессов растворения твёрдых веществ Реакции ионного обмена. Электролитическая диссоциация
Реакции ионного обмена. Электролитическая диссоциация Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл.
Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл. Презентация на тему Жидкий металл - ртуть
Презентация на тему Жидкий металл - ртуть 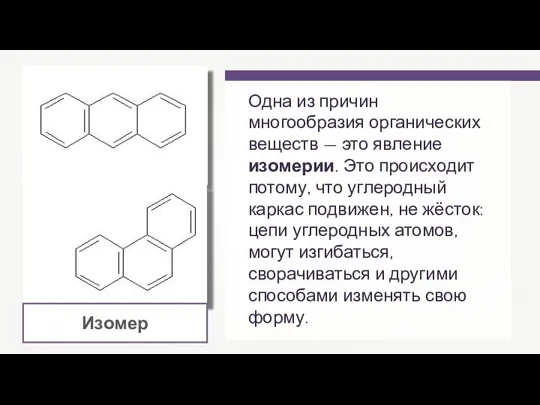 Номенклатура и изомерия алкенов
Номенклатура и изомерия алкенов Серная кислота. Свойства серной кислоты
Серная кислота. Свойства серной кислоты Химия и сельское хозяйство
Химия и сельское хозяйство prezentatsiya-po-fizike-7-klass-tri-agregatnyh-sostoyaniya-veshchestva
prezentatsiya-po-fizike-7-klass-tri-agregatnyh-sostoyaniya-veshchestva Презентация на тему Химические средства гигиены и косметика
Презентация на тему Химические средства гигиены и косметика  Общие вопросы материаловедения
Общие вопросы материаловедения Углеводы (Сахариды)
Углеводы (Сахариды)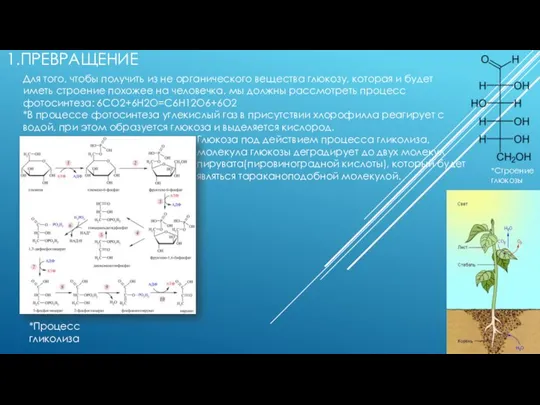 Превращение из не органического вещества в глюкозу
Превращение из не органического вещества в глюкозу Alkalické kovy
Alkalické kovy Многообразие органических веществ
Многообразие органических веществ Электрохимические процессы
Электрохимические процессы Силикатная промышленность
Силикатная промышленность Презентация на тему Органическая химия
Презентация на тему Органическая химия  Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Растворы электролитов
Растворы электролитов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой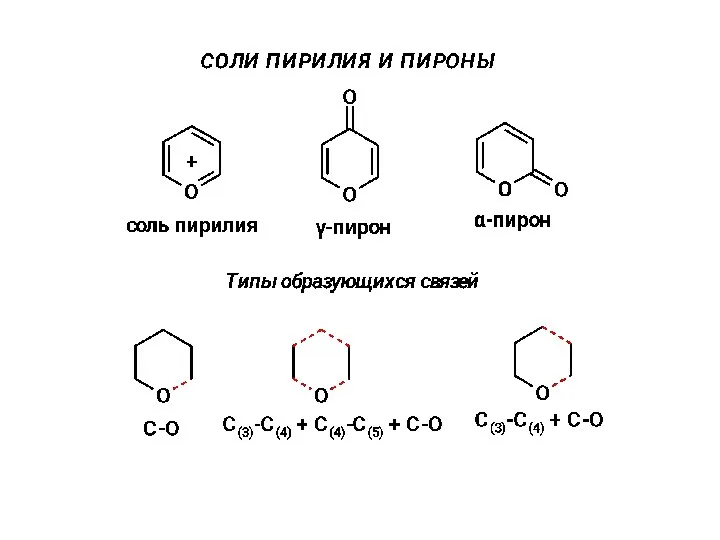 Соли пирилия и пироны
Соли пирилия и пироны Простые вещества - неметаллы
Простые вещества - неметаллы Соединения Ca и Mg, представителей элементов II группы главной подгруппы
Соединения Ca и Mg, представителей элементов II группы главной подгруппы Образовательные технологии, используемые на уроках химии для повышения мотивации обучения
Образовательные технологии, используемые на уроках химии для повышения мотивации обучения