Содержание
- 2. Что читать? Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. Ахметов Н. С. Общая
- 3. Закон Ломоносова-Клапейрона Уравнение состояния идеального газа: PV = nRT где n – число молей газа; P
- 4. Система СИ Уравнение состояния идеального газа: PV = nRT где n – число молей газа; P
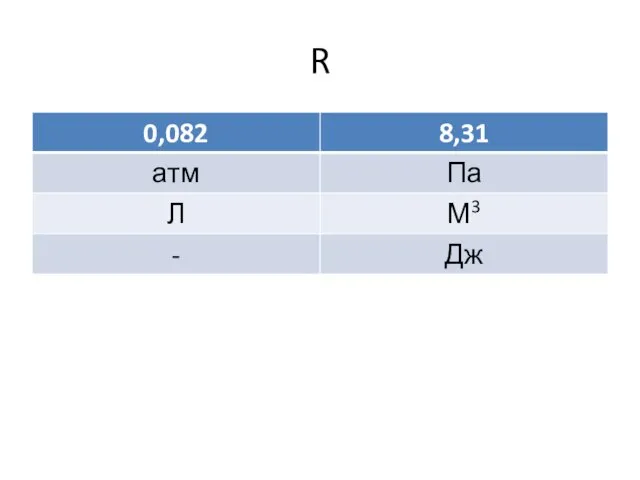
- 5. R
- 6. 1 моль газа занимает объем 22,4 литра при 1 атмосфере и 0 OС (273,15 К) (н.у)
- 7. Различные толкования ст. у. Ст. у. в современной химической термодинамике не привязаны к температуре, и соответствуют
- 8. В наших учебниках и задачках Стандартные условия (ст. у.) – температура 25 °С (298,15 К, сотые
- 9. Энтропия S Мера хаоса (не совсем верно/понятно) Мера возможностей системы
- 11. S, S°, ΔS.
- 13. Скачать презентацию









 Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Магний и кальций
Магний и кальций Свойства белков
Свойства белков Жидкая углекислота
Жидкая углекислота Презентация на тему Кристаллическая решетка
Презентация на тему Кристаллическая решетка  Электронное и пространственное строение алкенов. Гомология и изомерия алкенов
Электронное и пространственное строение алкенов. Гомология и изомерия алкенов Нитробактерии. Нитратное дыхание
Нитробактерии. Нитратное дыхание Про краски
Про краски Вероятность протекания химических реакций
Вероятность протекания химических реакций Природные источники углеводородов
Природные источники углеводородов Типы загрязнений биосферы
Типы загрязнений биосферы Степень окисления
Степень окисления Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Силикатная промышленность
Силикатная промышленность Аллотропия Аллотропные видоизменения (модификации)
Аллотропия Аллотропные видоизменения (модификации) Кислоты в химии
Кислоты в химии Состав и строение атома. Изотопы
Состав и строение атома. Изотопы Количество вещества. Моль
Количество вещества. Моль Методи визначення корозійної стійкості матеріалів (тема 11)
Методи визначення корозійної стійкості матеріалів (тема 11) Классификация органических соединений. 10 класс
Классификация органических соединений. 10 класс Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка
Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка Характеристика элемента по Периодической системе Д.И. Менделеева
Характеристика элемента по Периодической системе Д.И. Менделеева Презентация на тему Химический состав клетки: ультрамикроэлементы
Презентация на тему Химический состав клетки: ультрамикроэлементы  Получение серной кислоты
Получение серной кислоты Искусство фотографии и химия
Искусство фотографии и химия Предмет органической химии
Предмет органической химии Химия и география. Викторина
Химия и география. Викторина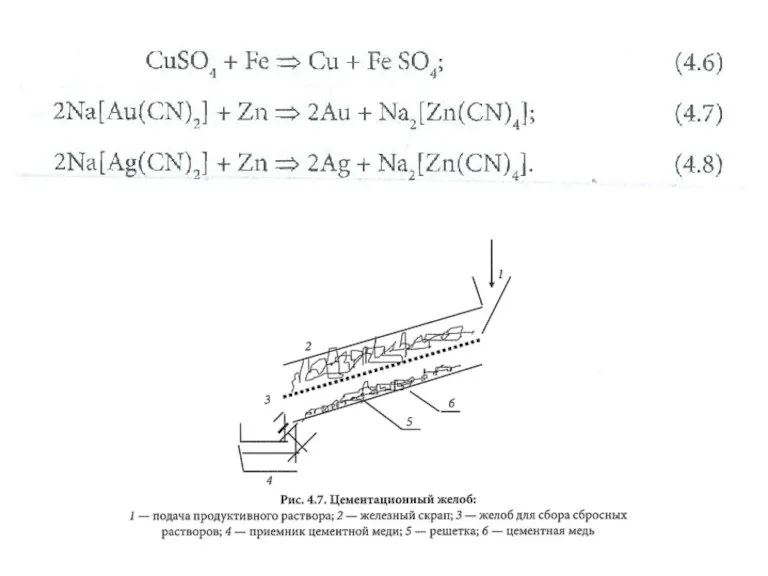 Гальванохимическая очистка. Сорбция
Гальванохимическая очистка. Сорбция