Содержание
- 2. Тема урока: Фосфорная кислота и ее свойства.
- 3. Сегодня на уроке мы должны: Образовательные: Изучить физические и химические свойства фосфорной кислоты через проведение химического
- 4. Сегодня на уроке мы должны: План: 1. Молекулярная формула фосфорной кислоты. 2. Получение и физические свойства.
- 5. Р2O5 H3РO4 Ст/о (Р) = + 5
- 6. Молекулярная формула фосфорной кислоты и физические свойства: твердое бесцветное, кристаллическое вещество, хорошо растворимое в воде в
- 7. Производство фосфорной кислоты. а) Горение фосфора в ложечке, которую вносят в колбу. 2Р+5О2 = Р2О5 После
- 8. Химические свойства общие с другими кислотами: Водный раствор кислоты изменяет окраску индикаторов. Диссоциирует в 3 ступени:
- 9. Специфические свойства фосфорной кислоты: 6 а) При нагревании постепенно превращается в метафосфорную кислоту 2Н3РО4 = Н4Р2О7
- 10. H3РO4
- 11. Выберите вещества с которыми будет реагировать фосфорная кислота: КОН, Си, К2SО3, СО2, NО? 2. Какому молекулярному
- 13. Скачать презентацию








 Стекло. История открытия. Самое древнее производство Эпохи фараонов
Стекло. История открытия. Самое древнее производство Эпохи фараонов Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Подготовка к ГИА по химии
Подготовка к ГИА по химии Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Гидроксиды металлов
Гидроксиды металлов Химические равновесия в растворах. Лекция 2 часть 2
Химические равновесия в растворах. Лекция 2 часть 2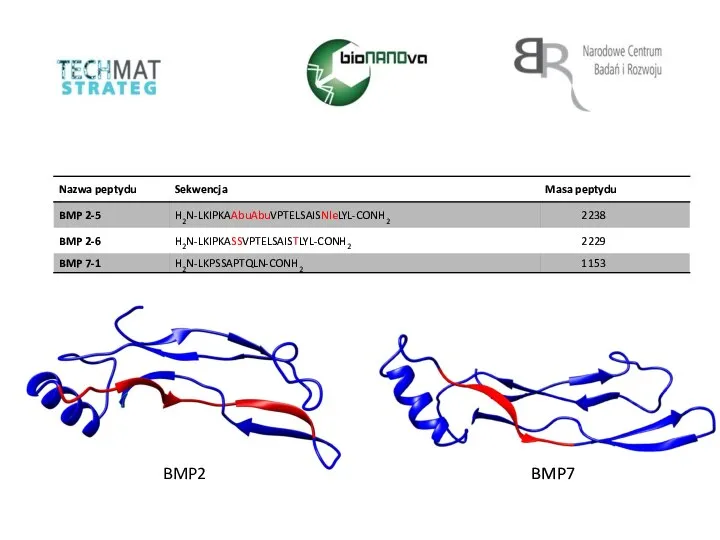 Nazwa peptydu. Sekwencja
Nazwa peptydu. Sekwencja Полімери. Пінополістирол
Полімери. Пінополістирол 5 группа элементов
5 группа элементов Химические свойства насыщенных альдегидов и кетонов (продолжение)
Химические свойства насыщенных альдегидов и кетонов (продолжение) Водородная химическая связь
Водородная химическая связь Коррозия. способы защиты от коррозии
Коррозия. способы защиты от коррозии Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Электролиз воды
Электролиз воды Генетические ряды углеводородов. Обобщение и систематизация знаний
Генетические ряды углеводородов. Обобщение и систематизация знаний Адсорбционные материалы. Цеолиты
Адсорбционные материалы. Цеолиты Химическая термодинамика
Химическая термодинамика Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Физическая химия. Вводная лекция
Физическая химия. Вводная лекция Строение вещества. ОВР. Окислительно-восстановительные реакции
Строение вещества. ОВР. Окислительно-восстановительные реакции Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C
Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C Мыльная история
Мыльная история Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства алотропні модифікації неметалів
алотропні модифікації неметалів Презентация для заочников
Презентация для заочников Генетическая связь неорганических соединений
Генетическая связь неорганических соединений Алкины. Понятие об алкинах
Алкины. Понятие об алкинах