Слайд 2Основные свойства
Чем большим радиусом атома обладает химический элемент, тем он проявляет более

сильные металлические свойства, и тем более сильными основными свойствами обладают его соединения.
Основные свойства веществ проявляются во взаимодействии их с кислотами, кислотными оксидами, амфотерными оксидами и основаниями, а также некоторыми неметаллами (в определённых условиях).
Слайд 3Li Li2O LiOH
Na Na2O NaOH
K K2O KOH
Mg MgO Mg(OH)2
Ca CaO Ca(OH)2
Cr CrO

Cr(OH)2
Основные свойства проявляют оксиды (М2О и МО) и гидроксиды металлов (МОН и М(ОН)2)в степени окисления +1 и +2 (за исключением Be и Zn)
Слайд 4Кислотные свойства
Чем меньше радиус атома химического элемента, тем он проявляет более сильные

неметаллические свойства, и тем более сильными кислотными свойствами обладают его соединения.
Кислотные свойства обратны основным
Слайд 5P P2O5 H3PO4
S SO3 H2SO4
Cl2 Cl2O7 HClO4
V V2O5 HVO3
Cr CrO3 H2CrO4
Кислотные свойства

проявляют оксиды и гидроксиды неметаллов в степени окисления ≥+3, а также оксиды и гидроксиды металлов в степени окисления ≥+5
Слайд 6Амфотерные свойства
Проявляют химические элементы, которые занимают промежуточное (граничное) положение между типичными металлами

и типичными неметаллами, амфотерны и их соединения.
Амфотерность заключается во взаимодействии данных веществ (оксидов, гидроксидов) как с сильными основаниями (основными оксидами) так и кислотами (кислотными оксидами).
Слайд 7Be BeO Be(OH)2
Zn ZnO Zn(OH)2
Al Al2O3 Al(OH)3
Fe Fe2O3 Fe(OH)3
Cr Cr2O3 Cr(OH)3
Mn MnO2

Mn(OH)4
Амфотерные свойства проявляют оксиды и гидроксиды металлов в степени окисления +3, +4, а также соединения Be и Zn.
Слайд 8Основные свойства
Na2O + 2HCl = 2NaCl + H2O
Na2O + SO2 = Na2SO3
NaOH
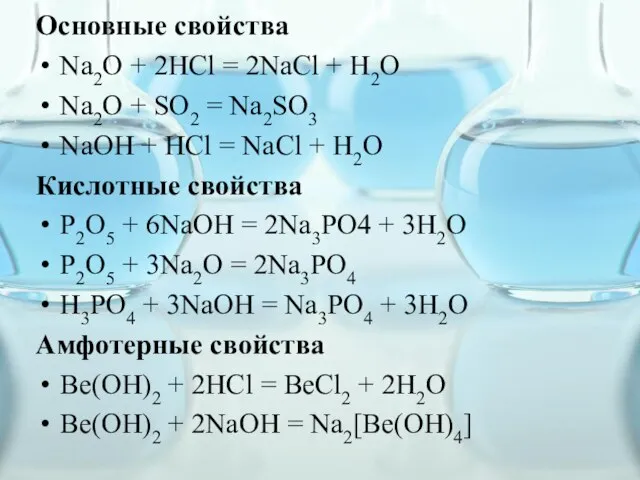
+ HCl = NaCl + H2O
Кислотные свойства
P2O5 + 6NaOH = 2Na3PO4 + 3H2O
P2O5 + 3Na2O = 2Na3PO4
H3PO4 + 3NaOH = Na3PO4 + 3H2O
Амфотерные свойства
Be(OH)2 + 2HCl = BeCl2 + 2H2O
Be(OH)2 + 2NaOH = Na2[Be(OH)4]
Слайд 9У химических элементов, которые проявляют множество степеней окисления для нижних характерны основные

свойства, для промежуточных – амфотерные, для высоких – кислотные. Например, Cr:
Слайд 10Амфотерность Zn(OH)2
Используя, выданные реактивы, получите гидроксид цинка и докажите его амфотерность путём

проведения соответствующих химических реакций.
Запишите в тетрадь уравнения проведённых химических реакций в молекулярном виде, а дома допишите их в полном и сокращённом ионном виде.









 Химическая кинетика и равновесие
Химическая кинетика и равновесие Окислительно-восстановительные реакции, 9 класс
Окислительно-восстановительные реакции, 9 класс Твердые электролиты
Твердые электролиты Nanofibers of aluminum oxide
Nanofibers of aluminum oxide Введение в хроматографию. Хроматографические методы анализа
Введение в хроматографию. Хроматографические методы анализа Металлы
Металлы Составление формул оксидов, оснований, солей
Составление формул оксидов, оснований, солей 10 класс Алкадиены более совершенная (2)
10 класс Алкадиены более совершенная (2) Химическая связь
Химическая связь Презентация на тему Типы химических реакций (8 класс)
Презентация на тему Типы химических реакций (8 класс)  Экстракционное разделение радионуклидов
Экстракционное разделение радионуклидов Проточные реакторы непрерывного действия. (Лекция 5)
Проточные реакторы непрерывного действия. (Лекция 5) Алкены
Алкены Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства  Арены. Бензол
Арены. Бензол Изменения, происходящие с веществами
Изменения, происходящие с веществами Железо
Железо Диффузия и осмос
Диффузия и осмос Соли как производные кислот и оснований. Их состав и названия
Соли как производные кислот и оснований. Их состав и названия Занимательная химия Программу составил
Занимательная химия Программу составил  Строение атома
Строение атома Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Соли. Классификация солей
Соли. Классификация солей Геохимический барьер
Геохимический барьер 5 Нефть. Нефтепереработка. Конверсия метана
5 Нефть. Нефтепереработка. Конверсия метана Ліпіди
Ліпіди Электролиз растворов и расплавов неорганических и органических электролитов
Электролиз растворов и расплавов неорганических и органических электролитов Строение и номенклатура карбонильных соединений
Строение и номенклатура карбонильных соединений