Слайд 2№2
Оснóвные свойства оксидов уменьшаются в ряду
Ответ:
Li2O → Na2O → K2O
BaO → SrO → CaO
FeO → K2O → MgO
Al2O3 → Na2O → MgO

Слайд 3№3
Верны ли следующие суждения о металлах и их соединениях?
А. Восстановительные свойства у калия

выражены сильнее, чем у магния.
Б. Высшие оксиды металлов IA группы имеют состав R2O.
Ответ:
верно только А
верно только Б
верны оба суждения
оба суждения неверны
Слайд 4№5
Ковалентную полярную связь имеет каждое из двух веществ:
Ответ:
CS2 и PCl3
K и KOH
H2SO4 и S8
KH

и H2O
Слайд 5№6
Молекулярное строение имеет
Ответ:
сульфид калия
оксид бария
хлороводород
оксид кальция

Слайд 6№7
Среди перечисленных веществ:
к оснóвным оксидам относят:

Слайд 7№8
С водой при комнатной температуре может реагировать каждый из двух металлов:
Ответ:
барий и

медь
алюминий и ртуть
кальций и литий
натрий и серебро
Слайд 8№9
Оксид серы(IV) взаимодействует с
Ответ:
азотом
оксидом углерода(IV)
соляной кислотой
гидроксидом калия

Слайд 9№10
Гидроксид цинка взаимодействует с каждым из двух веществ:
Ответ:
HCl и NaOH
HNO3 и NaCl
Mg(OH)2 и NaNO3
H2S и Fe(OH)2

Слайд 10№11
Практически осуществима реакция между растворами
Ответ:
FeSO4 и KCl
Ca(NO3)2 и K2CO3
K2S и NaCl
MgCl2 и Fe(NO3)2

Слайд 11№12
В схеме превращений
CuO→ X1 → X2 → Cu(OH)2
веществами Х1 и Х2 являются соответственно
Ответ:
Cu(OH)2 и CuSO4
CuSO4 и CuCl2
Cu(OH)2 и CuCl2
CuCO3 и Cu3(PO4)2

Слайд 12№13
При взаимодействии пентена-1 с хлороводородом преимущественно образуется
Ответ:
1-хлорпентан
2-хлорпентан
2-хлорпентен
1,2-дихлорпентан

Слайд 13№14
Бутанол-1 образует сложный эфир при взаимодействии с
Ответ:
пропанолом
метаналем
муравьиной кислотой
соляной кислотой

Слайд 14№15
Верны ли следующие суждения о свойствах указанных кислородсодержащих органических соединений?
А. Метаналь взаимодействует с

гидроксидом меди(II).
Б. Муравьиная кислота вступает в реакцию «серебряного зеркала».
Ответ:
верно только А
верно только Б
верны оба суждения
оба суждения неверны
Слайд 15№16
Ацетилен в лаборатории получают
Ответ:
дегидрированием метана
дегидрогалогенированием дихлорэтана
гидролизом карбида алюминия
гидролизом карбида кальция

Слайд 16№17
Взаимодействие пропилена с бромом при обычных условиях относится к реакциям
Ответ:
присоединения
замещения
гидрогенизации
изомеризации

Слайд 17№18
Скорость реакции окисления оксида серы(IV) уменьшается при
Ответ:
использовании катализатора
понижении температуры
увеличении концентрации кислорода
увеличении давления

Слайд 18№19
Химическое равновесие в системе
2CO(г) ⇄ CO2(г) + C(тв) + 173 кДж
смещается в сторону продуктов реакции при
Ответ:
повышении давления
повышении

температуры
понижении давления
использовании катализатора
Слайд 19№20
Сульфат-ионы образуются при диссоциации вещества, формула которого
Ответ:
Na2SO4
H2SO3
Na2S
KHSO3

Слайд 20№21
Реакция обмена между растворами соляной кислоты и гидроксида бария проходит до конца

в результате взаимодействия ионов
Ответ:
Ba2+ и Сl−
Ba2+ и Н+
OH− и Ba2+
OH− и H+
Слайд 21№22
Какая соль не подвергается гидролизу?
Ответ:
сульфит натрия
карбонат натрия
сульфат натрия
ацетат натрия

Слайд 22№23
Свойства восстановителя кремний проявляет в реакции, уравнение которой
Ответ:
SiO2+2Mg=2MgO+SiSiO2+2Mg=2MgO+Si
Si+O2=SiO2Si+O2=SiO2
SiO2+4Mg=Mg2Si+2MgOSiO2+4Mg=Mg2Si+2MgO
H2SiО3=SiO2+H2O

Слайд 23№24
Нетоксичным является каждое из двух веществ:
Ответ:
H2 и C6H5OH
O2 и N2
Cl2 и H2S
CO и NH3
Слайд 24№25
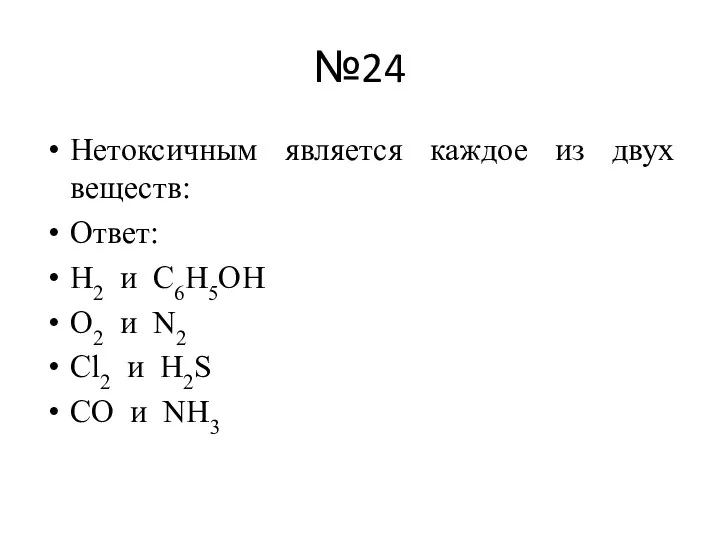
Установите соответствие между формулой вещества и реагентами, с каждым из которых это
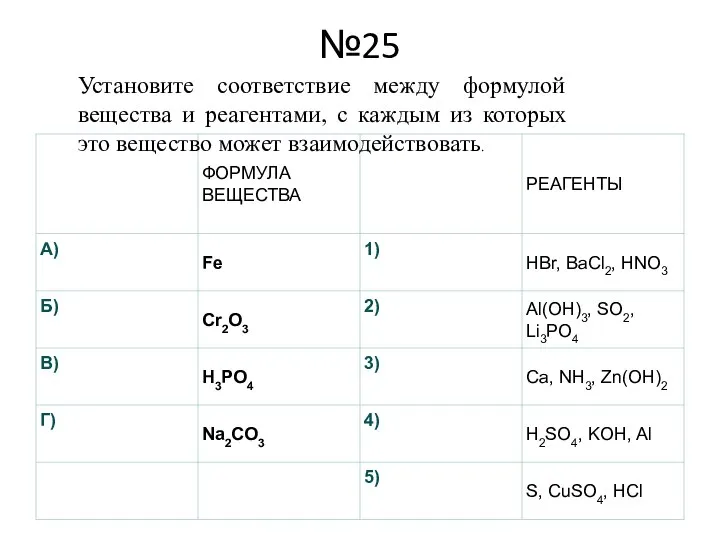
вещество может взаимодействовать.
Слайд 25№26
В отличие от бутана, бутадиен-1,3 вступает в реакции
Ответ:
горения
хлорирования
полимеризации
с бромоводородом
с раствором перманганата калия
с

аммиачным раствором оксида серебра
Слайд 26№27
Для пропанола характерна(-о):
Ответ:
sp2-гибридизация атомов углерода
твёрдое агрегатное состояние (н.у.)
существование изомеров
взаимодействие с натрием
реакция полимеризации
реакция

этерификации
Слайд 27№28
И диметиламин, и анилин взаимодействуют с
Ответ:
хлоридом кальция
гидроксидом натрия
бромоводородом
кислородом
серной кислотой
сульфатом железа(II)

Слайд 28№29
Смешали 80 г раствора с массовой долей нитрата натрия 25% и 20

г раствора этой же соли с массовой долей 40%. Массовая доля соли в полученном растворе равна ___________%. (Запишите число с точностью до целых.)
Слайд 29№30
Карбид алюминия массой 8,64 г растворили в избытке соляной кислоты. Объём (н.у) газа, выделившегося

при этом, составил ________ л. (Запишите число с точностью до целых.)
Слайд 30№31
Используя метод электронного баланса, составьте уравнение реакции:
FeSO4 + KClO3 + … → Fe2(SO4)3 + … + H2O
Определите окислитель и

восстановитель.
Слайд 31№32
Оксид хрома(VI) прореагировал с гидроксидом калия. Полученное вещество обработали серной кислотой, из

образовавшегося раствора выделили соль оранжевого цвета. Эту соль обработали бромоводородной кислотой. Полученное простое вещество вступило в реакцию с сероводородом.
Напишите уравнения четырёх описанных реакций.
Слайд 32№33
Верны ли следующие суждения о процессе обжига колчедана при производстве серной кислоты?
Ответ:
верно

только А
верно только Б
верны оба суждения
оба суждения неверны
Слайд 33№34
В соответствии с термохимическим уравнением реакции
СН4(г) + 2О2(г) = СО2(г) + 2Н2О(г) + 896 кДж
89,6 кДж теплоты

выделится при горении метана количеством вещества
Ответ:
0,1 моль
0,2 моль
0,25 моль
0,5 моль
Слайд 34№35
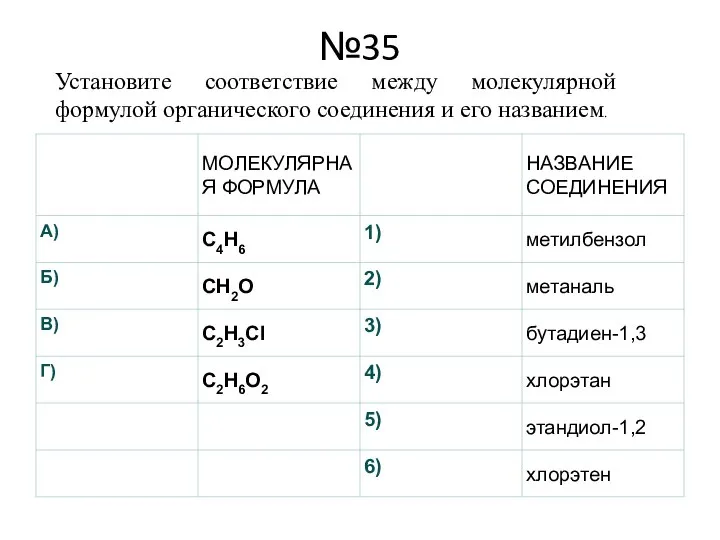
Установите соответствие между молекулярной формулой органического соединения и его названием.
Слайд 35№36
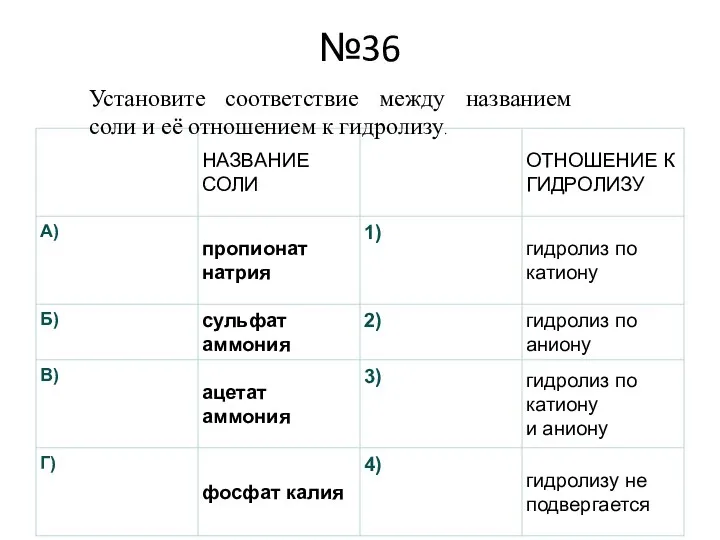
Установите соответствие между названием соли и её отношением к гидролизу.
Слайд 36№37
Оксид хрома(VI) прореагировал с гидроксидом калия. Полученное вещество обработали серной кислотой, из

образовавшегося раствора выделили соль оранжевого цвета. Эту соль обработали бромоводородной кислотой. Полученное простое вещество вступило в реакцию с сероводородом.
Напишите уравнения четырёх описанных реакций.
Слайд 37№38
Используя метод электронного баланса, составьте уравнение реакции:
FeSO4 + KClO3 + … → Fe2(SO4)3 + … + H2O
Определите окислитель и

восстановитель.




































 Химические средства защиты растений
Химические средства защиты растений Уровень С1 в ГИА
Уровень С1 в ГИА Получение дисперсных систем. Метод конденсации. Метод диспергирования. Эффект Ребиндера. Лекция 11
Получение дисперсных систем. Метод конденсации. Метод диспергирования. Эффект Ребиндера. Лекция 11 Окислительно-восстановительные реакции (1)
Окислительно-восстановительные реакции (1) Фенол
Фенол Гравиметрический анализ (ГА) - метод количественного химического анализа, основанный на точном измерении массы определяемого
Гравиметрический анализ (ГА) - метод количественного химического анализа, основанный на точном измерении массы определяемого Коагуляция в дисперсных системах
Коагуляция в дисперсных системах Презентация на тему Полимеры и их получение
Презентация на тему Полимеры и их получение  Общие физические и химические свойства металлов. 9 класс
Общие физические и химические свойства металлов. 9 класс Основы химической термодинамики и термохимии. Лекция 3
Основы химической термодинамики и термохимии. Лекция 3 Коллоидные растворы
Коллоидные растворы Основи масообміну
Основи масообміну Презентация на тему Электролиз: что полезно знать
Презентация на тему Электролиз: что полезно знать  Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4
Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4 Химические свойства щелочей (тема 6)
Химические свойства щелочей (тема 6) Химическая связь
Химическая связь Хром. Элемент vi группы
Хром. Элемент vi группы Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома
Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома Азотсодержащие органические соединения
Азотсодержащие органические соединения Химические свойства кислорода. Применение кислорода
Химические свойства кислорода. Применение кислорода Карбоновые кислоты
Карбоновые кислоты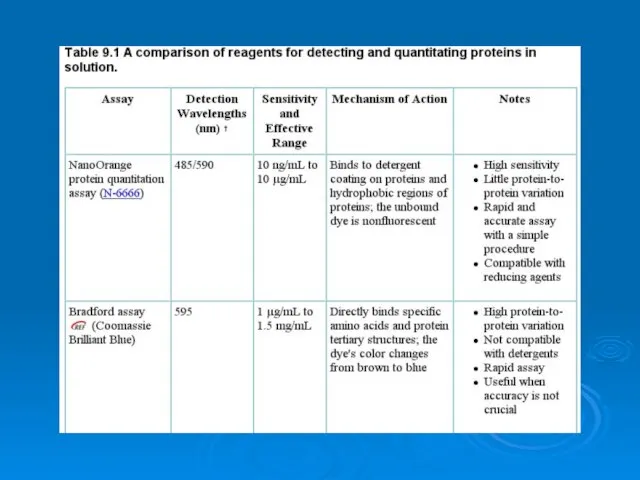 Analysis of proteins
Analysis of proteins Презентация на тему Подгруппа углерода
Презентация на тему Подгруппа углерода  Насыщенные жирные кислоты
Насыщенные жирные кислоты Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1) Вдоль по радуге
Вдоль по радуге Презентация на тему Природные источники углеводородов
Презентация на тему Природные источники углеводородов  кремний и его соединения
кремний и его соединения