Содержание
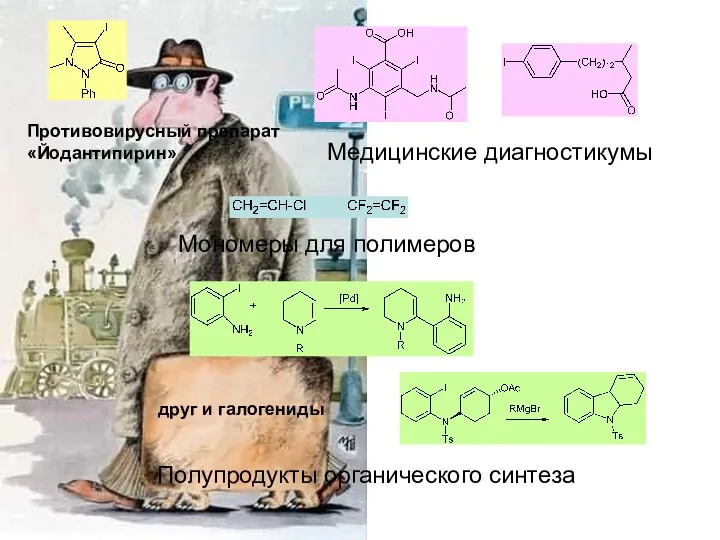
- 2. друг и галогениды Противовирусный препарат «Йодантипирин» Медицинские диагностикумы Полупродукты органического синтеза Мономеры для полимеров
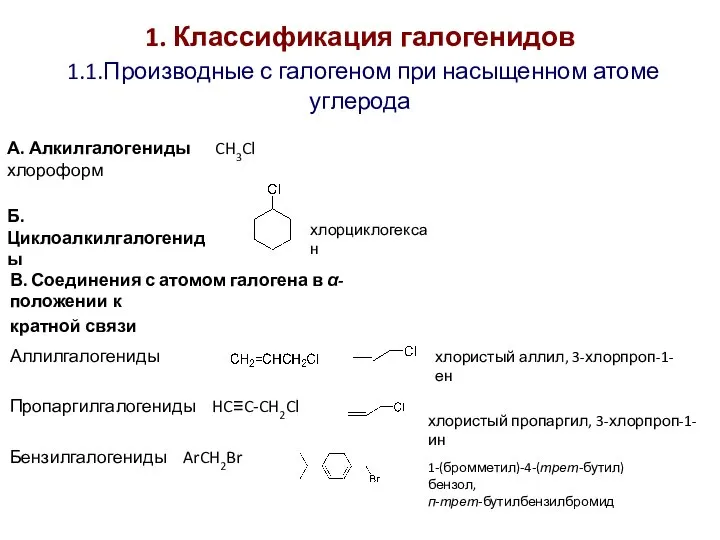
- 3. 1. Классификация галогенидов 1.1.Производные с галогеном при насыщенном атоме углерода А. Алкилгалогениды CH3Cl хлороформ Б. Циклоалкилгалогениды
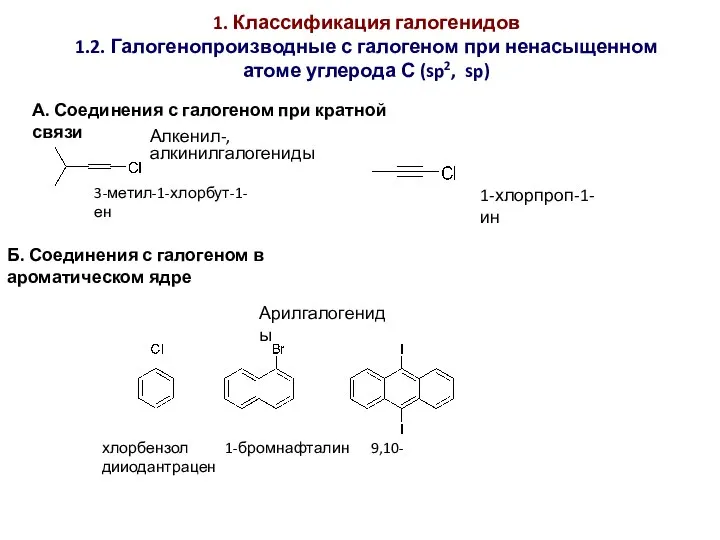
- 4. 1. Классификация галогенидов 1.2. Галогенопроизводные с галогеном при ненасыщенном атоме углерода С (sp2, sp) А. Соединения
- 5. 2. Номенклатура органических галогенидов 2.1. Тривиальная: СНCl3 - хлороформ СHI3 -иодоформ CHBr3 – бромоформ H2C=CСl-CH=CH2 -
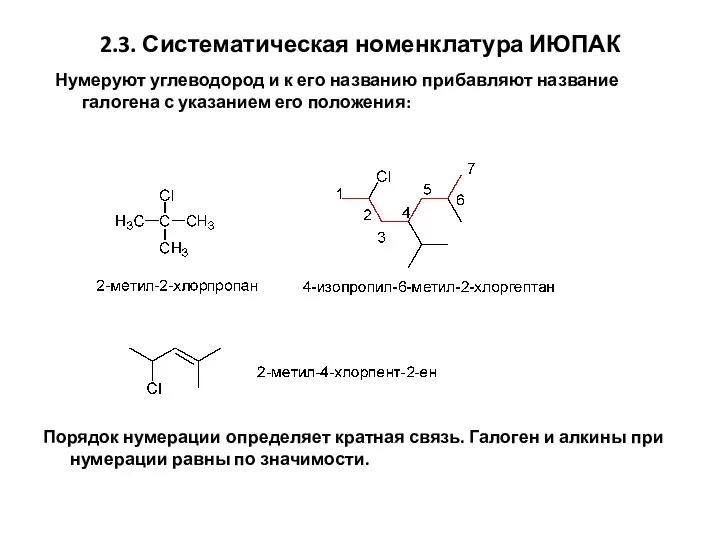
- 6. 2.3. Систематическая номенклатура ИЮПАК Порядок нумерации определяет кратная связь. Галоген и алкины при нумерации равны по
- 7. 5. Физические свойства органических галогенидов Галогенопроизводные углеводородов - бесцветные газы или жидкости со своеобразным запахом; В
- 8. Реакции алкилгалогенидов С2Н5О- - основание, отрывающее Н+ Если в результате элиминирования в качестве основного продукта образуется
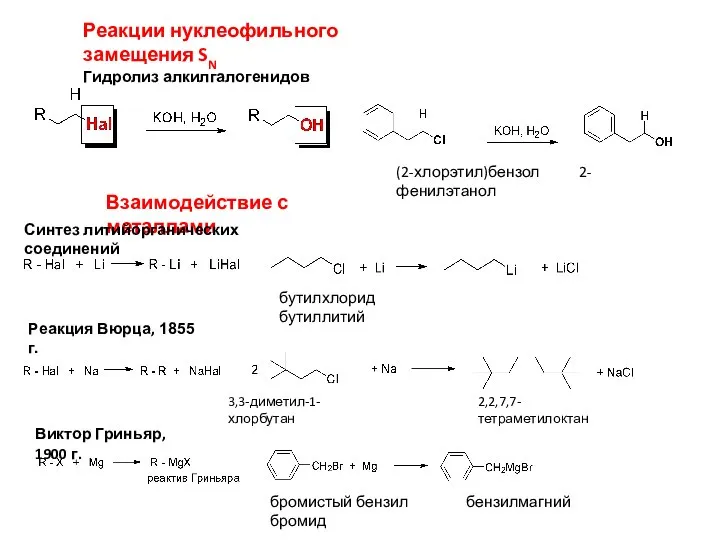
- 9. Реакции нуклеофильного замещения SN Гидролиз алкилгалогенидов (2-хлорэтил)бензол 2-фенилэтанол Взаимодействие с металлами Синтез литийорганических соединений Реакция Вюрца,
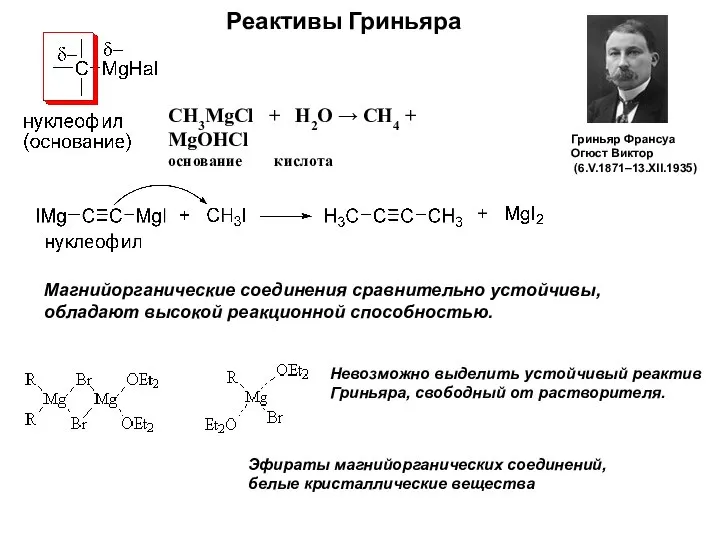
- 10. Реактивы Гриньяра Магнийорганические соединения сравнительно устойчивы, обладают высокой реакционной способностью. Невозможно выделить устойчивый реактив Гриньяра, свободный
- 12. Скачать презентацию



 Закономерности управления каталитическими процессами. Катализ
Закономерности управления каталитическими процессами. Катализ Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Химические свойства металлов
Химические свойства металлов Строение атома
Строение атома Шоу Юный химик
Шоу Юный химик Химические свойства
Химические свойства Анилин. Строение и свойства анилина
Анилин. Строение и свойства анилина Indikatori. R. Boila eksperiments
Indikatori. R. Boila eksperiments VVEDENIE_V_OGRANIChESKUYu_KhIMIYu
VVEDENIE_V_OGRANIChESKUYu_KhIMIYu Презентация
Презентация Химическая кинетика и равновесие
Химическая кинетика и равновесие Генетическая связь веществ. Виды реакций
Генетическая связь веществ. Виды реакций Строение атома. Планетарная модель атома Резерфорда
Строение атома. Планетарная модель атома Резерфорда ОГЭ химия. Основной государственный экзамен
ОГЭ химия. Основной государственный экзамен Уравнения химических реакций
Уравнения химических реакций Вспоминаем химию
Вспоминаем химию Презентация на тему Степень окисления 8 класс
Презентация на тему Степень окисления 8 класс  Углеводороды. Урок-игра
Углеводороды. Урок-игра Ситалл – искусственный поликристаллический материал
Ситалл – искусственный поликристаллический материал Презентация на тему Предельные одноатомные спирты
Презентация на тему Предельные одноатомные спирты  Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота
Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота Вещество и тело. Чистые вещества и смеси
Вещество и тело. Чистые вещества и смеси Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура Растворы. Квалификации химических веществ:
Растворы. Квалификации химических веществ: Исследование воздействия плазмы метана на свойства оксида графена
Исследование воздействия плазмы метана на свойства оксида графена Азот
Азот Изомерия, её виды
Изомерия, её виды Гидролиз солей – частный случай РИО
Гидролиз солей – частный случай РИО