Содержание
- 2. вещество молекула
- 3. Необходимо взять столько граммов вещества, какова относительная атомная или относительная молекулярная масса этого вещества. Как отмерить
- 4. молекула воды 1 моль воды = 18 г Mr(H2O) = 18
- 5. молекула кислорода 1 моль кислорода = 32 г Mr(O2) = 32
- 7. Лоренцо Авогадро (1776 – 1856 гг.) При одинаковых температуре и давлении в равных объёмах идеальных газов
- 10. Число молекул (N)
- 11. Количество вещества (n) Молярная масса — физическая величина, которая равна отношению массы вещества к его количеству.
- 12. М — молярная масса M = г/моль киломоль: 1 кмоль = 1000 моль миллимоль: 1 ммоль
- 13. n=m/М (по массе) n=N/Na (по числу частиц) n=V/Vm (по объему) Формулы для определения количества вещества
- 14. Молярный объем V=Vm·n V=m:ρ n =V/ Vm m=M· V/ Vm объем 1 моля газа при н.у.
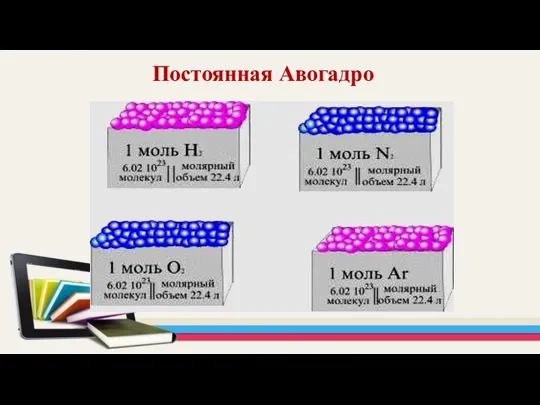
- 15. Постоянная Авогадро
- 16. Задача 1. Сколько молекул содержит углекислый газ количеством вещества 2,5 моль? Дано: Решение.
- 17. Задача: Какую массу имеют 2 моль воды? Дано: n(H2O)=2 моль Найти: m-? Решение: 1) M(H2O) =
- 18. Задача 2. Какова масса железа (в граммах), соответствующая количеству вещества 0,25 моль? Дано: m(Fe) – ?
- 19. Задача: Определите количество вещества содержащееся в 10 г СаО? Дано: m(СаO)=10г. m= M· n n -?
- 20. Задача 2. Какова масса железа (в граммах), соответствующая количеству вещества 0,25 моль? Дано: m(Fe) – ?
- 21. Задача: Определите число молекул в 0,35 моль воды? Дано: n(Н2O)=0,35 моль N = n *Na n=N/Na
- 22. Задача 3. Определите массу хлора (Cl), содержащегося в 29,25 г поваренной соли (NaCl). Дано: M(Na) =
- 23. Задача: Чему равно число атомов 0,75 моль серы? N = n *Na N (S)= 0,75 моль
- 24. Задача 3. Определите массу хлора (Cl), содержащегося в 29,25 г поваренной соли (NaCl). Дано: M(Na) =
- 25. Дано: N (MgO) = 18 x 1023 N (S) = 3 x 1023 n (MgO) -
- 27. Скачать презентацию






















 Спирты. Тест
Спирты. Тест Металлы. Общие свойства
Металлы. Общие свойства Презентация на тему Химические свойства алкенов
Презентация на тему Химические свойства алкенов  Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия
Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия  Химия цвета
Химия цвета Зола. Свойства щёлока
Зола. Свойства щёлока Вещества в окружающей природе и в технике
Вещества в окружающей природе и в технике Относительная атомная масса элементов
Относительная атомная масса элементов Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Полимерные материалы
Полимерные материалы Аммиак. Состав вещества
Аммиак. Состав вещества Подгруппа алюминия
Подгруппа алюминия Углеводороды
Углеводороды Опыты по теме Свойства основных классов неорганических соединений
Опыты по теме Свойства основных классов неорганических соединений Атомы, молекулы и ионы
Атомы, молекулы и ионы Алмазы
Алмазы Альдегиды, их химические и физические свойства. Получение и применение альдегидов
Альдегиды, их химические и физические свойства. Получение и применение альдегидов Описание молекул
Описание молекул Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Химическое равновесие в гомогенных системах
Химическое равновесие в гомогенных системах Щелочные металлы
Щелочные металлы Составление ионных уравнений
Составление ионных уравнений Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения
Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения teoriya_elektroliticheskoy_dissotsiatsii
teoriya_elektroliticheskoy_dissotsiatsii Семь доисторических металлов
Семь доисторических металлов Презентация на тему Применение спиртов
Презентация на тему Применение спиртов  Белки. Структуры белков
Белки. Структуры белков Обобщающий урок по теме «Соединения химических элементов» 8 класс.
Обобщающий урок по теме «Соединения химических элементов» 8 класс.