Содержание
- 2. Урок по химии в 8-м классе. Обобщение и систематизация знаний по теме "Изменения, происходящие с веществами"
- 3. Аукцион знаний. Укажите о каких явлениях, физических или химических, идет речь в следующих высказываниях поэтов. Ответ
- 4. Когда металл в крутые формы льем, Мне верится, что оживут в металле Горячие полдневные поля. Кипит
- 5. 1.Каковы признаки химических реакций? 2.Какие условия необходимы для проведения химических реакций? 3.Когда и кем был открыт
- 6. Эта красавица всем вам знакома С ней вы встречаетесь в школе и дома, Бесцветна, чиста почти,
- 7. Я известна с давних пор и имею спрос, Опусти меня в раствор, В медный купорос. Изменить
- 8. 4.Напишите уравнения реакций а) Нитрат серебра + Хлорид железа (III) ? Хлорид серебра + Нитрат железа
- 9. Расставьте коэффициенты и определите тип химических реакций 1. CaO + HCl ? CaCl2 + H2O 2.
- 10. 1. CaO + 2HCl = CaCl2 + H2O 2. 2K + 2H2O = 2KOH + H2
- 12. Физминутка Вносим в почву мы фосфаты. Не забудем и нитраты. Ну, а осенью, друзья Испеку пирог
- 13. Решите задачу. Рассчитайте объём водорода(н.у.), полученного при взаимодействии 14,4 г. цинка, содержащего 10% примесей с избытком
- 14. Решение задачи. Дано: M(Zn) = 14,4 г. ωпр = 10% н.у. V(H2) - ? Zn +
- 15. 1) Выберите реакцию разложения. 2) Найдите реакцию обмена. 3) Выберите реакцию соединения. 4) Найдите реакцию замещения.
- 16. а) 2NaNO3 = 2NaNO2 + O2 б) KCl + AgNO3 = KNO3 + AgCl в) SiO2
- 17. РЕФЛЕКСИЯ Вырази свои мысли: 1.На уроке я работал(а): Активно/ пассивно 2.Своей работой на уроке я: Доволен/
- 19. Скачать презентацию








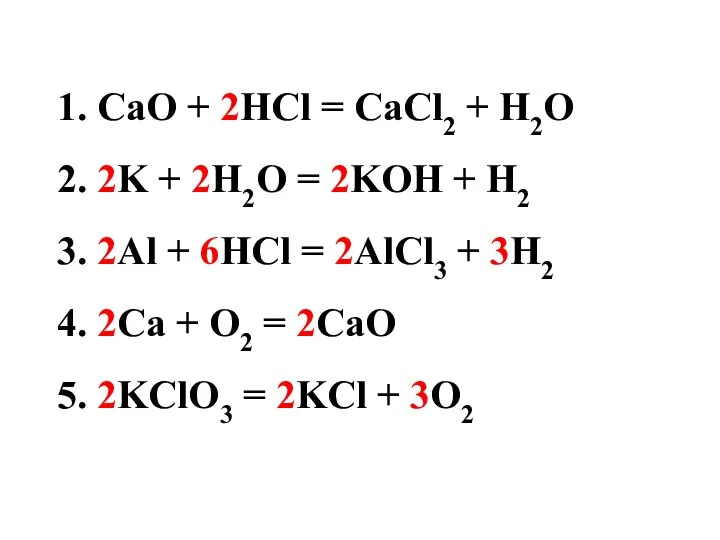







 Закалка без полиморфного превращения
Закалка без полиморфного превращения Презентация по Химии "Химическая номенклатура и филология"
Презентация по Химии "Химическая номенклатура и филология"  Щелочно-земельные металлы и магний
Щелочно-земельные металлы и магний Обобщение знаний по курсу органической химии
Обобщение знаний по курсу органической химии Нефть и её переработка
Нефть и её переработка Калифорний Cf
Калифорний Cf Амины. Номенклатура
Амины. Номенклатура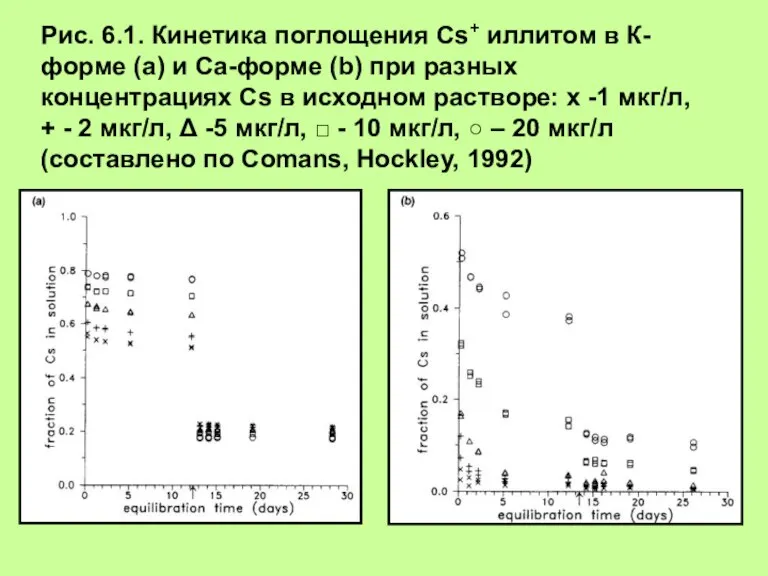 Определение коэффициента селективности при бинарном обмене
Определение коэффициента селективности при бинарном обмене Коррозия металлов и ГЭ
Коррозия металлов и ГЭ Ar, Mr
Ar, Mr Алкины
Алкины Срез знаний по химии
Срез знаний по химии Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Турнир Знатоков Химии
Турнир Знатоков Химии Типичные реакции кислот
Типичные реакции кислот Активизация познавательной деятельности на уроках химии при работе с МГП (малыми графическими пособиями)
Активизация познавательной деятельности на уроках химии при работе с МГП (малыми графическими пособиями) Презентация на тему Фосфорная кислота и ее свойства
Презентация на тему Фосфорная кислота и ее свойства  Общая характеристика элементов VII группы главной подгруппы. Хлор
Общая характеристика элементов VII группы главной подгруппы. Хлор Навчальний проект Дослідження зміни концентрації CO2 у класній кімнаті під час занять
Навчальний проект Дослідження зміни концентрації CO2 у класній кімнаті під час занять 8. ионная связь
8. ионная связь Железо - основа всего мира
Железо - основа всего мира Теория электролитической диссоциации. Контрольный тест
Теория электролитической диссоциации. Контрольный тест Предмет химии, простые и сложные вещества
Предмет химии, простые и сложные вещества Массовые доли растворенного вещества
Массовые доли растворенного вещества Склероглюкан
Склероглюкан Синтетические моющие средства
Синтетические моющие средства Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Окислительно-восстановительные реакции
Окислительно-восстановительные реакции