Содержание
- 2. Для этого необходимо выполнить составить уравнения реакций в молекулярном виде Определить степень окисления элементов В реакциях,
- 3. Составим молекулярные уравнения реакций 2Cu + O2 ? 2CuO CuO + 2HCl ? CuCl2 + H2O
- 4. Определим степень окисления элементов 2Cu0 + O20? 2Cu+2O-2 Cu +2 O-2 + 2H+Cl- ? Cu+2Cl2-1 +
- 5. Степень окисления элементов изменилась только в первой реакции 2Cu0 + O20? 2Cu+2O-2 Определим переход электронов Найдем
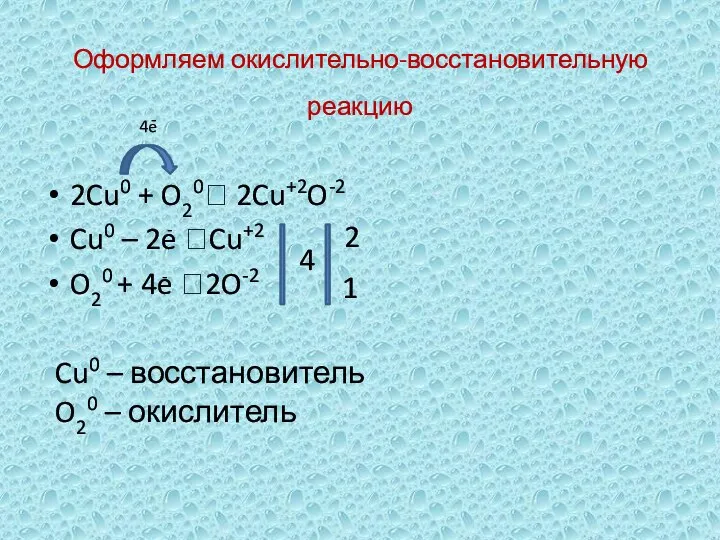
- 6. Оформляем окислительно-восстановительную реакцию 2Cu0 + O20? 2Cu+2O-2 Cu0 – 2e ?Cu+2 O20 + 4e ?2O-2 4
- 7. Составляем полные ионные уравнения CuO + 2H+ + 2Сl - ? Cu+2 + 2Cl - +
- 8. Составляем краткие ионные уравнения CuO + 2H+ ?Cu+2 + H2O Cu+2 + 2OH - ? Cu(OH)2
- 10. Скачать презентацию






 Органическая химия
Органическая химия Трансляция. Активирование аминокислоты
Трансляция. Активирование аминокислоты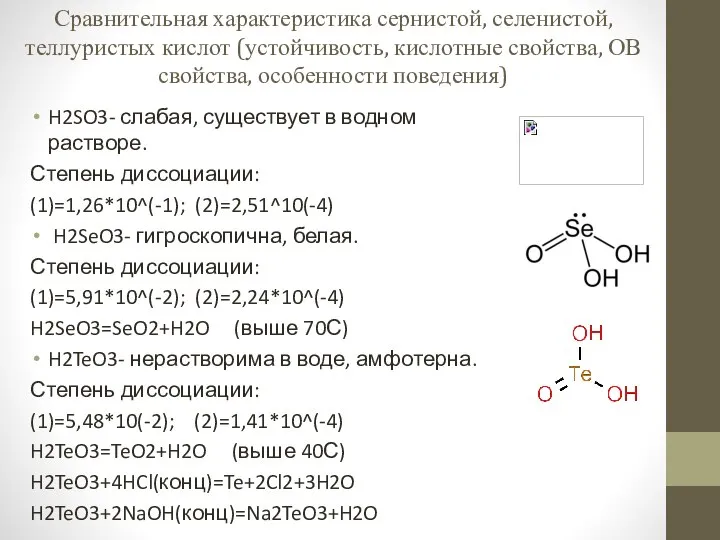 Сравнительная характеристика сернистой, селенистой, теллуристых кислот
Сравнительная характеристика сернистой, селенистой, теллуристых кислот Химические реакции
Химические реакции Кинетика и равновесие. Лекция №3
Кинетика и равновесие. Лекция №3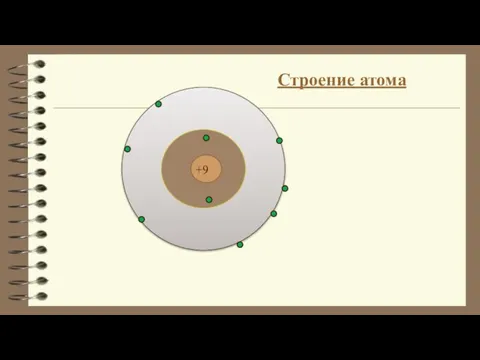 Строение атома
Строение атома Химия элементов
Химия элементов Химик белемнәрне тормышта куллану
Химик белемнәрне тормышта куллану Ацетиленди гидратациялау
Ацетиленди гидратациялау Химический элемент азот N и его соединения
Химический элемент азот N и его соединения Презентация на тему Аллотропные видоизменения неметаллов
Презентация на тему Аллотропные видоизменения неметаллов  Химическая связь
Химическая связь Основы строения и свойства материалов
Основы строения и свойства материалов Влияние бытовой химии на здоровье человека
Влияние бытовой химии на здоровье человека Нуклеиновые кислоты
Нуклеиновые кислоты Про краски
Про краски Углеродистые стали
Углеродистые стали Реакции ионного обмена и условия их протекания
Реакции ионного обмена и условия их протекания Экстракционное разделение радионуклидов
Экстракционное разделение радионуклидов Альдегиды и кетоны
Альдегиды и кетоны Осмотическое давление
Осмотическое давление Степень окисления
Степень окисления Условия среды, вызывающие коррозию металла
Условия среды, вызывающие коррозию металла Физические и химические явления в химии. Признаки химических реакций
Физические и химические явления в химии. Признаки химических реакций Химическая связь. Ковалентная связь
Химическая связь. Ковалентная связь Замедленное коксование гудрона
Замедленное коксование гудрона Структура, свойства и термическая обработка железоуглеродистых сплавов
Структура, свойства и термическая обработка железоуглеродистых сплавов Самородные металлы
Самородные металлы