Содержание
- 2. Цели урока: Обобщить и закрепить знания о классификации, номенклатуре, свойствах органических и неорганических кислот Научить объяснять
- 3. Определение кислот Кислоты в природе Классификация кислот Химические свойства кислот Получение кислот Применение кислот План урока:
- 4. Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только гидратированные ионы водорода (H3O+). 1.
- 5. В 1923г. была предложена протолитическая теория Бернстедом-Лаури. Кислоты – это молекулы или ионы, которые являются донорами
- 6. 2. Кислоты в природе Кислотные дожди (азотная, серная кислоты) Кислоты в пище (яблочная, щавелевая, лимонная, молочная,
- 7. Паук педипальпида стреляет в своих врагов струйкой, состоящей из уксусной кислоты. Плоские тысяченожки используют яд пострашнее
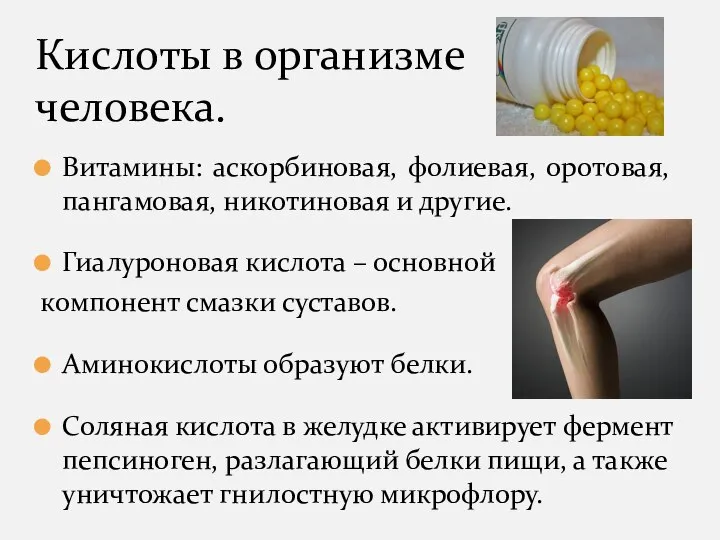
- 8. Витамины: аскорбиновая, фолиевая, оротовая, пангамовая, никотиновая и другие. Гиалуроновая кислота – основной компонент смазки суставов. Аминокислоты
- 9. По составу: Кислородосодержащие: НNO3, H2SO3; Бескислородные: HCl, H2S. По основности: (основность кислоты определяется числом катионов, которые
- 10. Взаимодействие с металлами, расположенными в электрохимическом ряду напряжений металлов до водорода. 4. Химические свойства кислот:
- 11. Взаимодействие с основными и амфотерными оксидами.
- 12. Взаимодействие с растворимыми и нерастворимыми основаниями. Могут образовывать средние и кислые соли. Это реакции нейтрализации.
- 13. Взаимодействие с солями Сильная кислота способна вытеснить слабую кислоту даже из нерастворимой соли.
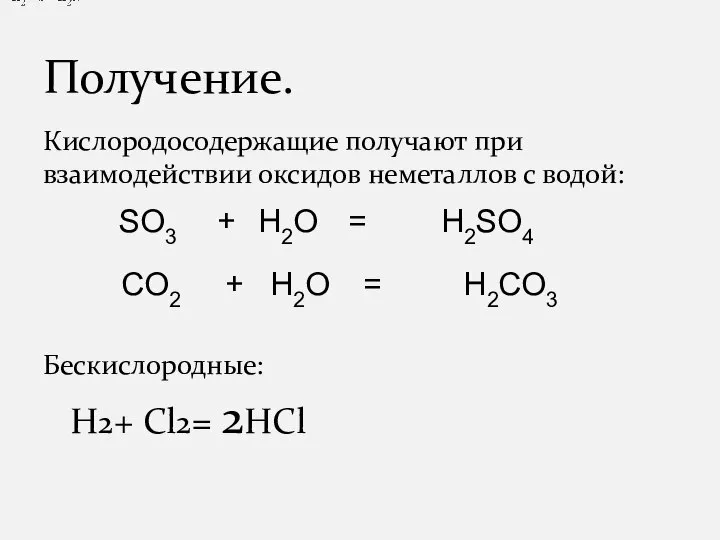
- 14. Кислородосодержащие получают при взаимодействии оксидов неметаллов с водой: Бескислородные: H2+ Cl2= 2HCl Получение.
- 15. Соляная кислота Для растворения окалины и ржавчины при никелировании, хромировании, цинковании и т.п. стальных и чугунных
- 16. Серная кислота Для производства фосфорных и азотных удобрений В производстве взрывчатых веществ Искусственных волокон Красителей Пластмасс
- 17. Азотная кислота Производство азотных удобрений Взрывчатых веществ Лекарственных веществ Красители Пластмассы Искусственные волокна
- 18. Задание 1. Напишите формулы и дайте характеристику кислотам на основе их классификации: кремниевая кислота, плавиковая кислота.
- 20. Скачать презентацию















 Вымораживание воды
Вымораживание воды Галогены. Свойства фтора, брома, йода
Галогены. Свойства фтора, брома, йода Железо как химический элемент
Железо как химический элемент Углеводы
Углеводы Презентация на тему Электролитическая диссоциация (8 класс)
Презентация на тему Электролитическая диссоциация (8 класс)  Алюминий и сплавы алюминия
Алюминий и сплавы алюминия Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Презентация на тему Палладий
Презентация на тему Палладий  Коллоидно-химическая теория схватывания и твердения вяжущих веществ
Коллоидно-химическая теория схватывания и твердения вяжущих веществ Новейшие достижения в области высокомолекулярных соединений
Новейшие достижения в области высокомолекулярных соединений Углерод и его свойства
Углерод и его свойства Презентация на тему Химические волокна
Презентация на тему Химические волокна  Соединения алюминия
Соединения алюминия Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды
Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды Электролиз
Электролиз Превращения веществ
Превращения веществ Периодическая система химических элементов. Периоды. Группы
Периодическая система химических элементов. Периоды. Группы Знаки химических элементов
Знаки химических элементов Химическая кинетика. Экзаменационные вопросы
Химическая кинетика. Экзаменационные вопросы СПИРТЫ, ФЕНОЛЫ
СПИРТЫ, ФЕНОЛЫ Презентация на тему Общая характеристика неметаллов
Презентация на тему Общая характеристика неметаллов  Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Процесс образования неметаллических включений в стали
Процесс образования неметаллических включений в стали Многообразие веществ
Многообразие веществ Биосинтез пиримидиновых нуклеотидов
Биосинтез пиримидиновых нуклеотидов Химические свойства основных оксидов. 9 класс
Химические свойства основных оксидов. 9 класс Предельные углеводороды (алканы)
Предельные углеводороды (алканы)